课标要求 1
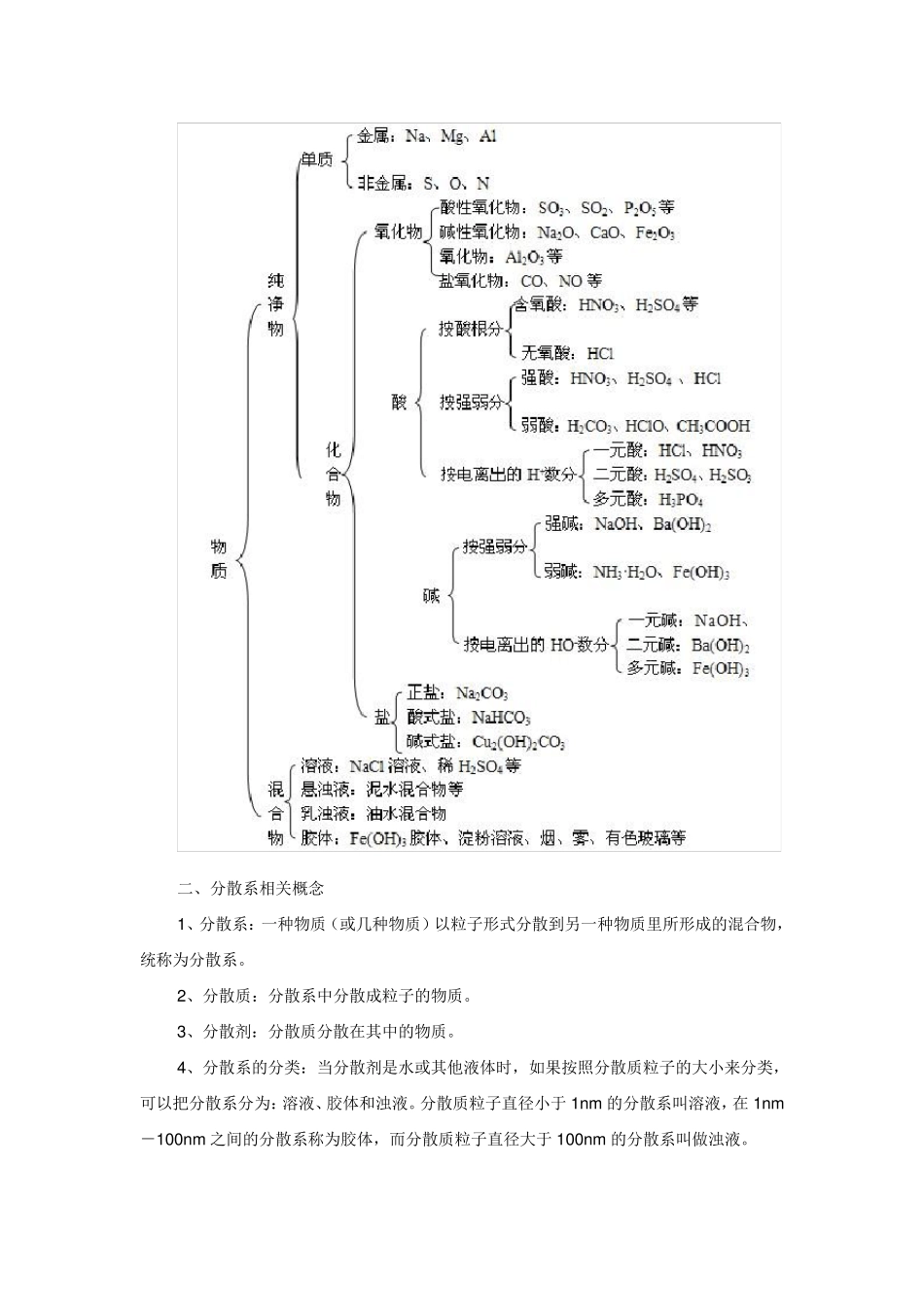
能根据物质的组成和性质对物质进行分类 2
知道根据分散质粒子的大小,把分散系分为溶液、胶体和浊液 3
知道用丁达尔效应区分溶液和胶体 4
知道酸、碱、盐在溶液中能发生电离,能正确书写强酸、强碱和可溶性盐的电离方程式
通过实验事实认识离子反应的意义及其发生的条件,能正确书写常见的离子方程式
能够根据溶液中存在的离子判断是否发生复分解反应,从而判断溶液中离子能否大量共存
了解 Cl-、SO42-、CO32-等常见离子的检验方法
了解常见变化的分类方法
根据实验事实了解氧化还原反应的本质是电子的转移
举例说明生产、生活中常见的氧化还原反应
熟记常见物质的化合价,能根据反应前后元素化合价有无变化,判断反应是否为氧化还原反应
能判断氧化剂和还原剂
要点精讲 一、物质的分类 二、分散系相关概念 1、分散系:一种物质(或几种物质)以粒子形式分散到另一种物质里所形成的混合物,统称为分散系
2、分散质:分散系中分散成粒子的物质
3、分散剂:分散质分散在其中的物质
4、分散系的分类:当分散剂是水或其他液体时,如果按照分散质粒子的大小来分类,可以把分散系分为:溶液、胶体和浊液
分散质粒子直径小于 1nm 的分散系叫溶液,在 1nm-100nm 之间的分散系称为胶体,而分散质粒子直径大于 100nm 的分散系叫做浊液
下面比较几种分散系的不同: 注意:三种分散系的本质区别:分散质粒子的大小不同
三、胶体 1、胶体的定义:分散质粒子直径大小在10-9~10-7m 之间的分散系
2、胶体的分类: ①根据分散质微粒组成的状况分类: 如:胶体胶粒是由许多等小分子聚集一起形成的微粒,其直径在1nm~100nm 之间,这样的胶体叫粒子胶体
②根据分散剂的状态划分: 如:烟、云、雾等的分散剂为气体,这样的胶体叫做气溶胶;AgI