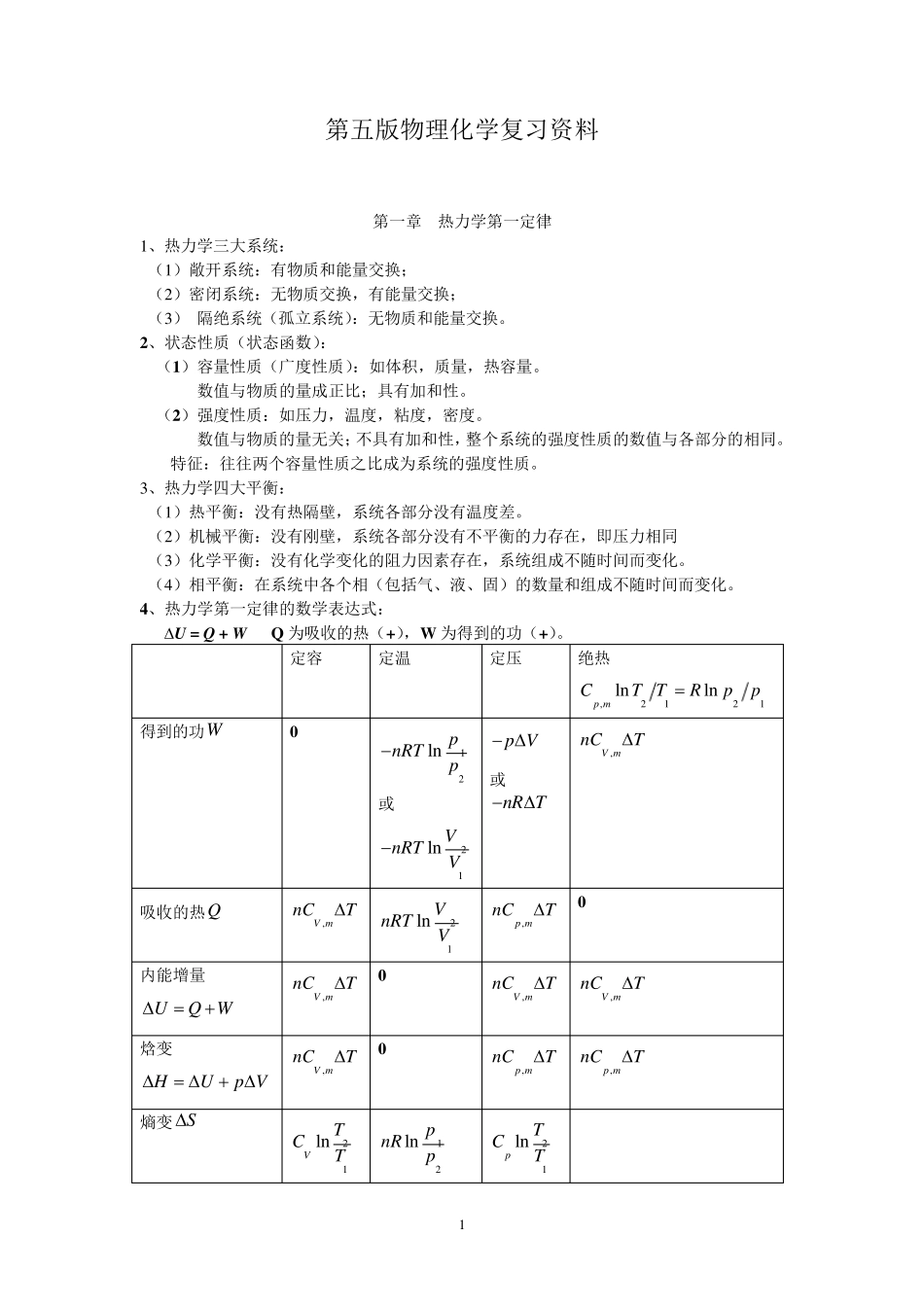
1 第五版物理化学复习资料 第一章 热力学第一定律 1、热力学三大系统: (1)敞开系统:有物质和能量交换; (2)密闭系统:无物质交换,有能量交换; (3) 隔绝系统(孤立系统):无物质和能量交换。 2、状态性质(状态函数): (1)容量性质(广度性质):如体积,质量,热容量。 数值与物质的量成正比;具有加和性。 (2)强度性质:如压力,温度,粘度,密度。 数值与物质的量无关;不具有加和性,整个系统的强度性质的数值与各部分的相同。 特征:往往两个容量性质之比成为系统的强度性质。 3、热力学四大平衡: (1)热平衡:没有热隔壁,系统各部分没有温度差。 (2)机械平衡:没有刚壁,系统各部分没有不平衡的力存在,即压力相同 (3)化学平衡:没有化学变化的阻力因素存在,系统组成不随时间而变化。 (4)相平衡:在系统中各个相(包括气、液、固)的数量和组成不随时间而变化。 4、热力学第一定律的数学表达式: U = Q + W Q 为吸收的热(+),W 为得到的功(+)。 定容 定温 定压 绝热 ,2121lnlnp mCT TRpp 得到的功W 0 12ln pnRTp 或21ln VnRTV p V 或nR T ,V mnCT 吸收的热Q ,V mnCT 21ln VnRTV ,p mnCT 0 内能增量 UQW ,V mnCT 0 ,V mnCT ,V mnCT 焓变 HUp V ,V mnCT 0 ,p mnCT ,p mnCT 熵变 S 21lnVTCT 12ln pnRp 21lnpTCT 2 或21ln VnRV 亥姆霍兹(定温定容) AUT S pdV 吉布斯(定温定压) GHT S 21ln pnRTp 12、在通常温度下,对理想气体来说,定容摩尔热容为: 单原子分子系统 ,V mC= 32 R 双原子分子(或线型分子)系统 ,V mC= 52 R 多原子分子(非线型)系统 ,V mC632 RR 定压摩尔热容: 单原子分子系统 ,52p mCR 双原子分子(或线型分子)系统 ,,p mV mCCR,72p mCR 多原子分子(非线型)系统 ,4p mCR 可以看出:,,p mVmCCR 13、,p mC的两种经验公式:,2p mCabTcT (T 是热力学温度,a,b,c,c’ 是经 ,2'p mcCabTT 验常数,与物质和温度范围有关) 14、在发生一绝热过程时,由于0Q,于是dUW 理想气体的绝热可逆过程,有:,V mnCdTpdV 22,11lnlnV mTVCRTV 21,12ln,lnV mpVCCp mpV ,,p mV mCpVC 常数 =>...