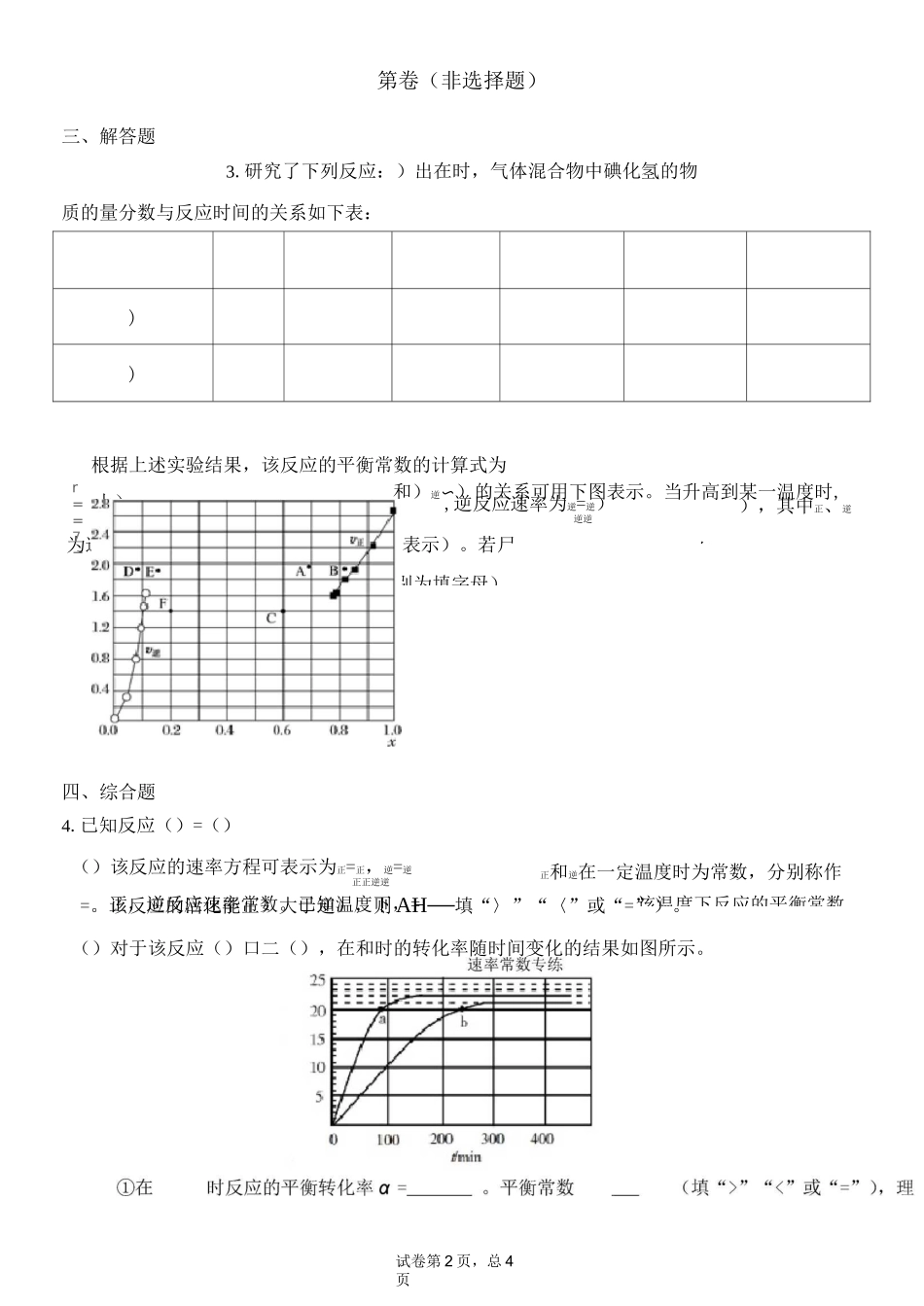
速率常数专练试卷第 1 页,总 4页一、单选题1.Bodensteins 研究了反应 2HI(g)・、I2(g)+H2(g),某温度下,上述反应中,正反应速率为 uT=k 正c2(HI),逆反应速率为 u%=k 逆 C(I2)・C(H2),,其中 k 正、k 逆为速率常数,根据以上内容得出的结论,正正逆逆 22 正逆不正确的是A. 反应物浓度越大,正反应速率越大B.生成物浓度越大,逆反应速率越大C.该反应的平衡常数 K=k 正/k 逆正逆D. 速率常数的大小与反应程度无关系二、多选题2.恒容条件下,1molSiHCl3发生如下反应:2SiHC13(g)==SiH2Cl2(g)+SiC14(g)。已知:v 正=»消耗(SiHCl3)=k 正x2(SiHCl3),v 逆=2v 消耗(SiH2Cl2)=k 逆x(SiH2Cl2)x(SiCl4),k 正、k 逆分别为正、逆向反应速率常数(仅与温度有关),x 为物质的量分数。如图是不同温度下 x(SiHCl3)随时间的变化。下列说法正确的是A. 该反应为放热反应,v