1/55 GMP 内审检查表(1) Q A 序 号 项目 检查内容 检查情况 检查说明 符合 基本符合 不符合 1 组织机构与职责 部门组织机构图、部门职责、岗位职责经起草、批准
建立符合药品质量管理要求的质量目标
部门职责应明确:质量管理部门应当参与所有与质量有关的活动,负责审核所有与生产质量有关的文件;质量管理部们的职责不得委托给其他部门人员,质量管理部门独立履行职责,不受其他部门及企业负责人的干扰
是否具有适当的资质并经培训合格的人员;查看在岗人员基本情况,包括年龄、职务、工作职责、专业、职称、工作年限等
质量总监、质量受权人、质量保证部经理的资质和工作经历,是否符合要求
2 文件管理 是否有文件管理的操作规程,规定文件的起草、修订、审核、批准、替换或撤销、复制、保管和销毁等程序
文件分发、收回、撤销、复制、销毁应有记录
分发、使用的文件应当为批准的现行文本
有文件编号编制的管理文件,确保每个文件编号(或代码)的唯一性
文件的起草、修订、审核、批准均有适当的人员签名并注明日期
文件应当标明题目、种类、目的、文件编号、版本号、颁发部门、生效 日期、分发部门、制定人、审核人、批准人、变 更 历史 等
文件的文字 应当确切 、清 晰 、易 懂
与生产质量有关的文件和记录的复制、分发应得到 有效 的控 制
文件应当定期审核、修订
文件应当分类存 放 、条 理分明,便 于 查阅
有下 列 活动的操作规程:确认 和验 证,设 备 的装 配 和校 准,厂 房 和设 备 的维护 、清 洁 和消 毒 ,培训、更 衣 及卫 生等与人员相 关的事 宜 ,环 境 监测 ,虫 害控 制,变 更 控 制,偏 差 处 理,投 诉 ,药品召 回,退 货
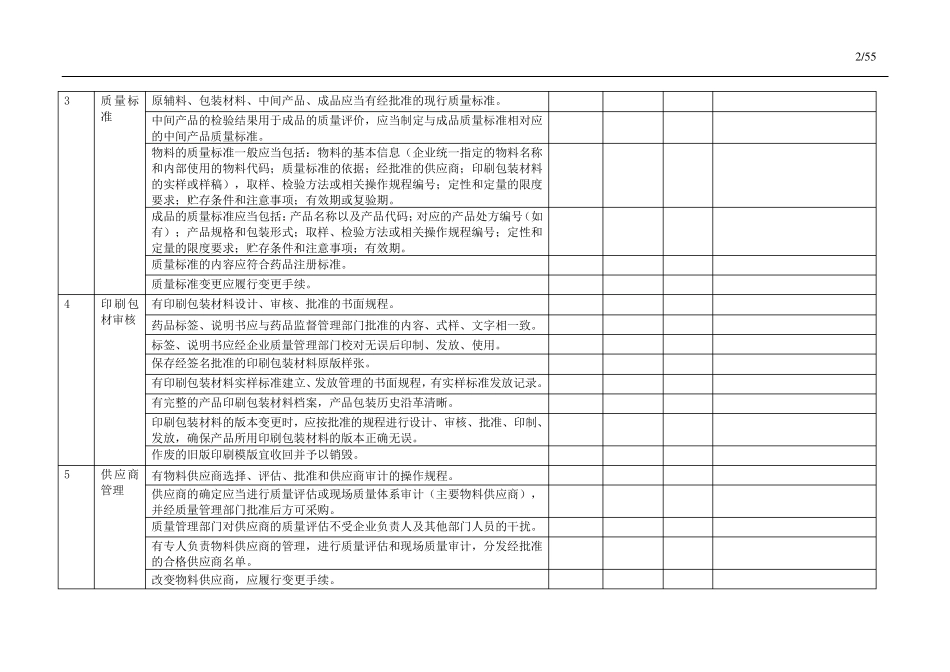
2 /5 5 3 质量标准 原辅料、包装材料、中间产品、成品应当有经批准的现行质量标准
中间产品的检验结果用