中国3000 万经理人首选培训网站 不合格药材(品)处理程序及报告制度 1 .目的 规范不合格品的控制管理,确保不合格品不出厂销售
2 .适用范围 适用于药品的加工生产、包装、贮藏及销售的质量管理
3 .职责 (1)各加工生产、包装、贮藏及销售员发现不合格情况立向质管部报告
(2)质管部负责不合格品的审查、确认与上报、处理,并监督销毁与记录
(3)仓贮部专人负责不合格品专账保管及其报损销毁
4 .程序 4.1 不合格的范围界定:凡药材来源、性状、鉴别、检查、浸出物、制法、含量测定、微生物测定、药品包装、标签及说明书查验等项中,任一项不符合法定质量标准或国家药监局有关规定的药材、药品、均判定为不合格药品
还包括 SFDA 禁止使用或明令淘汰的药品
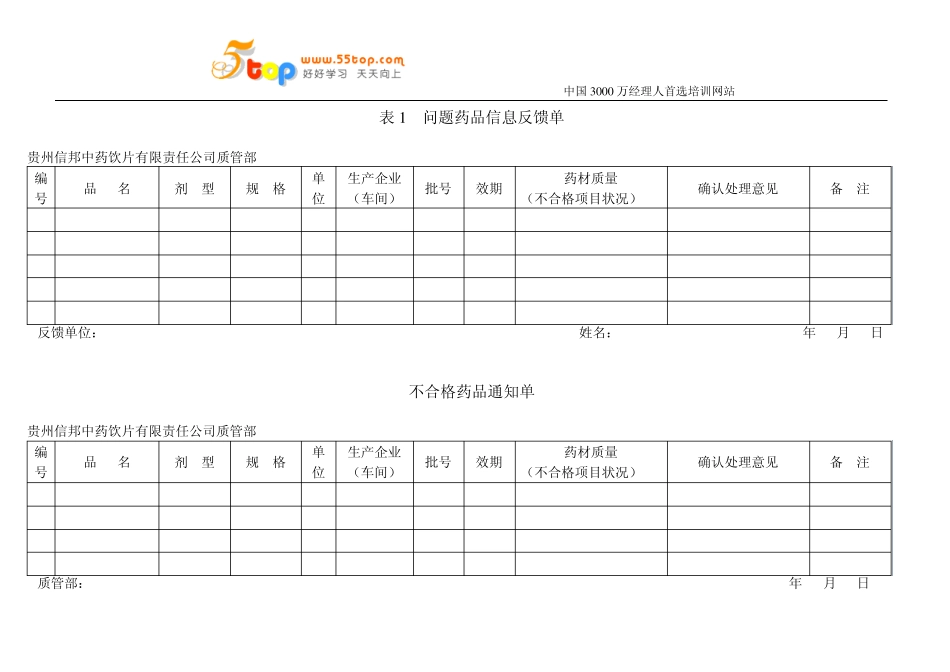
4.2 不合格品的报告与确认 4.2.1 原药材进入生产加工前,应对其质量进行查检清理,对来源、性状不符合要求,及剔除部分等不合格品,应立即填写《信息反馈单》,标明品名、规格、批号、数量及挂红牌,向质管部报告
4.2.2 对药材加工中半成品、成品及包装或发货销售中发现的不合格情况,应将不合格 物挂红牌,后立即填写《信息反馈单》向质管部报告
4.2.3 质管部接到《信息反馈单》后,应于12h 内对报告药品质量进行确认,必要时报送药检所检验
依据检验结果确定不合格品
向仓储 部发《不合格品通知单》并由质管部挂红牌封存于不合格品(区)库
4.3 对不合格品的处理
4.3.1 若是包装破损,药品内在质量未受污染或标签不合格品的非内在质量不合格品,应重交回生产加工部,更换包装或标签
4.3.2 若为药品质量受损的不合格,应由发现部门填《不合格药品报损审批表》经生产部、质管部、财务部、总经理批准同意后报损
4.3.3 质量不合格药品由质管部派员监督销毁,并作好《不合格药品销毁记录》,记录销毁药品、数量、销毁地点、销毁方式