下载后可任意编辑《医疗器械生产质量管理法律规范》无菌医疗器械检查自查报告自查企业名称盖章:自查产品名称(页面不够可附页)自查人员自查日期:企业负责人(签名)职务:(本表由检查人员填写)《医疗器械生产质量管理法律规范》无菌医疗器械现场检查记录表检查企业名称检查地址检查产品名称(含型号、规格)检查人员检查日期上海市食品药品监督管理局编制1下载后可任意编辑说明:根据《医疗器械生产质量管理法律规范》和《医疗器械生产质量管理法律规范无菌医疗器械实施细则》的要求,为了提高企业对质量管理体系自我检查的能力,统一检查标准,制定本自查报告以供参考
企业在申请质量管理体系考核之前,应根据本报告要求进行全面自查,并按要求逐项填写
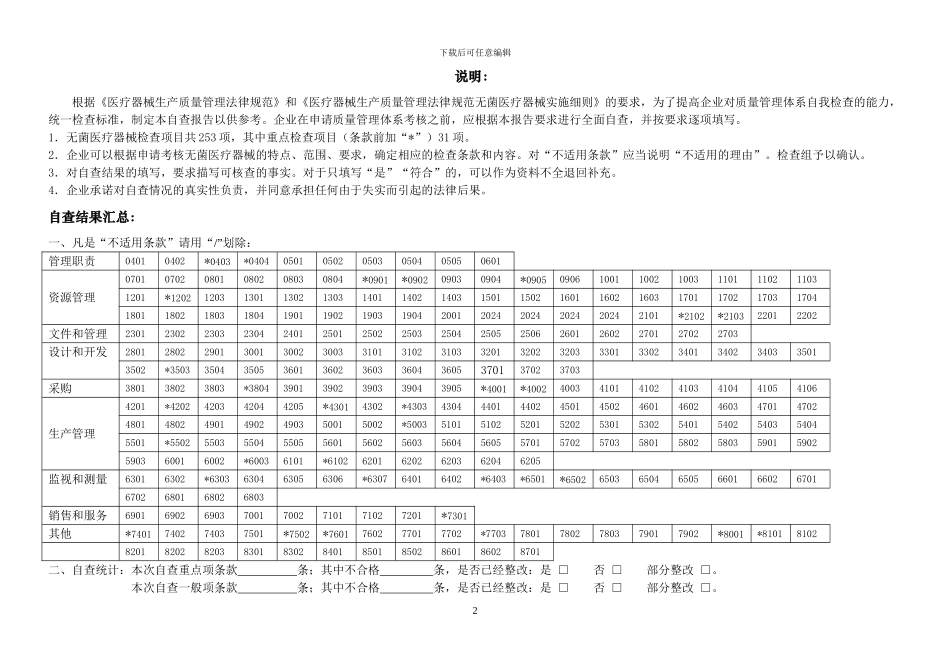
1.无菌医疗器械检查项目共 253 项,其中重点检查项目(条款前加“*”)31 项
2.企业可以根据申请考核无菌医疗器械的特点、范围、要求,确定相应的检查条款和内容
对“不适用条款”应当说明“不适用的理由”
检查组予以确认
3.对自查结果的填写,要求描写可核查的事实
对于只填写“是”“符合”的,可以作为资料不全退回补充
4.企业承诺对自查情况的真实性负责,并同意承担任何由于失实而引起的法律后果
自查结果汇总:一、凡是“不适用条款”请用“/”划除:管理职责04010402*0403*0404050105020503050405050601资源管理070107020801080208030804*0901*090209030904*090509061001100210031101110211031201*1202120313011302130314011402140315011502160116021603170117021703170418011802180318041901190219031904200120242024202420242101*2102*2103220