溶解热的测定 1 引言 1
1 实验目的 1
测量硝酸钾在不同浓度水溶液的溶解热,求硝酸钾在水中溶解过程的各种热效应
掌握量热装置的基本组合及电热补偿法测定热效应的基本原理
复习和掌握常用的测温技术 1
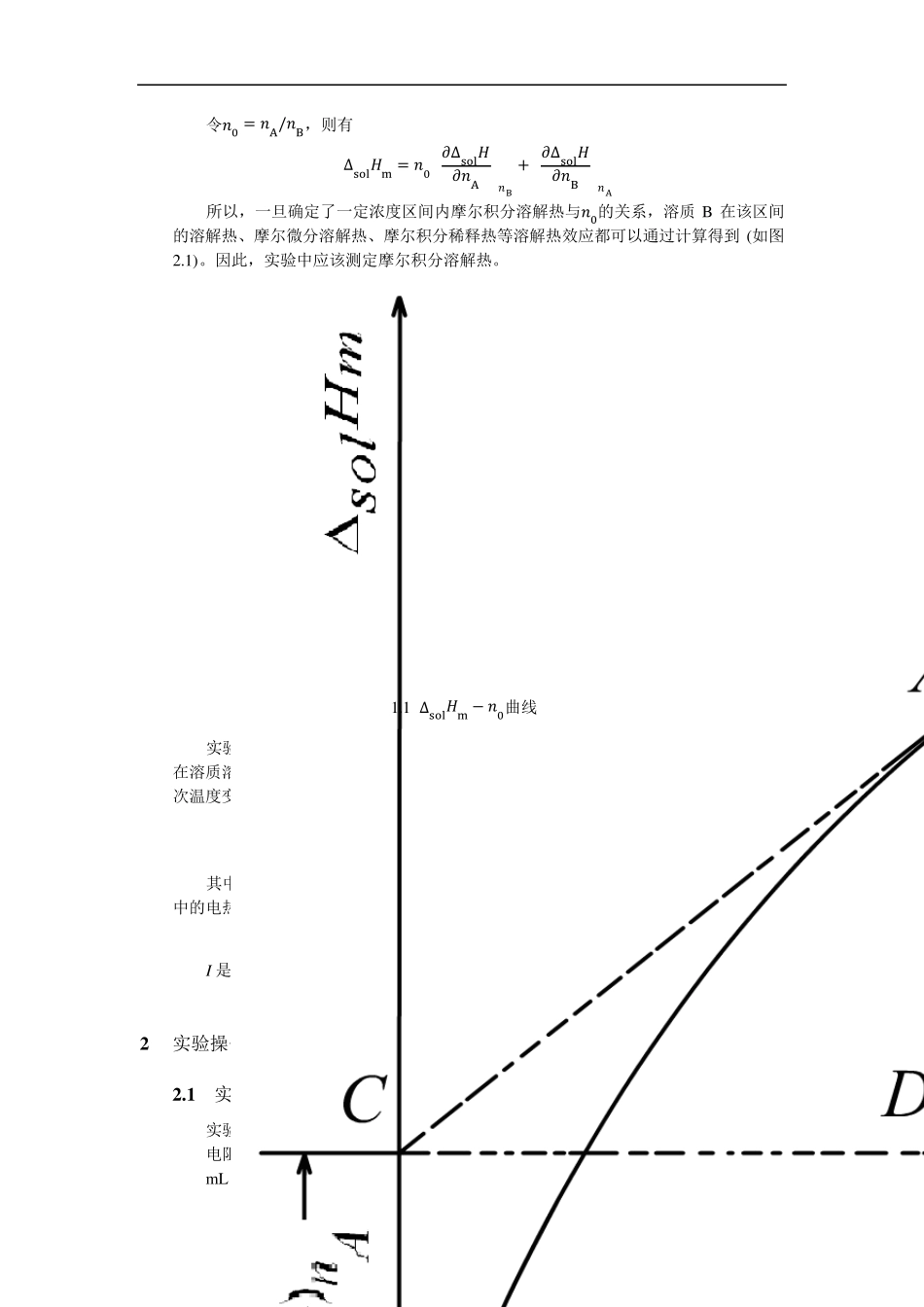
2 实验原理 在热化学中,关于溶解过程的热效应,有以下几个基本概念 溶解热 在恒温恒压下,溶质 B 溶于溶剂 A(或溶于某浓度溶液)中产生的热效应,用Δsolᵃ表示 摩尔积分溶解热 在恒温恒压下,1 mol 溶质溶解于一定量的溶剂中形成一定浓度的溶液,整个过程的热效应,用Δsolᵃᵅ表示: Δsolᵃᵅ = Δᵆᵅᵅᵃᵅᵃ 式中:ᵅᵃ是溶解于溶剂 A 中的溶质 B 的物质的量 摩尔微分溶解热 在恒温恒压下,1 mol 溶质溶于某一确定浓度的无限量的溶液中产生的热效应,以 (∂Δsol ᵃ∂ᵅB)ᵄ,ᵅ,ᵅA表示,简写为(∂Δsolᵃ∂ᵅB)ᵅA 稀释热 在恒温恒压下,一定量的溶剂 A 加到某浓度的溶液中使之稀释,所产生的热效应 摩尔积分稀释热 在恒温恒压下,在含有 1 mol 溶质的溶液中加入一定量的溶剂,使之稀释成另一浓度的溶液,这个过程产生的热效应,以Δdilᵃm表示: Δdilᵃm = Δsolᵃm2 − Δsolᵃm1 摩尔微分稀释热 在恒温恒压下,1 mol 溶剂加入到某一浓度无限量的溶液中所发生的热效应 在恒温恒压下,对于指定的溶剂 A 和溶质 B,溶解热的大小取决于 A 和 B 的物质的量,即 Δsolᵃ = ᵅ(ᵅA, ᵅB) 取全微分 Δsolᵃ = ᵅA (ᵱΔsolᵃᵱᵅA)ᵅB+ ᵅᵃ (ᵱΔsolᵃᵱᵅB)ᵅA 令ᵅ0 = ᵅA/ᵅB,则有 Δsolᵃm = ᵅ0 (ᵱΔsolᵃᵱᵅA)ᵅB+ (ᵱΔsolᵃᵱᵅB)ᵅA 所以,一旦确定了一定浓度区间内摩尔积分溶解热与ᵅ0的关系,溶质B 在该区间的溶解热、摩尔微分溶解热、摩尔积