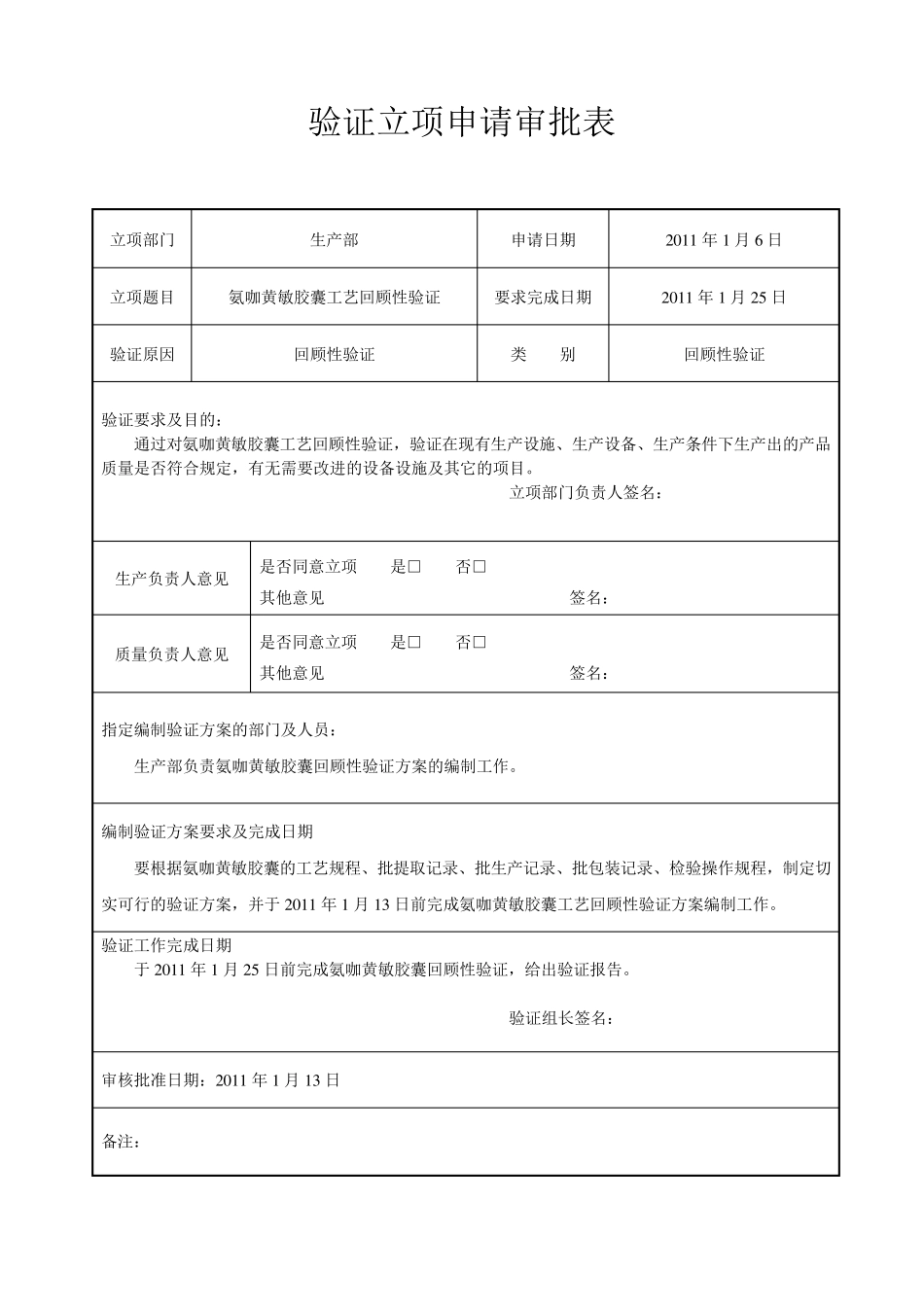
GMP 验 证 文 件 生 产工艺回顾性验 证 氨 咖 黄 敏 胶 囊 验证立项申请审批表 立项部门 生产部 申请日期 2 0 1 1 年1 月6 日 立项题目 氨咖黄敏胶囊工艺回顾性验证 要求完成日期 2 0 1 1 年1 月2 5 日 验证原因 回顾性验证 类 别 回顾性验证 验证要求及目的: 通过对氨咖黄敏胶囊工艺回顾性验证,验证在现有生产设施、生产设备、生产条件下生产出的产品质量是否符合规定,有无需要改进的设备设施及其它的项目
立项部门负责人签名: 生产负责人意见 是否同意立项 是□ 否□ 其他意见 签名: 质量负责人意见 是否同意立项 是□ 否□ 其他意见 签名: 指定编制验证方案的部门及人员: 生产部负责氨咖黄敏胶囊回顾性验证方案的编制工作
编制验证方案要求及完成日期 要根据氨咖黄敏胶囊的工艺规程、批提取记录、批生产记录、批包装记录、检验操作规程,制定切实可行的验证方案,并于 2 0 1 1 年1 月1 3 日前完成氨咖黄敏胶囊工艺回顾性验证方案编制工作
验证工作完成日期 于 2 0 1 1 年1 月2 5 日前完成氨咖黄敏胶囊回顾性验证,给出验证报告
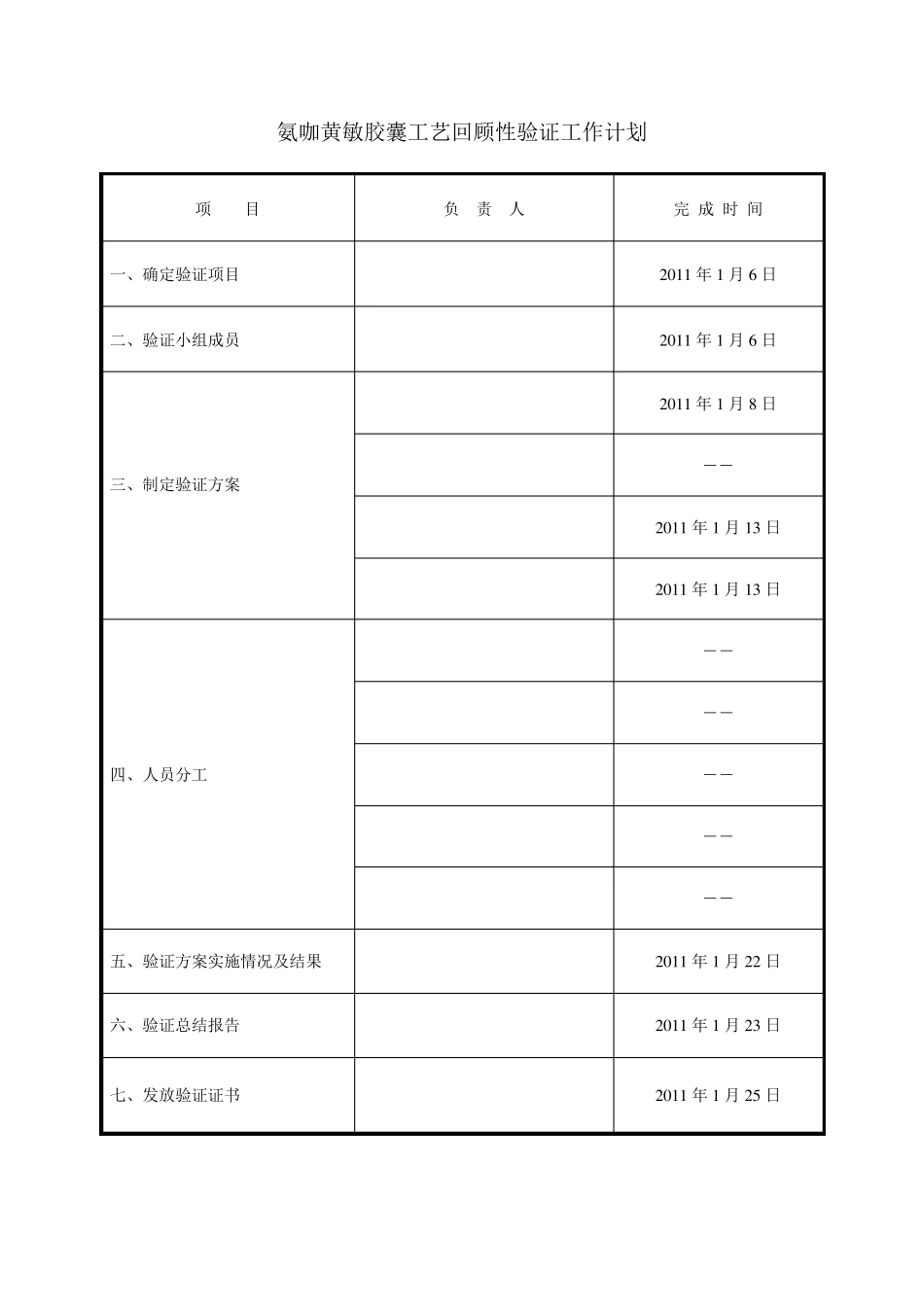
验证组长签名: 审核批准日期:2 0 1 1 年1 月1 3 日 备注: 氨咖黄敏胶囊工艺回顾性验证工作计划 项 目 负 责 人 完 成 时 间 一、确定验证项目 2 0 1 1 年1 月6 日 二、验证小组成员 2 0 1 1 年1 月6 日 三、制定验证方案 2 0 1 1 年1 月8 日 ―― 2 0 1 1 年1 月1 3 日 2 0 1 1 年1 月1 3 日 四、人员分工 ―― ―― ―― ―― ―― 五、验证方案实施情况及结果 2 0 1 1 年1 月2 2 日 六、验证总结报告 2 0 1 1 年1 月2 3 日 七、发放验证证书 2 0 1 1 年1 月2 5 日 目 录 一、回顾性验证