1 抚州市2012—2013学年度上学期期末考试 高二化学试题 命题教师:张政华(抚州一中) 李承平(临川一中) 注意:1
本卷全卷满分 100分,考试时间 100分钟 2
请同学们将答案直接填在答题卷上,收卷时只收答题卷 相对原子质量:H—1 C—12 O—16 Mg—24 Al—27 Cl—35
5 第Ⅰ卷(选择题,共 48分) 一、选择题:(共有 16个小题,每小题只有一个正确选项,每小题 3分,共 48分) 1.化学科学研究需要借助化学用语描述
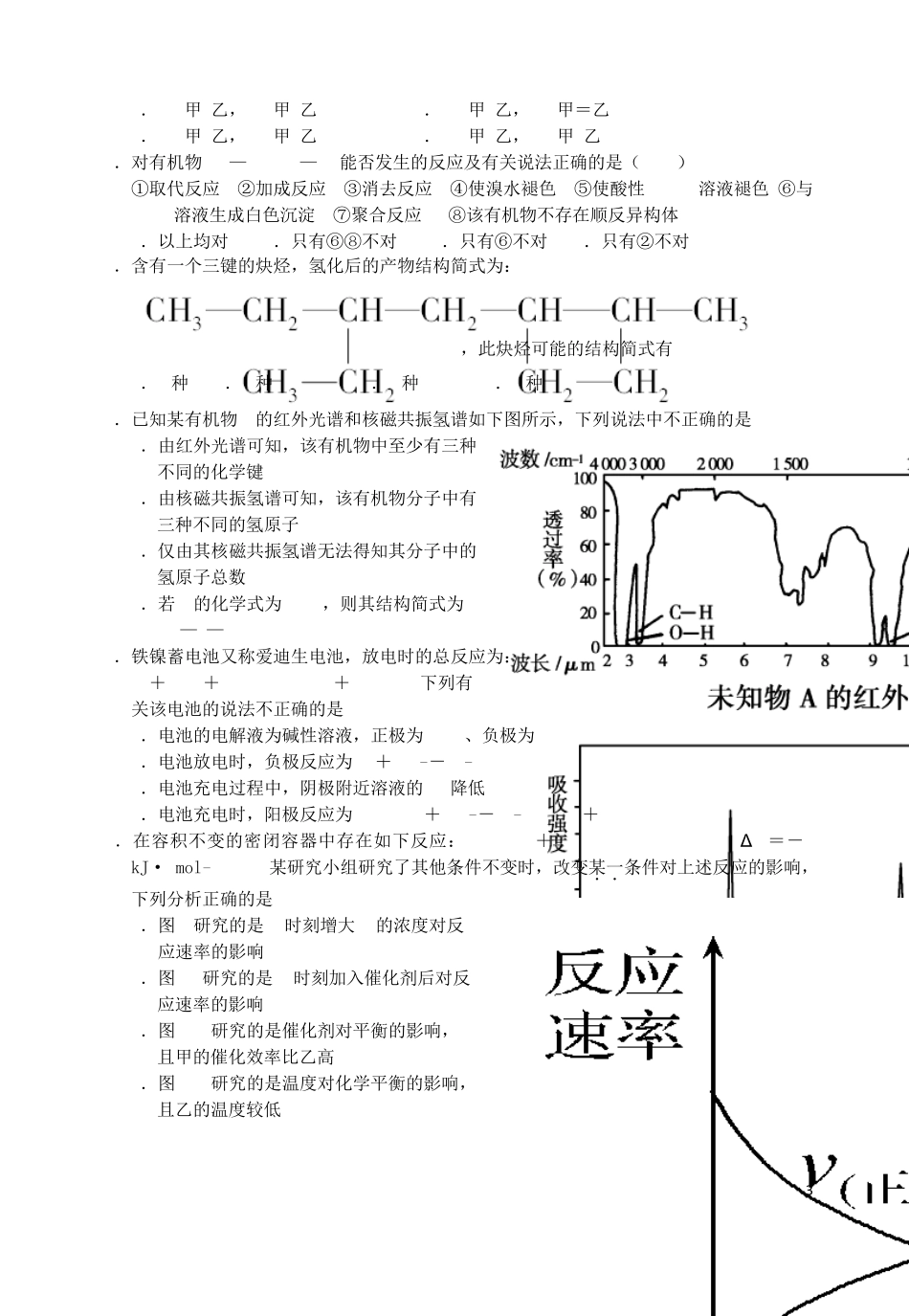
下列化学用语正确的是( ) A.乙烯的结构简式:CH2CH2 B.溴乙烷的电子式为: C.乙炔分子的球棍模型: D.HCO3-的水解方程式为:HCO3-+H2OCO32-+H3O+ 2.用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构简式如图,下 列说法正确的是 ( ) A.该烃可使溴水褪色 B.摩尔质量为 204 C.分子中所有原子可能共平面 D.完全燃烧生成 CO2 H2O SO3 3.下列事实中,不能用勒夏特列原理解释的是( ) A.配制 FeCl3溶液时为防止溶液浑浊常加入少量稀盐酸 B.H2、I2、HI平衡混合气体加压后颜色变深 C.实验室中常用排饱和食盐水的方法收集 Cl2 D.合成氨工业采用高压条件 4.工业上可利用合成气(CO和 H2的混合气体)生产甲醇
已知: CO(g)+2H2(g) CH3OH(g) Δ H=-92
9 kJ/mol 一定条件下,该反应在一体积固定的密闭容器中达到平衡
下列说法正确的是( ) A.该反应的△S<0 B.该反应在任何温度下均能自发进行 C.向容器中充入少量 He,平衡向正反应方向移动 D.升高温度平衡向正反应方向移动 5.下列实验装置及操作正确的是( ) A.构成原电池 B.检验溴乙烷消去后的产物是否含乙烯 2 C.测定H2O2的分解速率 D.研究钢铁的析