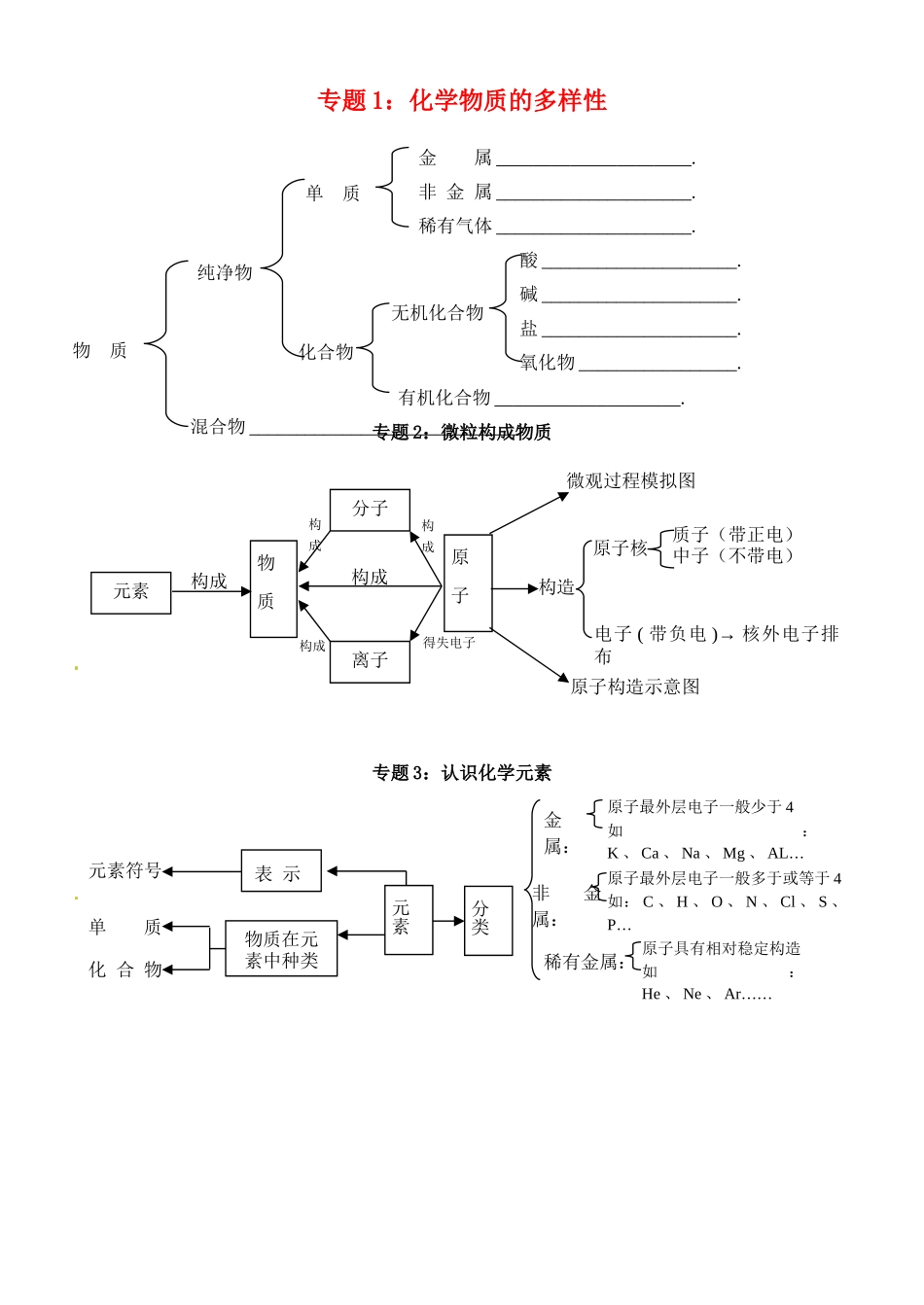
专题 1:化学物质的多样性专题 2:微粒构成物质专题 3:认识化学元素无机化合物有机化合物 ____________________
化合物单 质纯净物混合物 _____________________________
物 质金 属 _____________________
非 金 属 _____________________
稀有气体 _____________________
酸 _____________________
碱 _____________________
盐 _____________________
氧化物 _________________
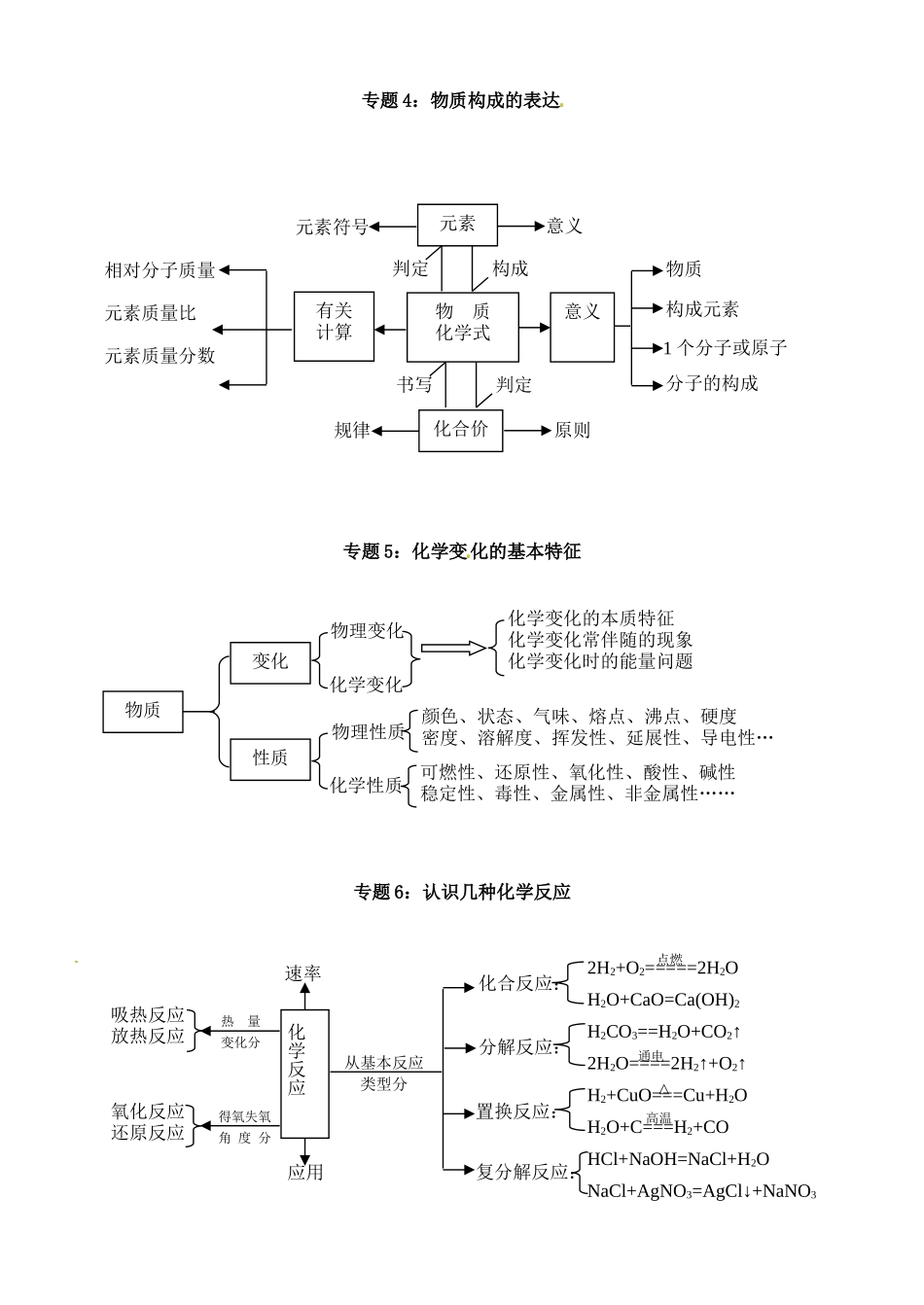
元素微观过程模拟图原子核质子(带正电)中子(不带电)电子 ( 带负电 )→ 核外电子排布原子构造示意图构造原 子分子离子物 质构成构成得失电子构成构成构成元素符号单 质 化 合 物表 示物质在元素中种类元素分类金属:非金属:稀有金属:原子最外层电子一般少于 4如:K 、 Ca 、 Na 、 Mg 、 AL…原子最外层电子一般多于或等于 4如: C 、 H 、 O 、 N 、 Cl 、 S 、P…原子具有相对稳定构造如:He 、 Ne 、 Ar……专题 4:物质构成的表达专题 5:化学变化的基本特征专题 6:认识几种化学反应相对分子质量元素质量比元素质量分数元素符号元素意义有关计算物 质化学式意义构成判定规律化合价原则判定书写物质构成元素1 个分子或原子分子的构成物质变化性质物理变化化学变化物理性质化学性质化学变化的本质特征化学变化常伴随的现象化学变化时的能量问题颜色、状态、气味、熔点、沸点、硬度密度、溶解度、挥发性、延展性、导电性…可燃性、还原性、氧化性、酸性、碱性稳定性、毒性、金属性、非金属性……吸热反应放热反应氧化反应还原反应热 量变化分得氧失氧角 度 分化学反应速率应用从基本反应类型分化合反应:分解反应