实验编号KClO3质量其它物质质量待测数据A1
2g无其它物质B1
2gCuO 0
5gba专题 4 化学反响条件的控制课题 2 催化剂对过氧化氢分解反响速率的影响【例 1】右图是讨论催化剂对过氧化氢分解反响速率影响的实验装置图
某学生讨论小组在50ml 量筒中盛满水,倒置于水槽中,通过分液漏斗把过氧化氢溶液参加锥形瓶中〔内中已有适量催化剂〕,记录各时间段收集到的氧气的体积
实验一:以二氧化锰作催化剂,进行以下四组实验
第 1 组:粉末状的二氧化锰 0
2g+ 5ml6% H2O2第 2 组:粉末状的二氧化锰 0
2g+ 3ml 10% H2O2第 3 组:粉末状的二氧化锰 0
1g+5ml6% H2O2第 4 组:颗粒状的二氧化锰 0
1g+5ml6% H2O2催化剂:MnO2第 1 组第 2 组第 3 组第 4 组前 15s 产生氧气的量〔ml〕111587前 30s 产生氧气的量〔ml〕2124119前 45s 产生氧气的量〔ml〕31351812前 60s 产生氧气的量〔ml〕45482615实验二:以不同的催化剂对过氧化氢〔均为 5ml6% H2O2〕分解反响速率影响进行讨论,记录反响的时间 t 和相应的量筒内的气体体积读数 V,用〔V2—V1〕/t 作为反响速率的表达式〔单位:ml·s-1〕,得到以下实验数据:催化剂产生气体速率/ ml·s-1催化剂产生气体速率/ ml·s-1MnO20
03CuO0
07活性炭0
12(1)写出 H2O2分解的反响方程式(2)实验一的几组数据能说明(3)实验二的几组数据反映出(4)用碰撞理论解释催化剂能增大化学反响速率的原因
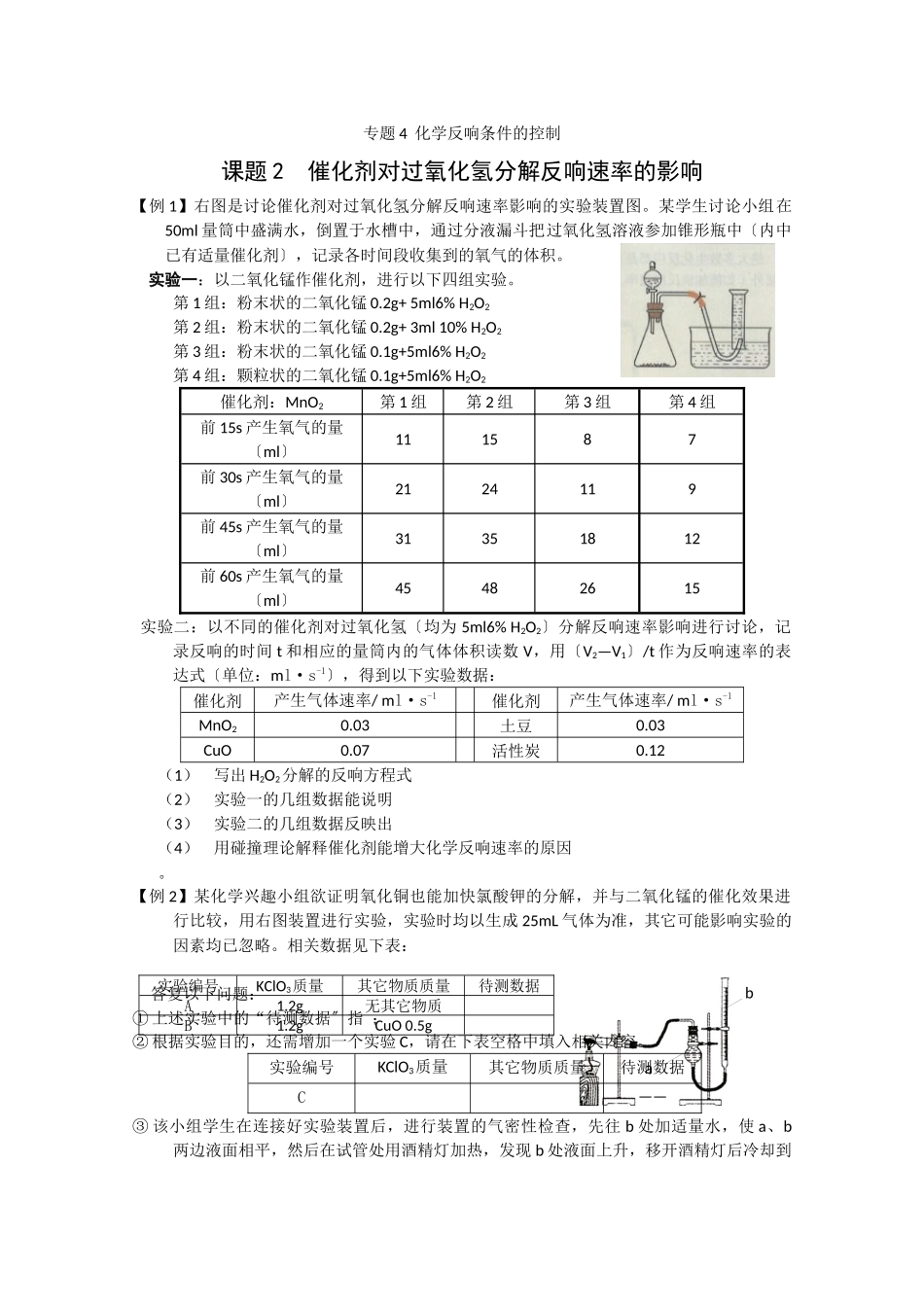
【例 2】某化学兴趣小组欲证明氧化铜也能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较,用右图装置进行实验,实验时均以生成 25mL 气体为准,其它可能影响实验的因素均已忽略
相关数据见下表