理想气体状态方程一、知识点击:1
理想气体:理想气体是一个理论模型,从分子动理论的观点来看,这个理论模型主要有如下三点:(1)分子本身的大小比起分子之间的平均距离来可以忽略不计
(2)气体分子在做无规则运动过程中,除发生碰撞的瞬间外,分子相互之间以及分子与容器器壁之间,都没有相互作用力
(3)分子之间以及分子与器壁之间的碰撞是完全弹性的,即气体分子的总动能不因碰撞而损失
由于不计分子之间的相互作用力,因而也就不计分子的势能,理想气体的内能就是所有分子的动能的总和
一定质量的理想气体内能的多少就只取决于温度,而与体积无关
在温度不太低,压强不太大的条件下,真实气体可看作为理想气体
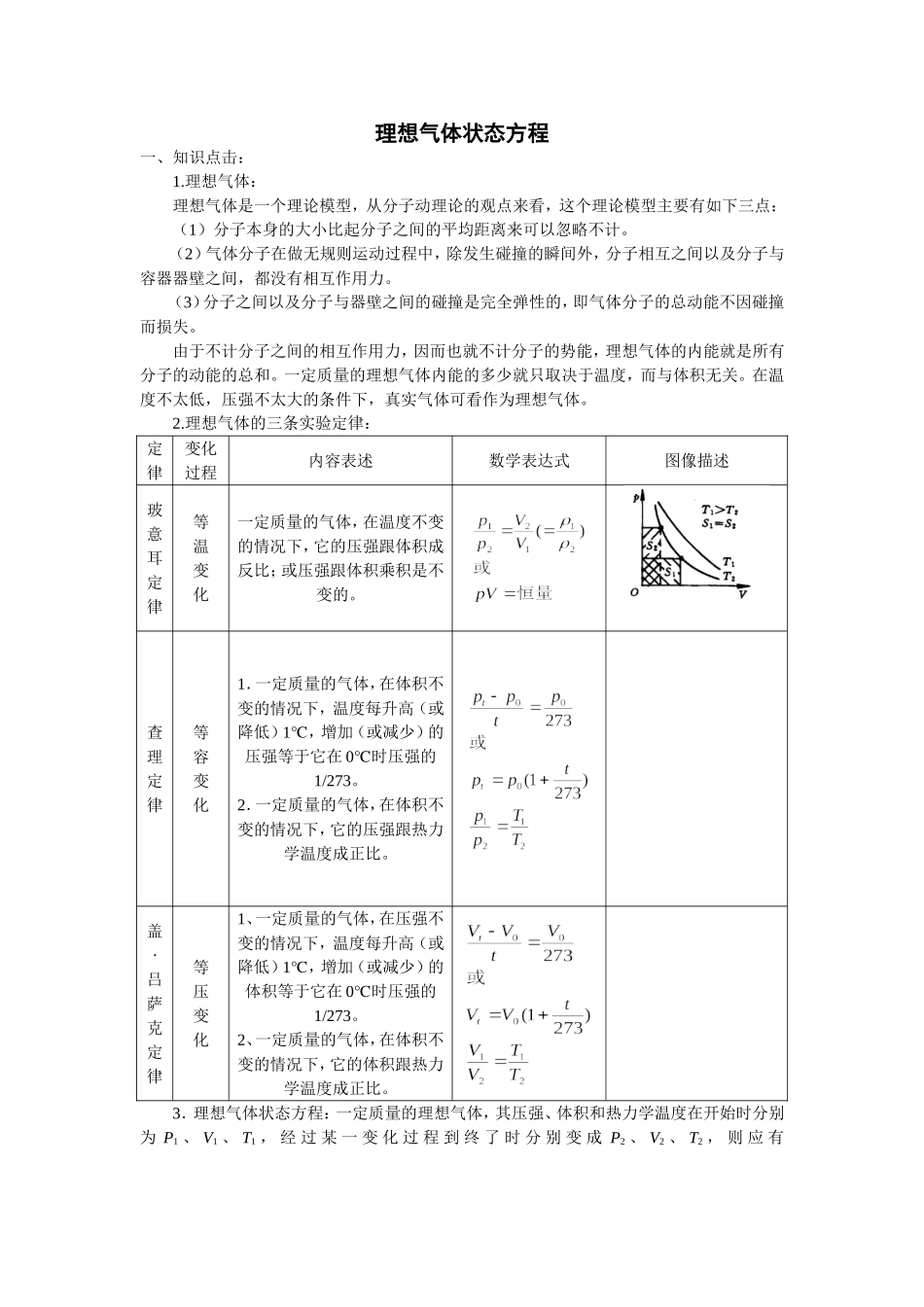
理想气体的三条实验定律:定律变化过程内容表述数学表达式图像描述玻意耳定律等温变化一定质量的气体,在温度不变的情况下,它的压强跟体积成反比;或压强跟体积乘积是不变的
查理定律等容变化1.一定质量的气体,在体积不变的情况下,温度每升高(或降低)1℃,增加(或减少)的压强等于它在0℃时压强的1/273
2.一定质量的气体,在体积不变的情况下,它的压强跟热力学温度成正比
盖·吕萨克定律等压变化1、一定质量的气体,在压强不变的情况下,温度每升高(或降低)1℃,增加(或减少)的体积等于它在0℃时压强的1/273
2、一定质量的气体,在体积不变的情况下,它的体积跟热力学温度成正比
3.理想气体状态方程:一定质量的理想气体,其压强、体积和热力学温度在开始时分别为P1、V1、T1,经过某一变化过程到终了时分别变成P2、V2、T2,则应有
这就是理想气体的状态方程
理想气体的状态方程是根据三条气体实验定律中的任意两条(例如玻意耳定律和查理定律)推导而得的
证明:如右图所示,ab为等容变化,根据查理定律有P1/T1=Pc/T2,bc为等温变化,根据波意耳定律有Pc·V1=P2·V2,两式联立起来,得到Pc=P1/