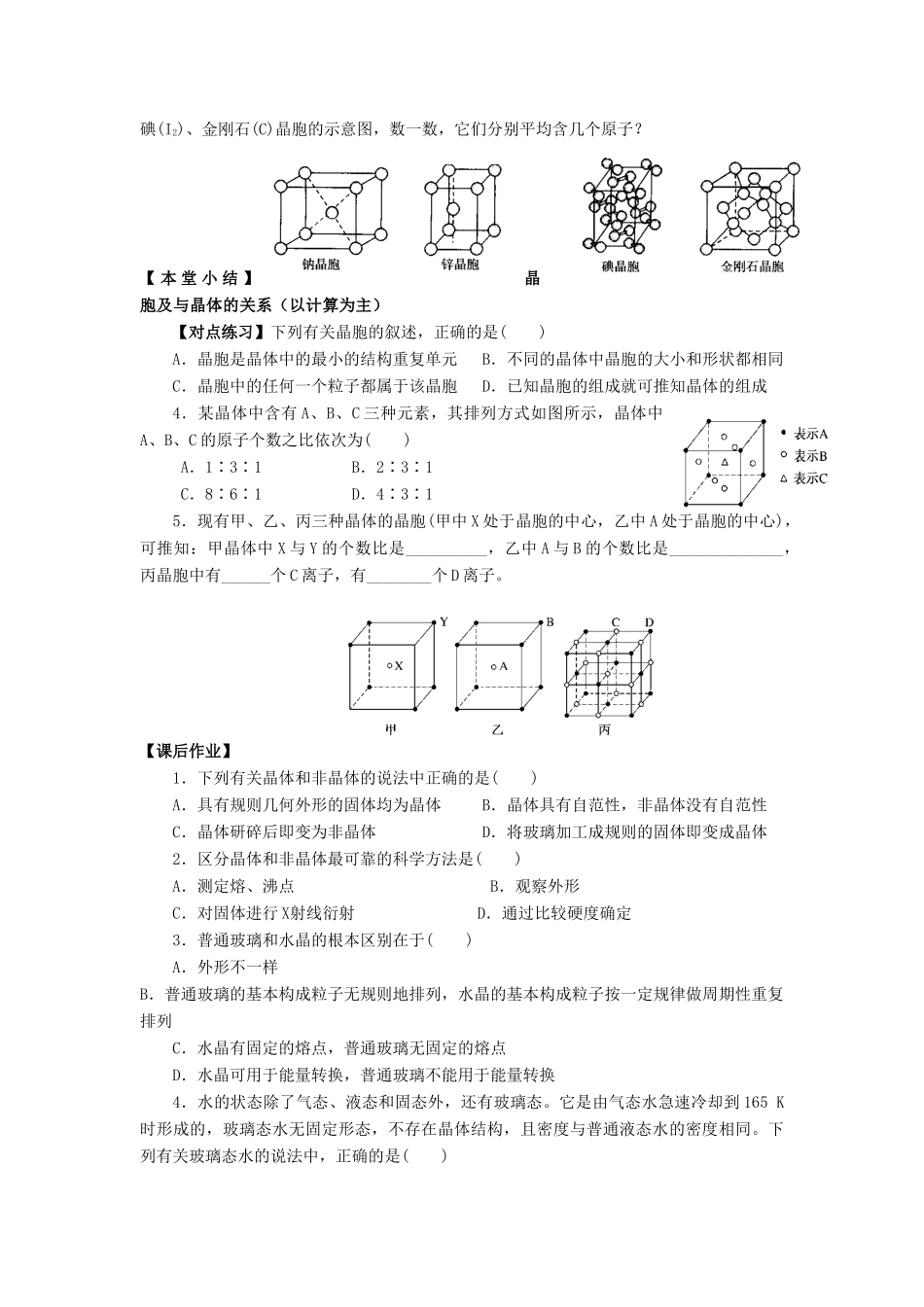
《选修三第三章第一节 晶体的常识》导学案(第 2 课时)学习时间 2011 — 2012 学年上学期 周【课标要求】 知识与技能要求:1
掌握晶胞的定义 2
掌握晶胞中原子个数的计算方法:【知识回顾与思考】 1
晶体有什么特征
如何来区别晶体和非晶体
【阅读】P63 -64 1
晶体结构的基本单元
图晶胞与晶体关系
一般说来,晶胞都是 ,整块晶体可看作是数量巨大的晶胞 而成;即指所有晶胞 都是 的, 相同
晶体化学式的确定主要采用均摊法,均摊法是指每个晶胞平均拥有的粒子数目,如某个粒子为 n 个晶胞所共用,则该粒子对一个晶胞的贡献为 1/n
⑴ 长方体形(或正方体形)晶胞中,不同位置的粒子对该晶胞的贡献(即晶胞对该粒子的均摊结果):① 处于顶点的粒子,同时为 个晶胞共有,每个粒子对该晶胞的贡献为
② 处于棱上的粒子,同时为 个晶胞共有,每个粒子对该晶胞的贡献为
③ 处于面上的粒子,同时为 个晶胞共有,每个粒子对该晶胞的贡献为
④ 处于体内的粒子,则完全属于该晶胞,每个粒子对该晶胞的贡献为
⑵ 非长方体晶胞粒子对晶胞的贡献视情况而定,如石墨晶胞(P71),每一层内碳原子排成正六边形,其顶点(一个碳原子)对六边形的贡献为
【典例解悟】如图所示的甲、乙、丙三种晶体试写出:(1)甲晶体的化学式(X 为阳离子)为
(2)乙晶体中 A、B、C 三种粒子的个数比是
(3)丙晶体中每个 D 周围结合 E 的个数是 个
【练习】现有甲、乙、丙、丁四种晶胞(如图 2-8 所示),可推知:甲晶体中 A 与 B的离子个数比为;乙晶体的化学式为______;丙晶体的化学式为______;丁晶体的化学式为______
2、钙-钛矿晶胞结构如图 2-9 所示
观察钙-钛矿晶胞结构,求该晶体中,钙、钛、氧的微粒个数比为多少
【学与问】教材 p64 下