第二节 富集在海水中的元素——氯(第 1 课时 氯气的制备和性质)【明确学习目标】1、了解氯元素的存在,初步掌握氯气的制备方法,能从氯原子结构特点理解氯气的主要化学性质(跟金属、非金属的反应)
(学习重点)2、了解氯气的主要物理性质;认识燃烧现象的本质
【预学能掌握的内容】一、活泼的黄绿色气体——氯气 1、氯元素的存在:氯元素在自然界中以 存在,主要以 形式存在于海水和陆地的盐矿中
2、氯气的实验室制法:阅读课本P82“科学史话”,舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一
实验室制取氯气是用软锰矿与浓盐酸混合加热,产生氯气,MnCl2和水
请写出舍勒发现氯气的化学反应方程式:(指出反应的氧化剂和还原剂;用双线桥表示电子转移的方向和数目
3、氯气的物理性质:颜色、状态气味水溶性毒性密度(比空气)4、氯气的化学性质:写出下列反应的化学方程式
(1)Cl2与金属的反应①与Na的反应: ;②与Fe的反应: ;③与Cu的反应:
(2)Cl2与非金属的反应① Cl2与H2的反应: ;② Cl2还能跟其他一些非金属单质反应,如与磷单质反应生成PCl5和PCl3:
【预学中的疑难问题】一、活泼的黄绿色气体——氯气〖交流展示〗小组交流课前预习收获与疑惑,讨论课本 P83 “思考与交流”并积极展示
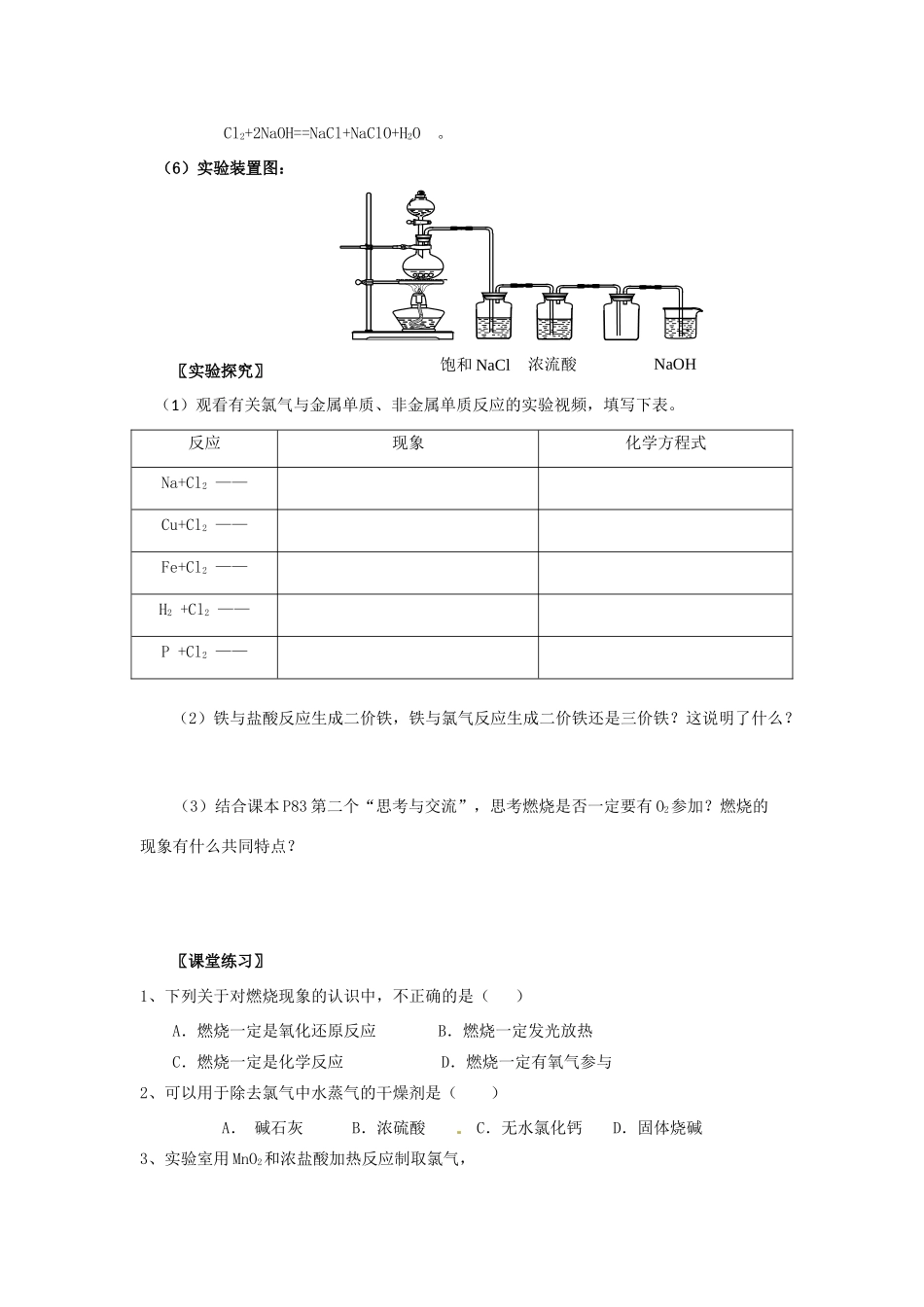
〖合作探究〗 观看氯气的实验室制法实验视频,合作交流完成知识梳理:氯气的实验室制法包括四个基本环节,即:制备(原料、原理、反应发生装置)、净化(除杂、干燥)、收集(收集方法、验满)、尾气处理
(1)原理:自然界中氯元素主要以 Cl-形态存在,因此制备氯气的基本原是就是用氧化剂将氯离子氧化成氯气单质 :2Cl-Cl2↑
① 实验室中通常用 MnO2作氧化剂和浓盐酸加热反应制取,请写出该反应的离子方程式:
②MnO2也可被 KMnO4、KClO3、NaClO 等强氧化剂