第 2 节 弱电解质的电离 盐类的水解第 1 课时 弱电解质的电离平衡[学习目标定位] 1
会描述弱电解质的电离平衡,能正确书写弱电解质的电离方程式,会分析电离平衡的移动
知道电离平衡常数的意义
1.将下列(Ⅰ)中的物质与(Ⅱ)、(Ⅲ)中的物质类型用短线连接起来
2.写出下列电解质的电离方程式:(1)Al2(SO4)3:Al2(SO4)3===2Al3++3SO;(2)NaOH:NaOH===Na++OH-;(3)H2SO4:H2SO4===2H++SO;(4)CH3COOH:CH3COOHCH3COO-+H+;(5)H2O:H2OH++OH-
3.(1)水的离子积常数表达式是 Kw= [H + ][OH - ]
(2)将纯水加热至较高温度,水的离子积变化是增大,pH 变化是减小
(3)室温下,某溶液中由水电离产生的[H+]=10-12 mol·L-1,则由水电离产生的[OH-]是 10 - 12_mol·L - 1 ,该溶液的 pH 可能是 2 或 12
探究点一 弱电解质的电离平衡1.弱电解质在水溶液中的电离都是可逆过程
醋酸是一种常见的弱电解质,它的电离方程式是 CH3COOHH++CH3COO-,在醋酸溶液中含有的溶质粒子有 H + 、 CH 3COO - 、 CH 3COOH
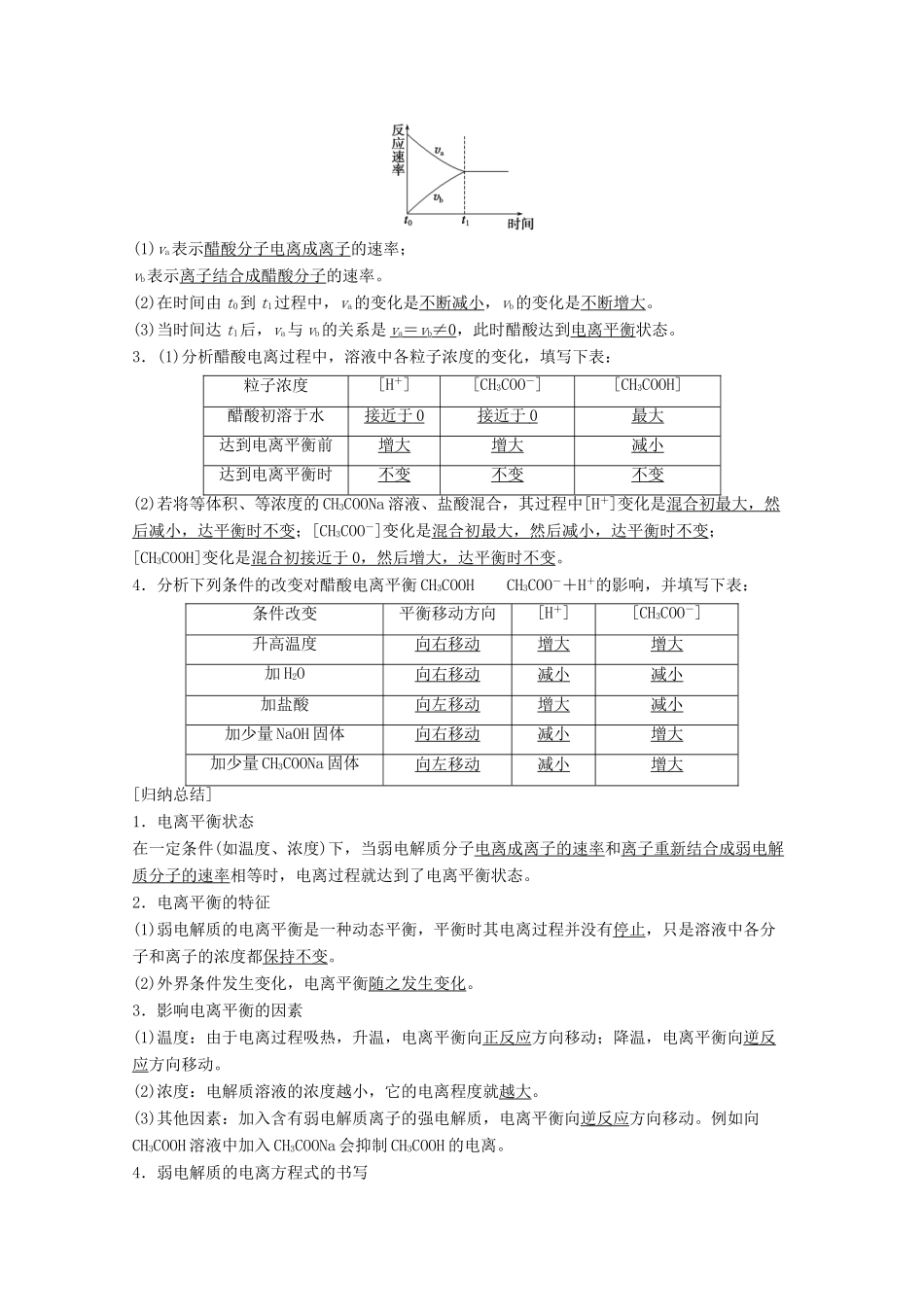
2.图是醋酸溶于水时,电离过程中,醋酸分子电离成离子的速率、离子重新结合成醋酸分子的速率随时间的变化曲线
请回答下列问题:(1)va表示醋酸分子电离成离子的速率;vb表示离子结合成醋酸分子的速率
(2)在时间由 t0到 t1过程中,va的变化是不断减小,vb的变化是不断增大
(3)当时间达 t1后,va与 vb的关系是 va= v b≠0,此时醋酸达到电离平衡状态
3.(1)分析醋酸电离过程中,溶液中各粒子浓度的变化,填写下表:粒子浓度[H+][CH3COO-][CH3C