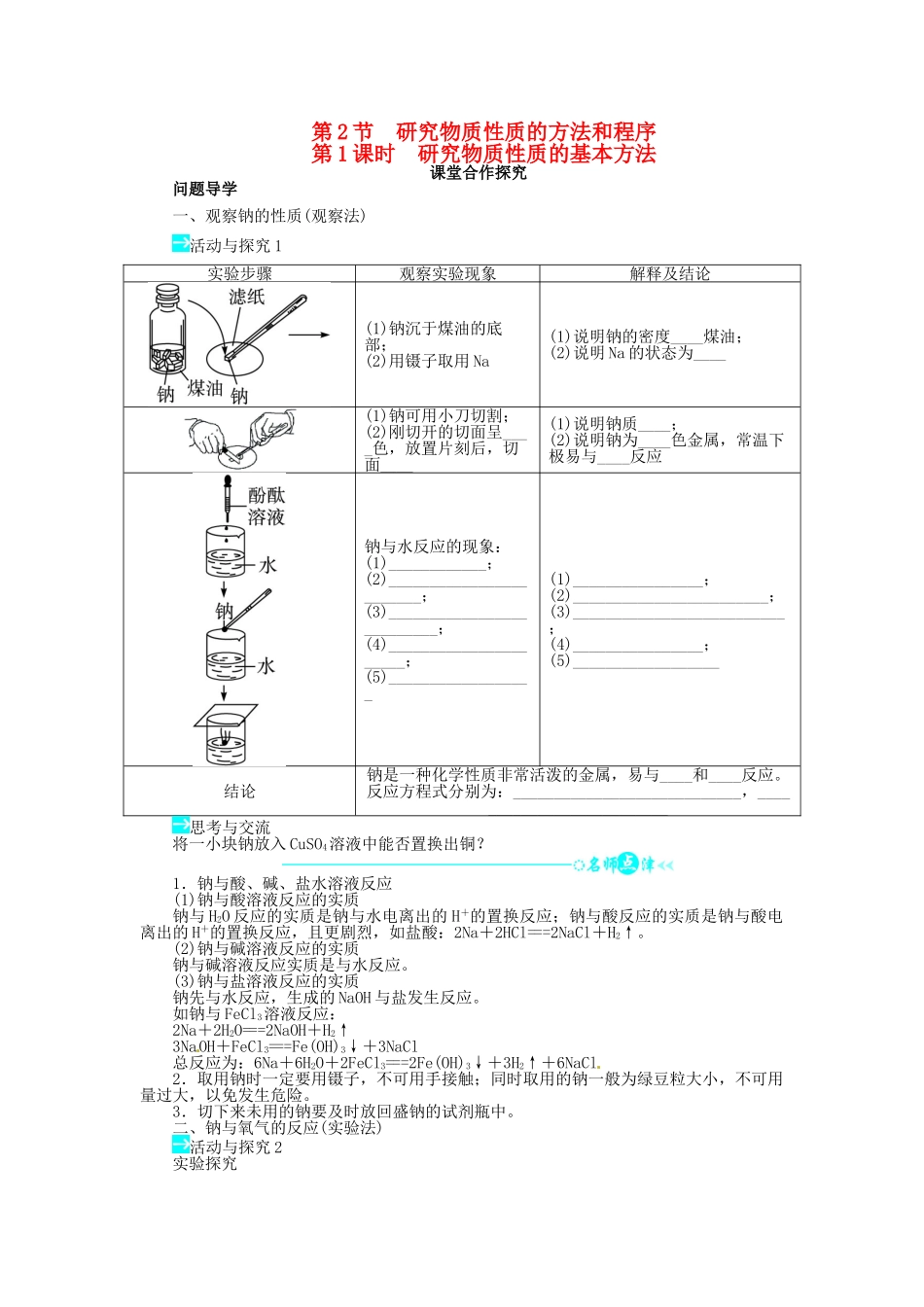
第 2 节 研究物质性质的方法和程序第 1 课时 研究物质性质的基本方法课堂合作探究问题导学一、观察钠的性质(观察法)活动与探究 1实验步骤观察实验现象解释及结论(1)钠沉于煤油的底部;(2)用镊子取用 Na(1)说明钠的密度____煤油;(2)说明 Na 的状态为____(1)钠可用小刀切割;(2)刚切开的切面呈____色,放置片刻后,切面____(1)说明钠质____;(2)说明钠为____色金属,常温下极易与____反应钠与水反应的现象:(1)____________;(2)________________________;(3)__________________________;(4)______________________;(5)__________________(1)________________;(2)________________________;(3)__________________________;(4)________________;(5)__________________结论钠是一种化学性质非常活泼的金属,易与____和____反应
反应方程式分别为:____________________________,__________________________思考与交流将一小块钠放入 CuSO4溶液中能否置换出铜
1.钠与酸、碱、盐水溶液反应(1)钠与酸溶液反应的实质钠与 H2O 反应的实质是钠与水电离出的 H+的置换反应;钠与酸反应的实质是钠与酸电离出的 H+的置换反应,且更剧烈,如盐酸:2Na+2HCl===2NaCl+H2↑
(2)钠与碱溶液反应的实质钠与碱溶液反应实质是与水反应
(3)钠与盐溶液反应的实质钠先与水反应,生成的 NaOH 与盐发生反应
如钠与 FeCl3溶液反应:2Na+2H2O===2NaOH+H2↑3Na