2008 年高考化学分类解析-化学与生活、环境和工业1.(08 海南卷)普钙是目前使用最广泛的磷肥,其主要成分是( )A.Ca5(PO4)3FB. Ca(H2PO4)2·H2O 和 CaSO4C.Ca3(PO4)2和 CaHPO4D.CaHPO4和 Ca(H2PO4)2答案:B2.与氨碱法比较,下列关于联合制碱法优点的判断中不正确的是( )A.提高了原料的原子利用率B.降低了生产成本C.减少了环境污染D.减轻了对设备的腐蚀答案:B3.(08 上海卷)食品检验是保证食品安全的重要措施,下列不属于食品安全检测指标的是( ) A.淀粉的含量B.二氧化硫的含量C.亚硝酸盐的含量D.甲醛的含量解析:选项 B、C、D 都是有毒物质,是食品安全检测的指标
答案:A 4.(08 上海卷)植物及其废弃物可以制取乙醇燃料,下列关于乙醇燃料的说法错误的是( )A.它是一种再生能源B.乙醇易燃烧,污染小C.乙醇只能在实验室内作燃料D.粮食作物是制乙醇的重要原料解析:乙醇不仅在实验室内可作燃料,而且还可作还可作内燃机等的燃料
答案:C 5.(08 广东卷)海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是( )A.海水中含有钾元素,只需经过物理变化就可以得到钾单质B.海水蒸发制海盐的过程中只发生了化学变化C.从海水中可以得到 NaCl,电解熔融 NaCl 可制备 Cl2D.利用潮汐发电是将化学能转化为电能解析:海水中钾元素以 K+形式存在,生成钾单质必然 发 生 化 学 反应,A 错
蒸发 制 海 盐 发 生的是物理变化,B 错
潮汐发电是将动能转化为电能,D 错
答案:C6.碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料
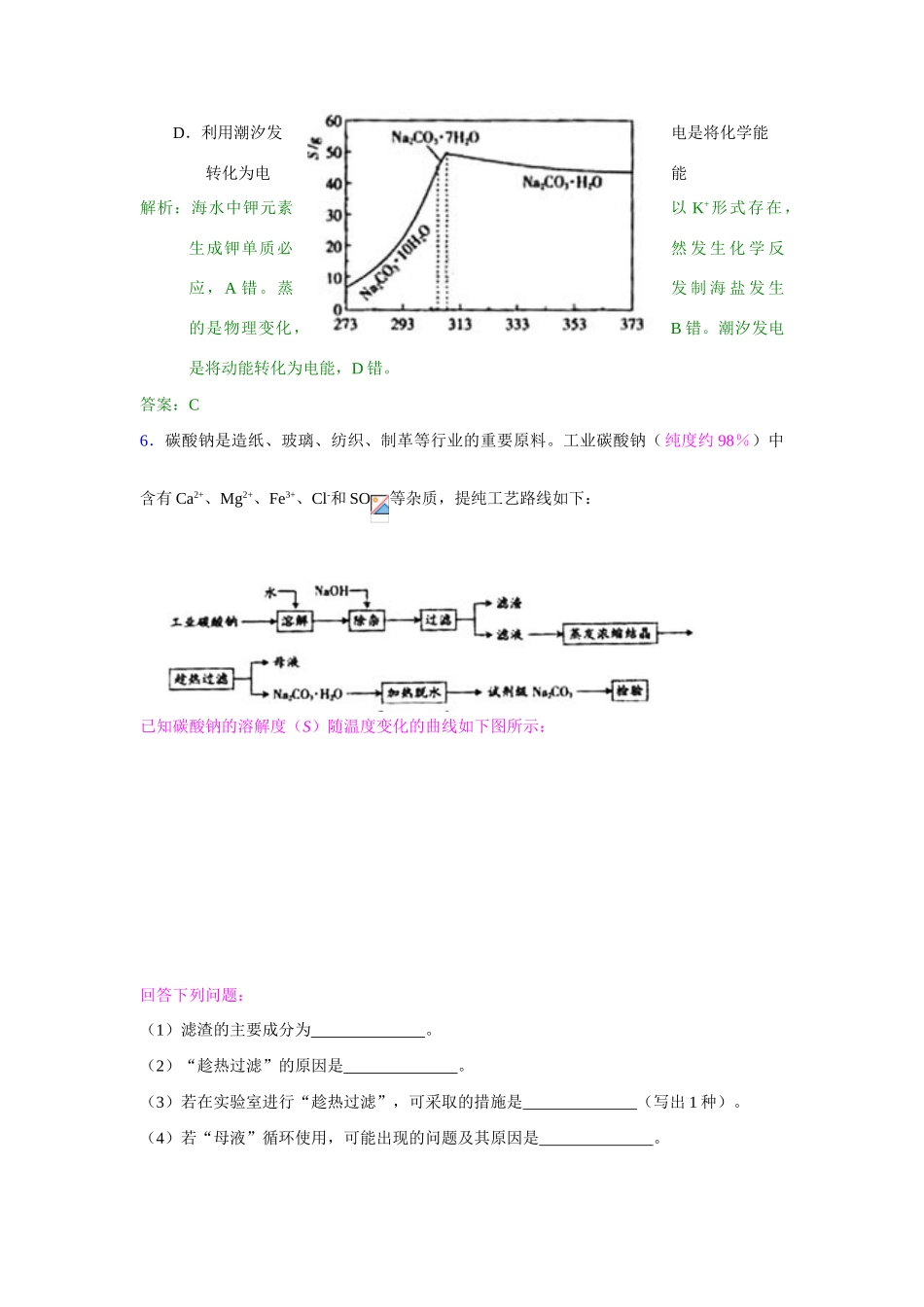
工业碳酸钠(纯度约 98%)中含有 Ca2+、Mg2+、Fe3+、Cl-和 SO等杂质,提纯工艺路线如下:已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:回答下列