山东省泰安市肥城市第三中学 2013-2014 学年高中化学 第 1 章 第 3 节《化学中常用的物理量 物质的量》(第 3 课时)学案 鲁科版必修 1学习内容学习指导即时感悟学习目标:1
知道物质的量及其单位摩尔的含义,明确 1 mol 的含义,并能进行物质的量与微观粒子数之间的换算
知道摩尔质量、气体摩尔体积及物质的量浓度的含义,能够进行物质的量与物质的质量、标准状况下气体的体积或溶液中溶质的含量之间的换算
【回顾﹒预习】物质的量的单位——摩尔(mol),摩尔质量(g/mol),气体摩尔体积(L/mol)、物质的量浓度(mol/L),阿伏加德罗常数,物质的量与微粒(原子
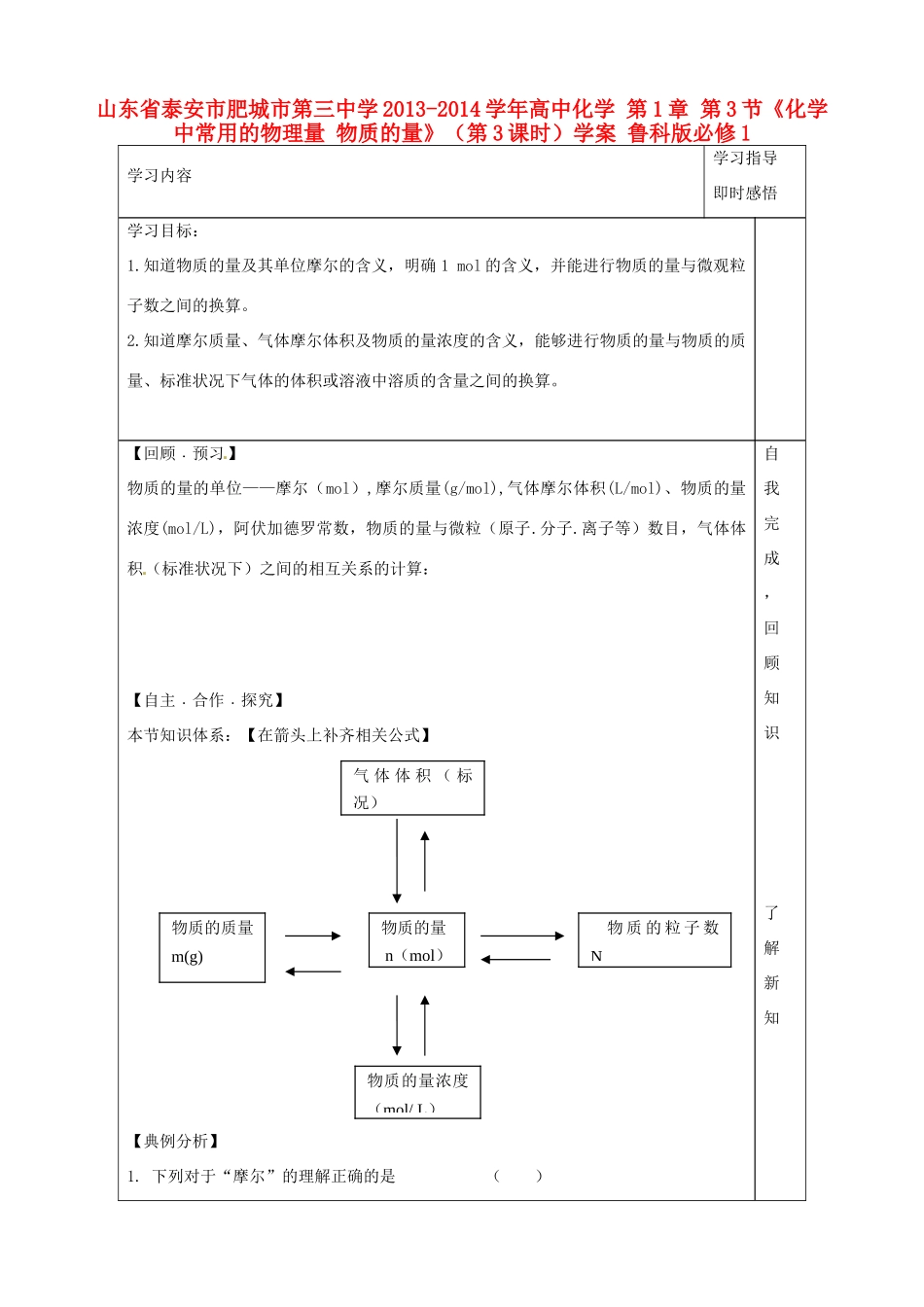
离子等)数目,气体体积(标准状况下)之间的相互关系的计算:【自主﹒合作﹒探究】本节知识体系:【在箭头上补齐相关公式】【典例分析】1
下列对于“摩尔”的理解正确的是( )自我完成,回顾知识 了解新知 气 体 体 积 ( 标况)物质的量 n(mol)物质的质量m(g)物质的量浓度(mol/ L)物 质 的 粒 子 数NA
摩尔是国际科学界建议采用的一种物理量B
摩尔是物质的量的单位,简称摩,符号为 molC
摩尔可以把物质的宏观数量与微观粒子的数量联系起来D
国际上规定,0
012kg 碳原子所含有的碳原子数目为 1 摩2
下列有关阿佛加德罗常数(NA)的说法错误的是 ( )A
32 克 O2 所含的原子数目为 NA B
5molH2O 含有的原子数目为 1
1molH2O 含有的 H2O 分子数目为 NAD
05 NA 个氯气分子的物质的量是 0
5mol【当堂达标】1
下列说法正确的是 ( )A
摩尔质量就等于物质的式量 B
摩尔质量是物质式量的 6
02×1023 倍 C
HNO3 的摩尔质量是 63g D
硫酸和磷酸的摩尔质量相等2