第二节 离子反应【学习目标】1.知道酸、碱、盐在溶液中发生电离,会书写强酸、强碱和可溶性盐的电离方程式
2.通过实验事实认识离子反应发生的条件,能正确书写有关离子方程式
3.了解 Cl—、SO42—、CO32—等常见离子的检验方法
【活动过程】活动一:认识酸、碱、盐在水溶液的电离
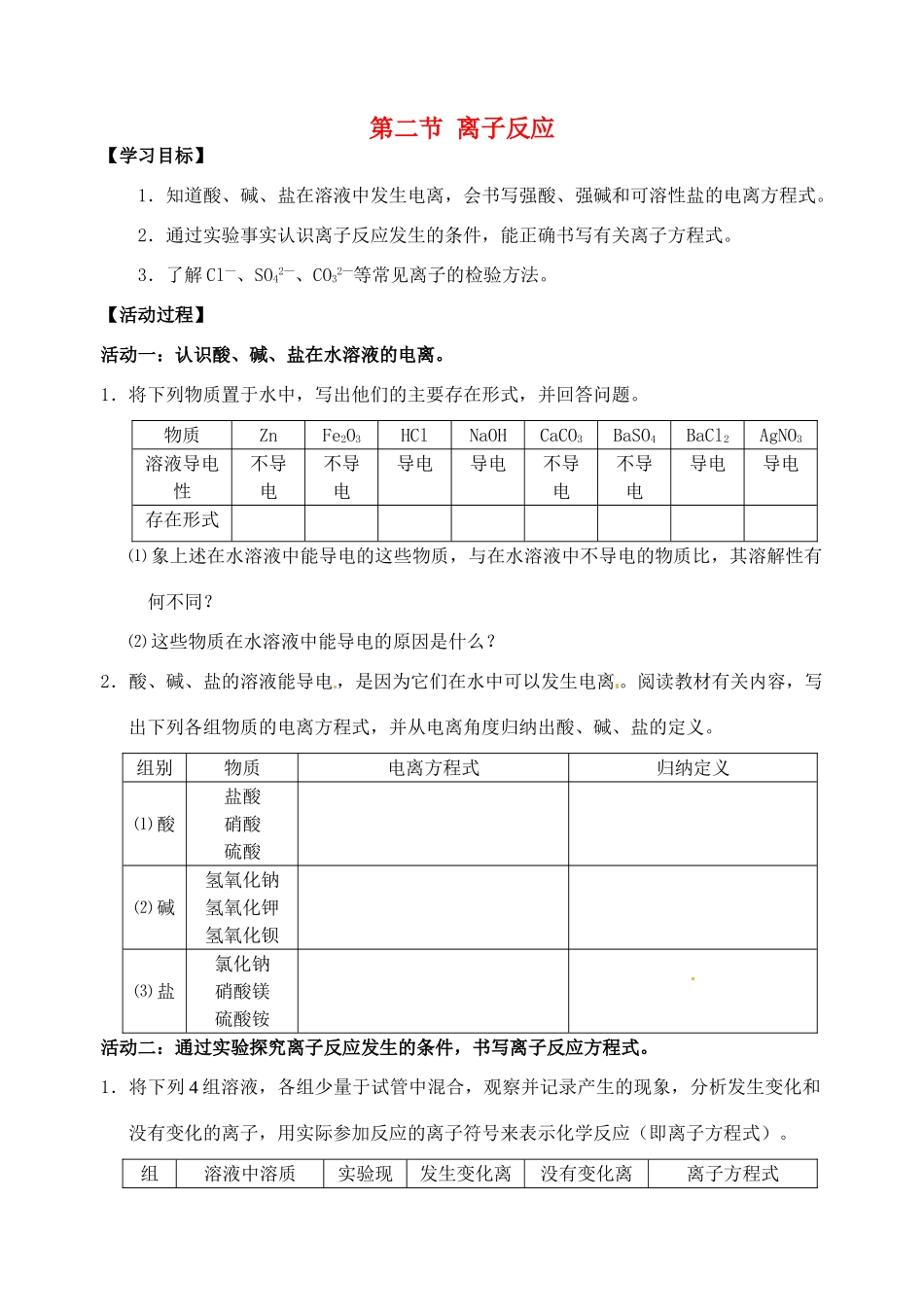
1.将下列物质置于水中,写出他们的主要存在形式,并回答问题
物质ZnFe2O3HClNaOHCaCO3BaSO4BaCl2AgNO3溶液导电性不导电不导电导电导电不导电不导电导电导电存在形式⑴ 象上述在水溶液中能导电的这些物质,与在水溶液中不导电的物质比,其溶解性有何不同
⑵ 这些物质在水溶液中能导电的原因是什么
2.酸、碱、盐的溶液能导电 ,是因为它们在水中可以发生电离
阅读教材有关内容,写出下列各组物质的电离方程式,并从电离角度归纳出酸、碱、盐的定义
组别物质电离方程式归纳定义⑴ 酸盐酸硝酸硫酸⑵ 碱氢氧化钠氢氧化钾氢氧化钡⑶ 盐氯化钠硝酸镁硫酸铵活动二:通过实验探究离子反应发生的条件,书写离子反应方程式
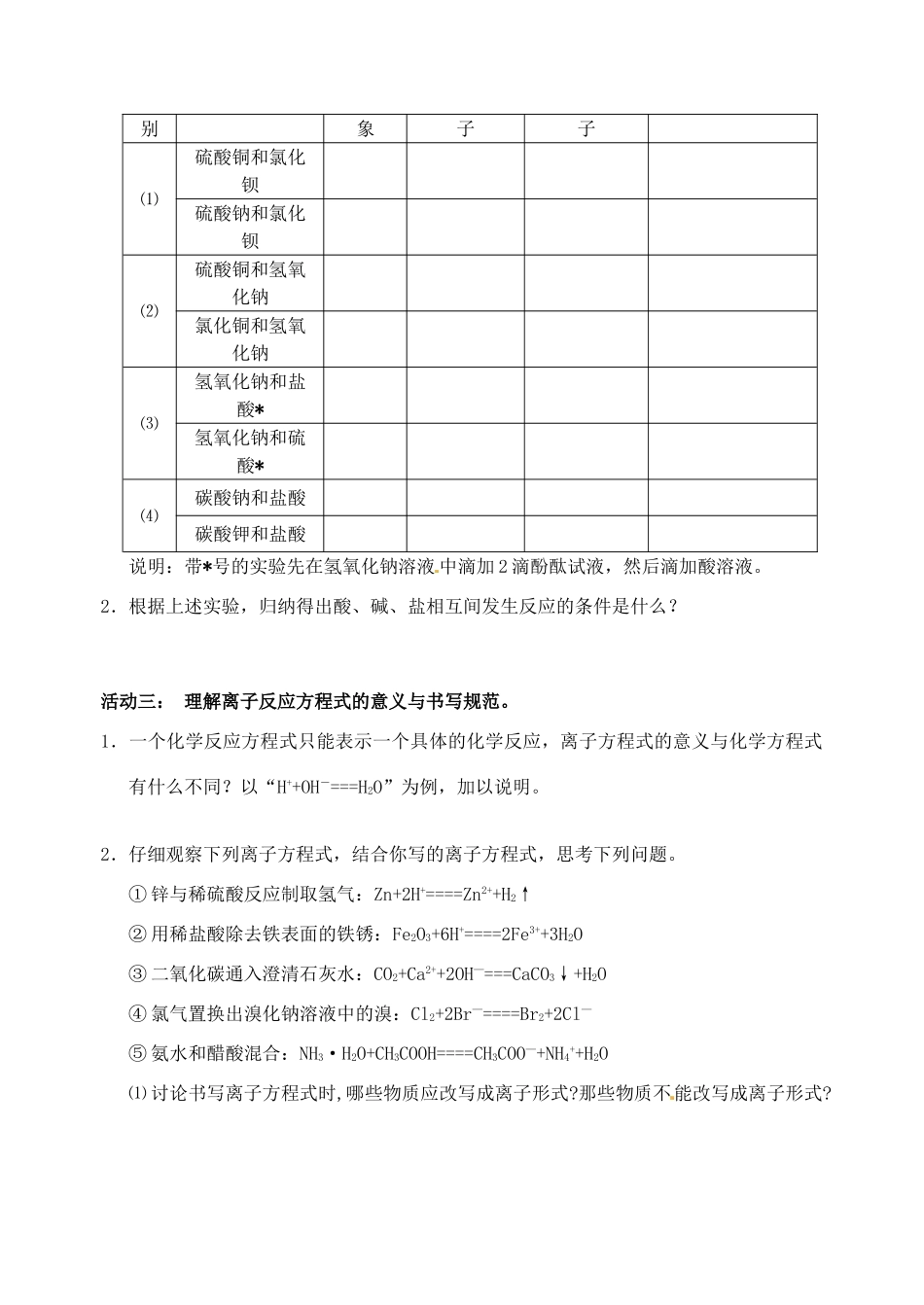
1.将下列 4 组溶液,各组少量于试管中混合,观察并记录产生的现象,分析发生变化和没有变化的离子,用实际参加反应的离子符号来表示化学反应(即离子方程式)
组溶液中溶质实验现发生变化离没有变化离离子方程式别象子子⑴硫酸铜和氯化钡硫酸钠和氯化钡⑵硫酸铜和氢氧化钠氯化铜和氢氧化钠⑶氢氧化钠和盐酸*氢氧化钠和硫酸*⑷碳酸钠和盐酸碳酸钾和盐酸说明:带*号的实验先在氢氧化钠溶液 中滴加 2 滴酚酞试液,然后滴加酸溶液
2.根据上述实验,归纳得出酸、碱、盐相互间发生反应的条件是什么
活动三: 理解离子反应方程式的意义与书写规范
1.一个化学反应方程式只能表示一个具体的化学反应,离子方程式的意义与化学方程式有什么不同
以“H++OH-===H2O”为例,加以说明
2.仔细观察下列离子方程式,结合你写的