第七单元 水溶液中的离子平衡能力提升强、弱电解质的比较强酸与一元弱酸的性质差异(以盐酸和醋酸为例)归纳如下:(1)盐酸中 HCl 全部电离,不存在 HCl 分子,只有 H+、Cl-、OH-(极少);醋酸在水溶液中部分电离,存在电离平衡,既含 H+、CH3COO-、OH-(极少),还有醋酸分子
(2)pH 相同的盐酸和醋酸,醋酸的物质的量浓度大于盐酸
(3)同温度、同浓度的盐酸的导电性强于醋酸溶液
(4)中和同体积、同 pH 的盐酸和醋酸,醋酸的耗碱量多于盐酸
(5)pH 相同、体积也相同的盐酸和醋酸,分别与足量活泼金属反应时,起始速率相同;在反应过程中,醋酸反应速率减小程度比盐酸慢,平均反应速率比盐酸快,产生的氢气也是醋酸多
(6)同浓度、同体积的盐酸和醋酸,分别与足量较活泼的金属反应,盐酸产生氢气的速率比醋酸大,但产生氢气的物质的量相等
(7)pH 相同、体积也相同的盐酸和醋酸,分别与等物质的量的强碱氢氧化钠发生中和反应后,若盐酸反应后溶液呈中性,则醋酸反应后溶液呈酸性
(8)同浓度、同体积的盐酸和醋酸,分别与等物质的量的强碱氢氧化钠发生中和反应后,盐酸反应后溶液呈中性,则醋酸反应后溶液呈碱性
(9)pH 相同、体积也相同的盐酸和醋酸,加水稀释相同倍数时,盐酸的 pH 增加程度大,醋酸的 pH 增加程度小
(10)盐酸和醋酸的溶液中分别加入相应的钠盐固体后,盐酸的 pH 几乎不变,而醋酸溶液的 pH 增大
(11)当盐酸与弱碱相互滴定达到滴定终点时,溶液显酸性,应选择酸性变色指示剂(甲基橙);当醋酸与强碱相互滴定时,溶液显碱性,应选择碱性变色指示剂(酚酞)
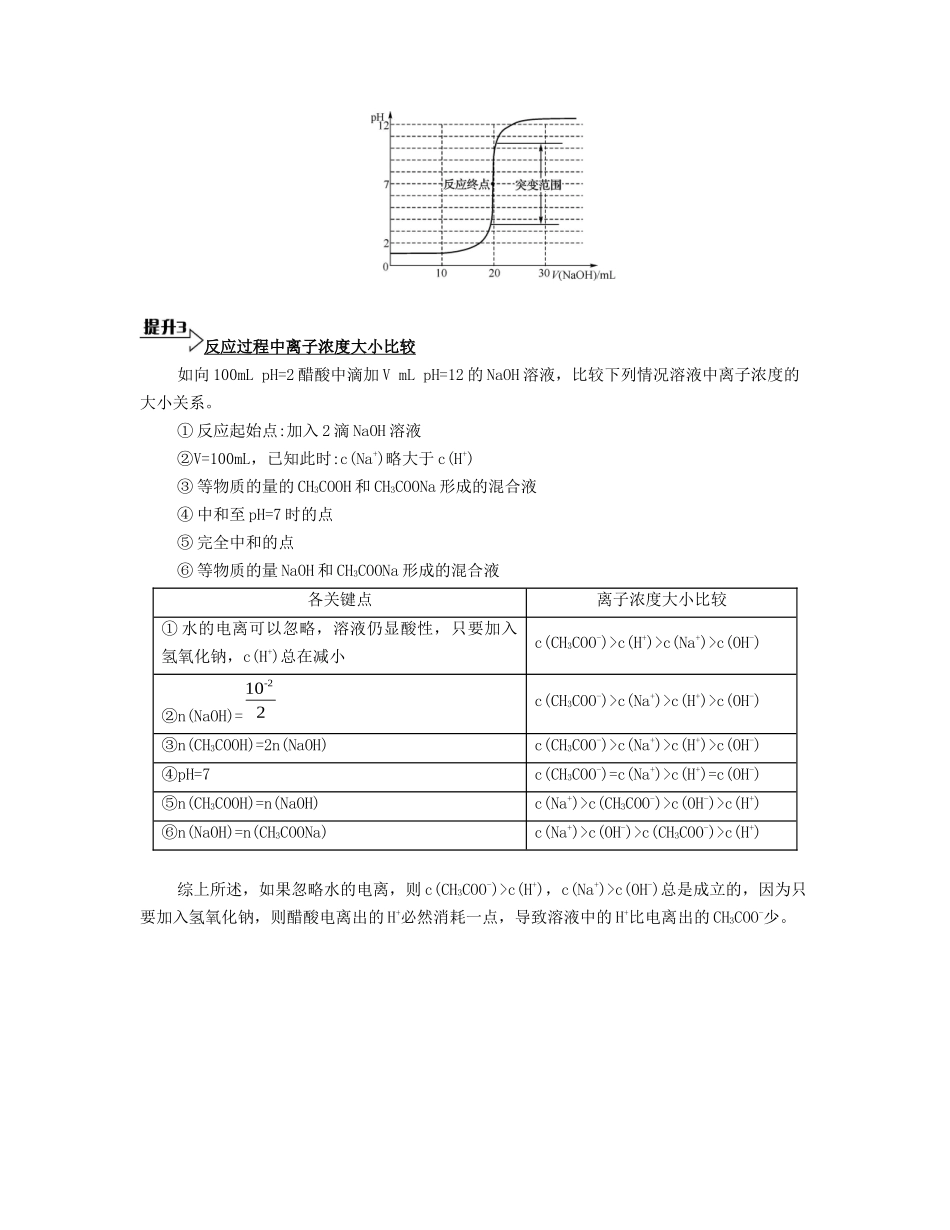
酸碱中和滴定 pH 变化曲线 以 0
100 0 mol·L-1NaOH 滴定 0
100 0 mol·L-1HCl 为例,pH 变化曲线如下图所示
理论上讲,强酸强碱完全反应时的 pH 应为 7,滴定时应选用在 pH