第三单元 氯、溴、碘及其重要化合物学习任务 1 氯及其重要化合物的性质与应用一、氯气的性质1.氯气的物理性质颜色状态气味密度毒性溶解性特性黄绿色气体有刺激性气味比空气大有毒能溶于水,1 体积水约溶解 2体积 Cl2易液化2
从氯原子的原子结构认识氯气的化学性质——氧化性依据氯气的氧化性完成下列方程式:(1)与金属反应①Fe:2Fe + 3Cl 2===== 2FeCl 3,棕红色烟
②Cu:Cu + Cl 2===== CuCl 2,棕黄色烟
(2)与非金属反应H2:H2+ Cl 2===== 2HCl ,苍白色火焰;H2和 Cl2的混合气体光照时会发生爆炸
(3)与还原性无机化合物反应① 与碘化钾溶液反应:Cl2+ 2I - == =2Cl - + I 2(填离子方程式)
② 与 SO2水溶液反应:Cl2+ SO 2+ 2H 2O == =H 2SO4+ 2HCl 、 Cl 2+ SO 2+ 2H 2O == =4H + + SO + 2Cl -(填化学方程式和离子方程式)
③ 与 FeCl2溶液反应:Cl2+ 2Fe 2 + == =2Fe 3 + + 2Cl - (填离子方程式)
3.从化合价的角度认识氯气的化学性质——歧化反应氯气与水或碱反应,氯元素的化合价既有升高又有降低,因而氯气既表现氧化性又表现还原性
(1)与水反应化学方程式:Cl2+ H 2O HCl + HClO ;离子方程式:Cl2+ H 2O H + + Cl - + HClO
(2)与碱反应① 与烧碱反应:Cl2+ 2NaOH == =NaCl + NaClO + H 2O(填化学方程式);② 制取漂白粉:2Cl2+ 2Ca(OH) 2== =CaCl 2+ Ca(ClO) 2+ 2H 2O(填化学方程式)
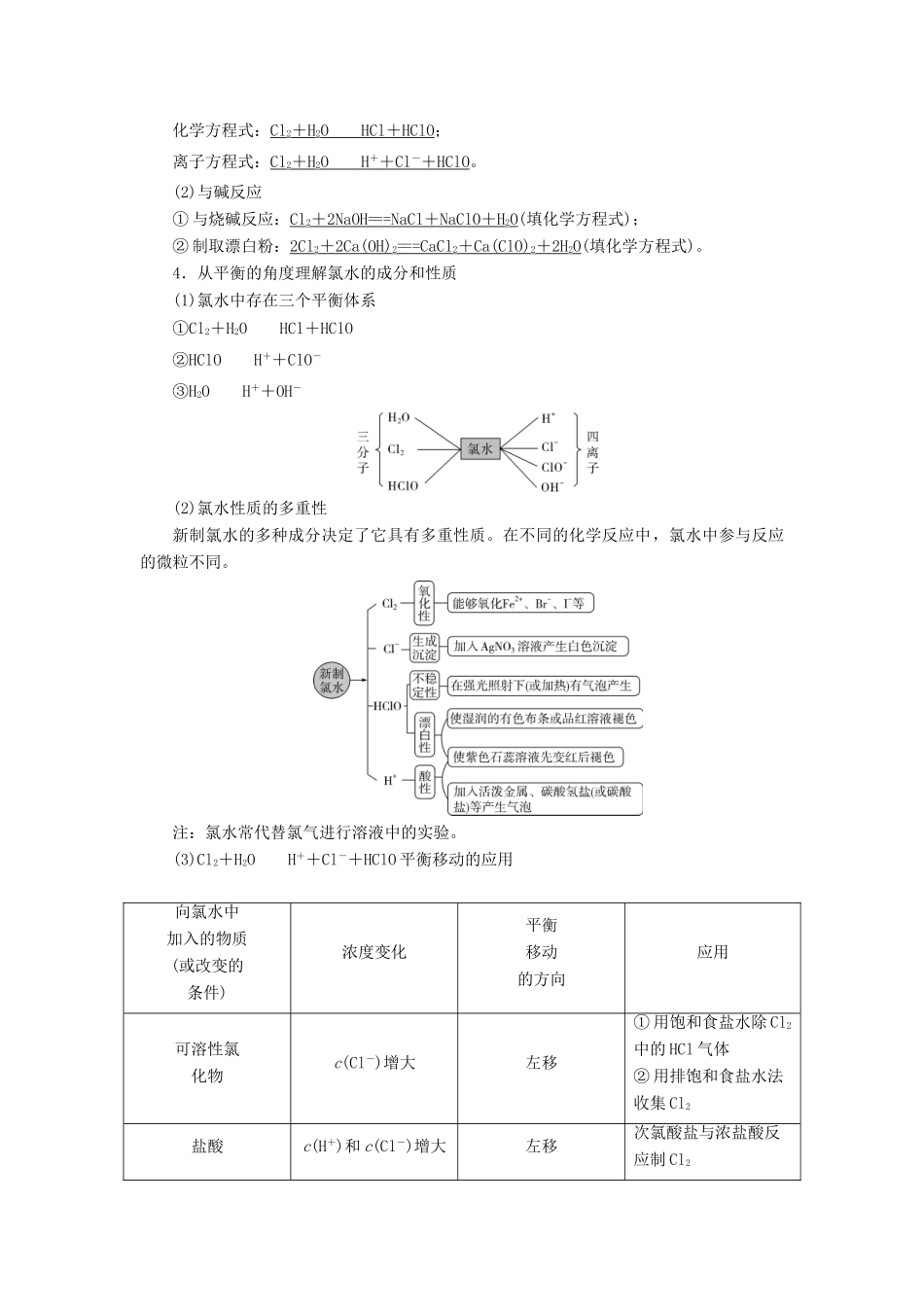
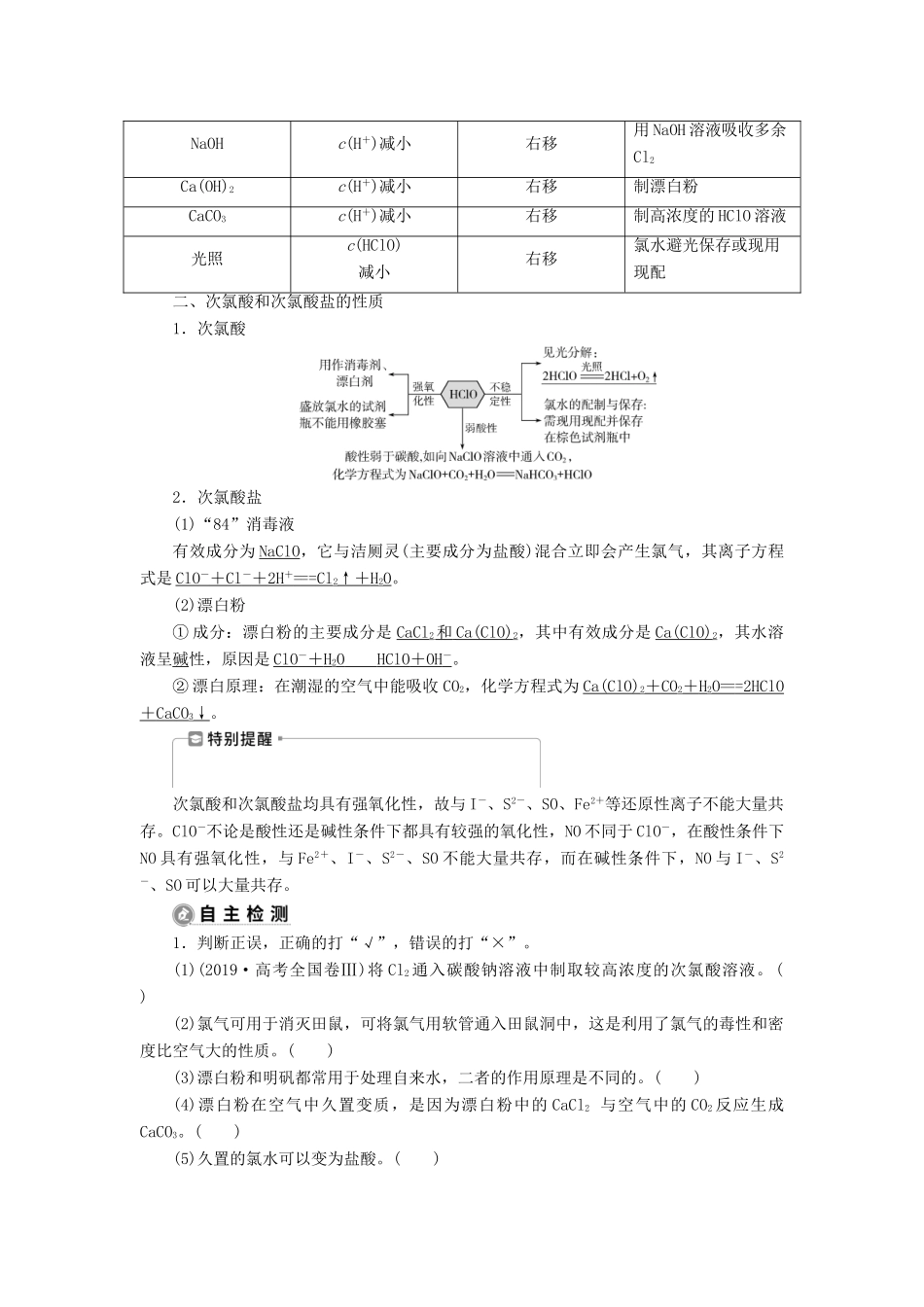
4.从平衡的角度理解氯水的成分和性质(1)氯水中存在三个平衡体系①Cl2+H2