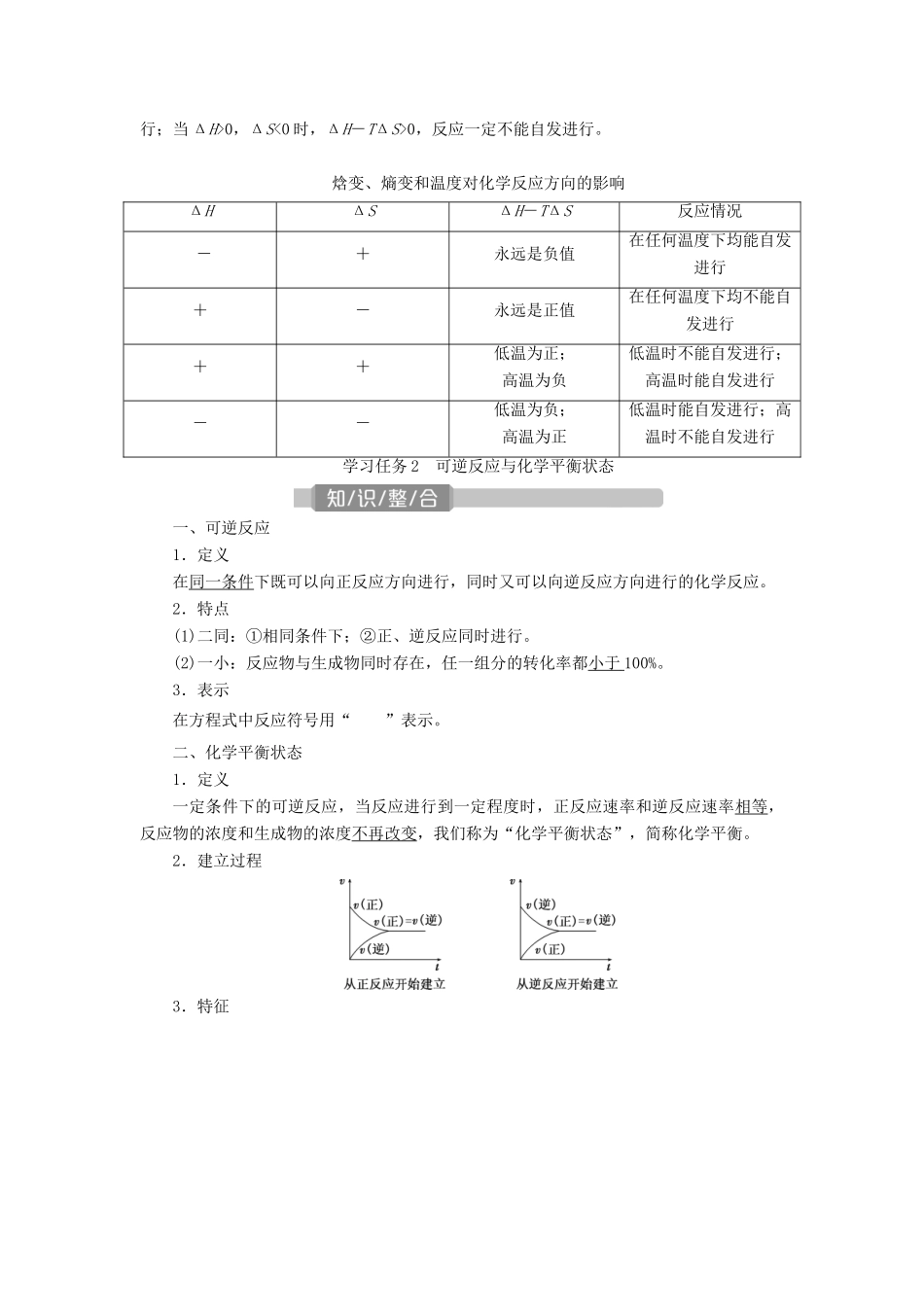
第二单元 化学反应的方向与限度学习任务 1 化学反应的方向1.自发过程(1)含义在一定条件下,不需要借助外力作用就能自动进行的过程
(2)特点① 体系趋向于从高能状态转变为低能状态(体系对外部做功或放出热量);② 在密闭条件下,体系有从有序转变为无序的倾向性(无序体系更加稳定)
2.化学反应方向的判据 1.判断正误,正确的打“√”,错误的打“×”
(1)(2019·高考江苏卷)一定温度下,反应 2H2 (g)+O2(g)===2H2O(g)能自发进行,该反应的 ΔH0B.纯碳和氧气反应生成 CO(g),ΔS>0C.H2O(g)变成液态水,ΔS>0D.CaCO3(s)加热分解为 CaO(s)和 CO2(g),ΔS>0解析:选 C
C 项,H2O(g)变成液态水,熵值减小,故 ΔS0B.反应 NH3(g)+HCl(g)===NH4Cl(s)在室温下可自发进行,则该反应的 ΔH0,ΔS>0D.常温下,反应 C(s)+CO2(g)===2CO(g)不能自发进行,则该反应的 ΔH>0解析:选 A
A 项,该反应是熵减的反应,常温下能自发进行说明 ΔH0;D 项,该反应 ΔS>0,常温下不能自发进行,则有 ΔH-TΔS>0,故ΔH>0
3.(2020·保定高三检测)下列反应中