第 3 节 化学能转化为电能——电池第 1 课时 原电池的工作原理、化学电源[课标要求]1.了解原电池的工作原理及其构成条件,了解常见的化学电源及其工作原理
2.掌握电极反应和电池反应方程式的书写
3.依据原电池的原理判断金属的活泼性强弱及设计原电池
1.原电池负极上发生氧化反应,正极上发生还原反应
2.原电池负极流出电子,正极流入电子
电解质溶液中阴离子移向负极,阳离子移向正极
3.原电池的构成条件:①两个活动性不同的电极;②有电解质溶液;③形成闭合回路
4.正极材料活泼性<负极材料活泼性,正极通常具备特定的现象:有气体生成、电极质量增加或不变等;负极通常不断溶解,质量减小
5.利用原电池原理可以加快某些氧化还原反应的速率
6.化学电源分为一次电池、可充电电池(二次电池)和燃料电池
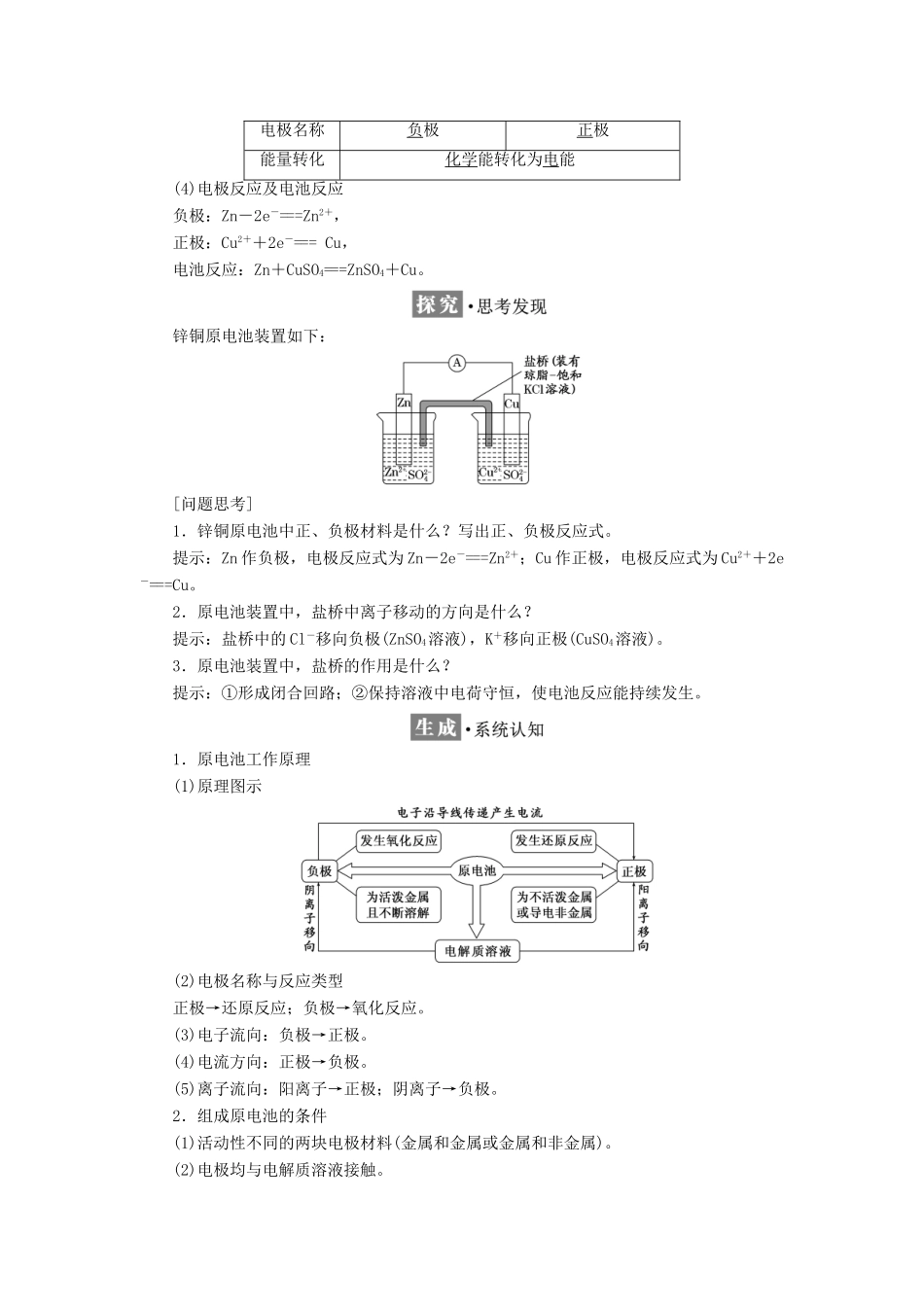
设计实验将锌与 CuSO4溶液的反应所释放的能量转化为电能,填写实验记录
(1)实验装置(2)实验现象电流计指针电极表面变化情况Ⅰ发生偏转锌片质量减少,铜片质量增加Ⅱ发生偏转锌片质量减少,铜片质量增加(3)实验分析Zn 极Cu 极电子流向由 Zn 极流向 Cu 极电子得失Zn 失电子溶液中 Cu2+得电子电极名称负极正极能量转化化学能转化为电能(4)电极反应及电池反应负极:Zn-2e-===Zn2+,正极:Cu2++2e-=== Cu,电池反应:Zn+CuSO4===ZnSO4+Cu
锌铜原电池装置如下:[问题思考]1.锌铜原电池中正、负极材料是什么
写出正、负极反应式
提示:Zn 作负极,电极反应式为 Zn-2e-===Zn2+;Cu 作正极,电极反应式为 Cu2++2e-===Cu
2.原电池装置中,盐桥中离子移动的方向是什么
提示:盐桥中的 Cl-移向负极(ZnSO4溶液),K+移向正极(CuSO4溶液)
3.原电池装置中,盐桥的作用是什么
提示:①形成闭合回路;②保持溶液中电荷守恒,使