关于发布《药品生产质量管理法律规范(2025 年修订)》无菌药品等 5 个附录的公告2025 年 02 月 24 日 发布国家食品药品监督管理局公 告 2025 年 第 16 号关于发布《药品生产质量管理法律规范(2025 年修订)》无菌药品等 5 个附录的公告有关管理事宜的公告 根据卫生部令第 79 号《药品生产质量管理法律规范(2025 年修订)》第三百一十条规定,现发布无菌药品、原料药、生物制品、血液制品及中药制剂等 5 个附录,作为《药品生产质量管理法律规范(2025 年修订)》配套文件,自 2025 年 3 月 1 日起施行
附件:1 .无菌药品 2 .原料药 3 .生物制品 4 .血液制品 5.中药制剂国家食品药品监督管理局二○一一年二月二十四日附录1:无菌药品第一章范围第一条 无菌药品是指法定药品标准中列有无菌检查项目的制剂和原料药,包括无菌制剂和无菌原料药
第二条 本附录适用于无菌制剂生产全过程以及无菌原料药的灭菌和无菌生产过程
第二章原则第三条无菌药品的生产须满足其质量和预定用途的要求,应当最大限度降低微生物、各种微粒和热原的污染
生产人员的技能、所接受的培训及其工作态度是达到上述目标的关键因素,无菌药品的生产必须严格根据精心设计并经验证的方法及规程进行,产品的无菌或其它质量特性绝不能只依赖于任何形式的最终处理或成品检验(包括无菌检查)
第四条 无菌药品按生产工艺可分为两类:采纳最终灭菌工艺的为最终灭菌产品;部分或全部工序采纳无菌生产工艺的为非最终灭菌产品
第五条 无菌药品生产的人员、设备和物料应通过气锁间进入干净区,采纳机械连续传输物料的,应当用正压气流保护并监测压差
第六条物料准备、产品配制和灌装或分装等操作必须在干净区内分区域(室)进行
第七条 应当根据产品特性、工艺和设备等因素,确定无菌药品生产用干净区的级别
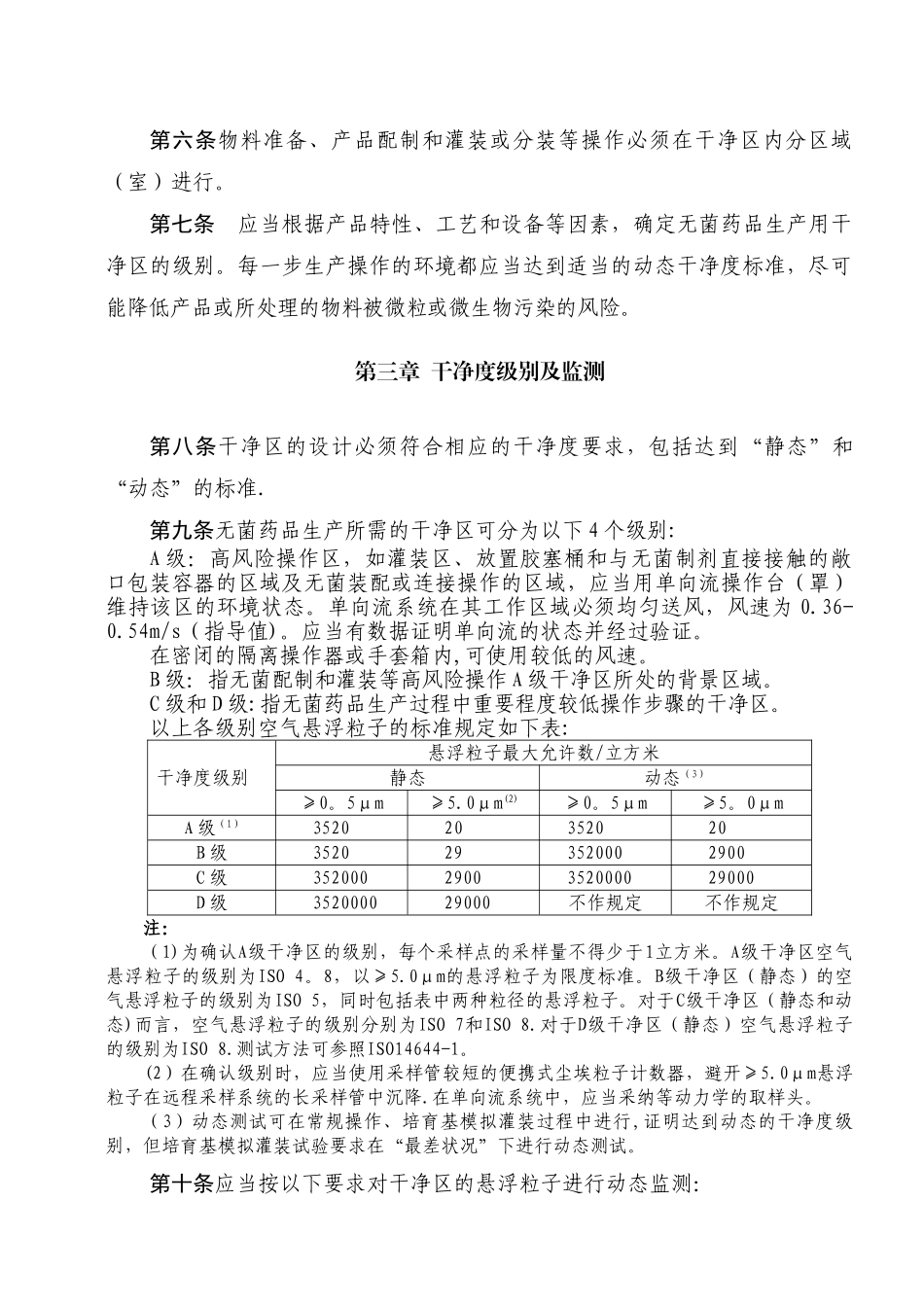
每一步生产操作的环境都应