实验名称:二组分溶液沸点--组成图的绘制班级:09 级应化一班 学号:202514120250报告人:裴哲民 同组人:匡江梅,李琪瑶,潘齐常,陈斌,梁细莲 实验时间:2011 年 9 月 16 日辅导老师:李传华一.实验目的1.测定常压下环己烷-乙醇二元系统的气液平衡数据,绘制沸点-组成相图
2.掌握双组分沸点的测定方法,通过实验进一步理解分馏原理
3.掌握阿贝折射仪的使用方法
二. 基本原理 在一定的外压下,纯液体的沸点是恒定的,但对于完全互溶双液系,沸点不仅与外压有关,而且还与其组成有关,并且在沸点时,平衡的气-液两相组成往往不同
根据相律:F=C-P+2,一个气液共存的二组分体系,其自由度为 2,只需再任意确定一个变量,其自由度就减为 1,整个体系的存在状态就可以用二维图来描述
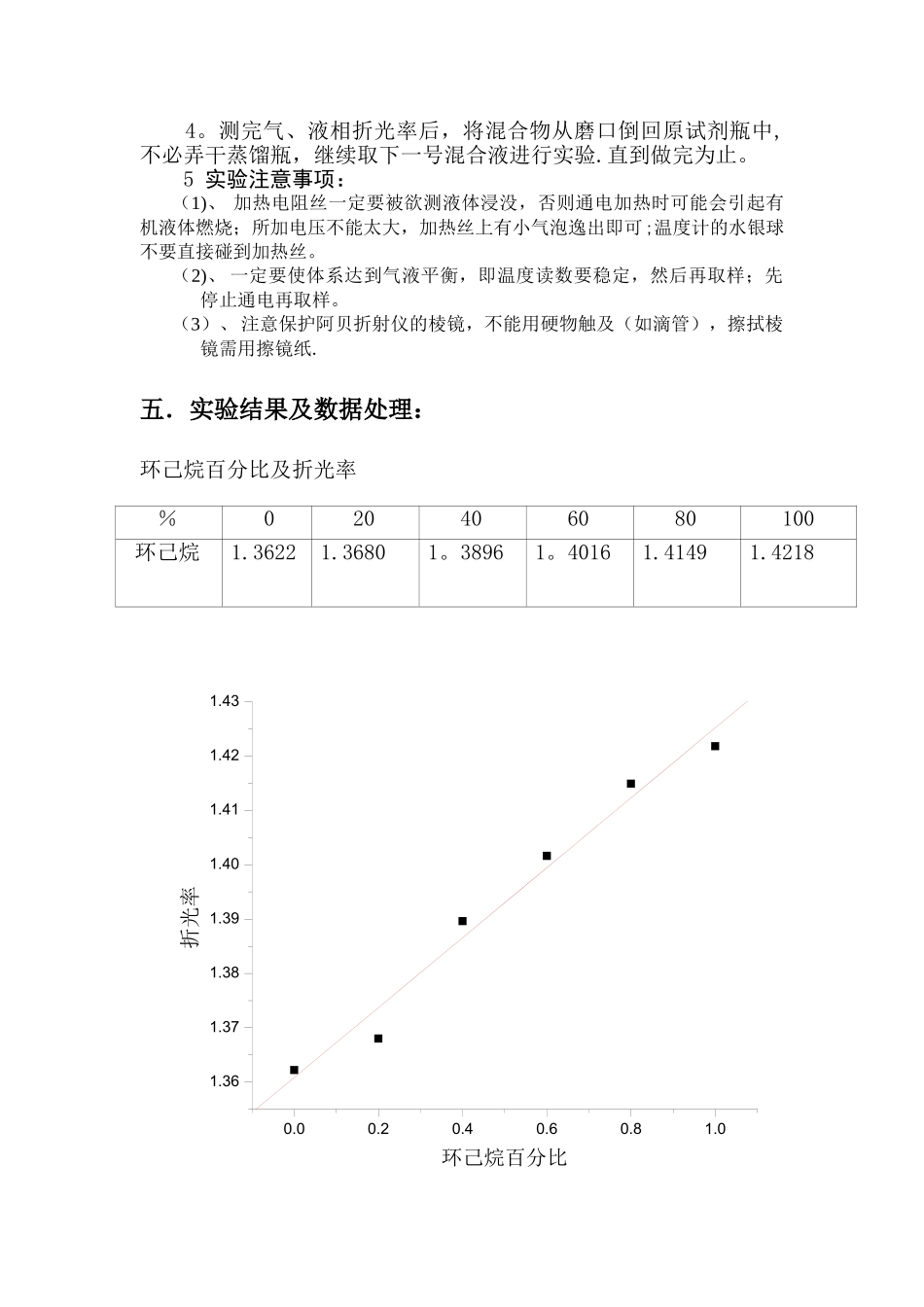
本实验中采纳在一定压力下,作出体系的温度 T 和组分 x 的关系图,即 T—x 图
完全互溶体系的 T—x 图可分为三类:①液体与 Raoult 定律的偏差不大,在 T—x 图上,溶液的沸点介于两种纯液体的沸点之间(图 1
a),如苯-甲苯系统;②由于两组分的相互作用,溶液与 Raoult 定律有较大的负偏差,在 T—x 图上存在最高沸点(图1
c),如卤化氢-水系统;③ 溶液与 Raoult 定律有较大的正偏差,在 T-x 图上存在最低沸点(图 1
b),如乙醇-水系统
②和③类溶液,在最高或最低沸点时的气—液两相组成相同,这些点称为恒沸点,此浓度的溶液称为恒沸点混合物,相应的温度称为恒沸温度,相应的组成称为恒沸组成
本实验所要测绘的环己烷-乙醇体系即属于第二类溶液
对于一个组成恒定的封闭系t/℃t/℃t/℃AAABBBxB(a)xB(b)气气气液液液xB(c)统,当系统达到气液平衡温度时,气液两相的组成和温度恒定不变,以此便能得到该温度下的平衡气—液两相组成的一对坐标
依次改变系统的组成