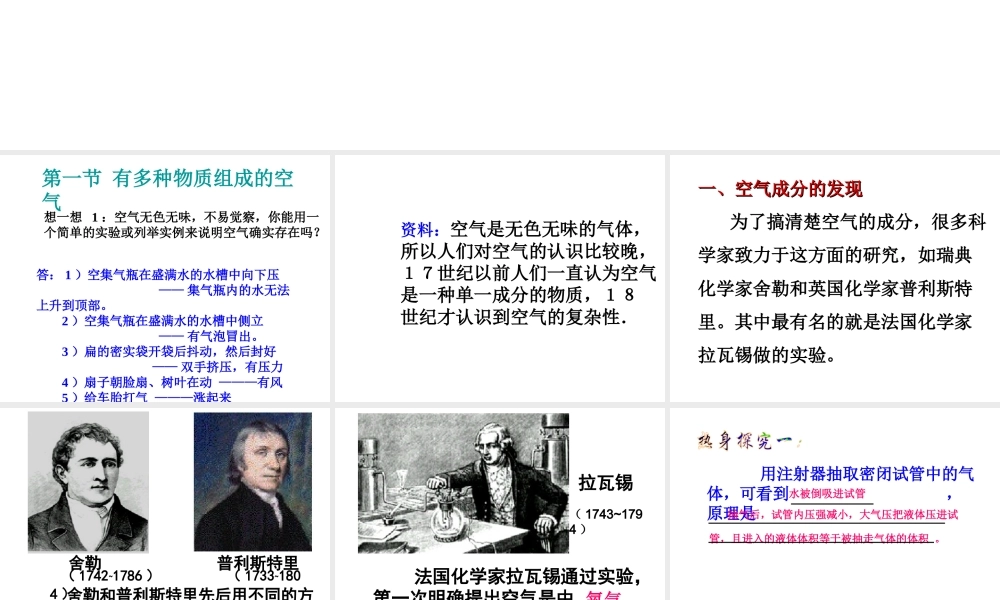
想一想 1 :空气无色无味,不易觉察,你能用一个简单的实验或列举实例来说明空气确实存在吗
答: 1 )空集气瓶在盛满水的水槽中向下压 —— 集气瓶内的水无法上升到顶部
2 )空集气瓶在盛满水的水槽中侧立 —— 有气泡冒出
3 )扁的密实袋开袋后抖动,然后封好 —— 双手挤压,有压力 4 )扇子朝脸扇、树叶在动 ———有风 5 )给车胎打气 ———涨起来第一节 有多种物质组成的空气 资料:空气是无色无味的气体,所以人们对空气的认识比较晚,17世纪以前人们一直认为空气是一种单一成分的物质,18世纪才认识到空气的复杂性.一、空气成分的发现一、空气成分的发现 为了搞清楚空气的成分,很多科学家致力于这方面的研究,如瑞典化学家舍勒和英国化学家普利斯特里
其中最有名的就是法国化学家拉瓦锡做的实验
舍勒 普利斯特里 ( 1742~1786 ) ( 1733~1804 ) 舍勒和普利斯特里先后用不同的方法制得了氧气
拉瓦锡( 1743~1794 ) 法国化学家拉瓦锡通过实验,第一次明确提出空气是由 和 组成的
氧气氮气 用注射器抽取密闭试管中的气体,可看到 , 原理是水被倒吸进试管 抽气后,试管内压强减小,大气压把液体压进试管,且进入的液体体积等于被抽走气体的体积
1 、空气中氧气含量的测定借助上述实验原理,设计实验方案,测定一瓶空气中氧气的含量
[ 实验指导 ] 认真看实验 2-1 观察与思考,注意领会操作要领, 3 分钟后能按正确步骤完成实验
一、探究空气的成分(一)空气中 O2 含量的测定1 、原理:红磷燃烧消耗了密闭容器内的 O2 ,使瓶内气压减少,打开止水夹后,在大气压的作用下,烧杯中的水倒流进瓶中,占据了瓶内原 O2 的体积
实验现象文字表达式 实验结论红磷燃烧时: 放出热量,产生大量的白烟 ( 固体小颗粒悬浮于空中)等装置冷却到室温后打开止水夹:水沿导管进入集气瓶且