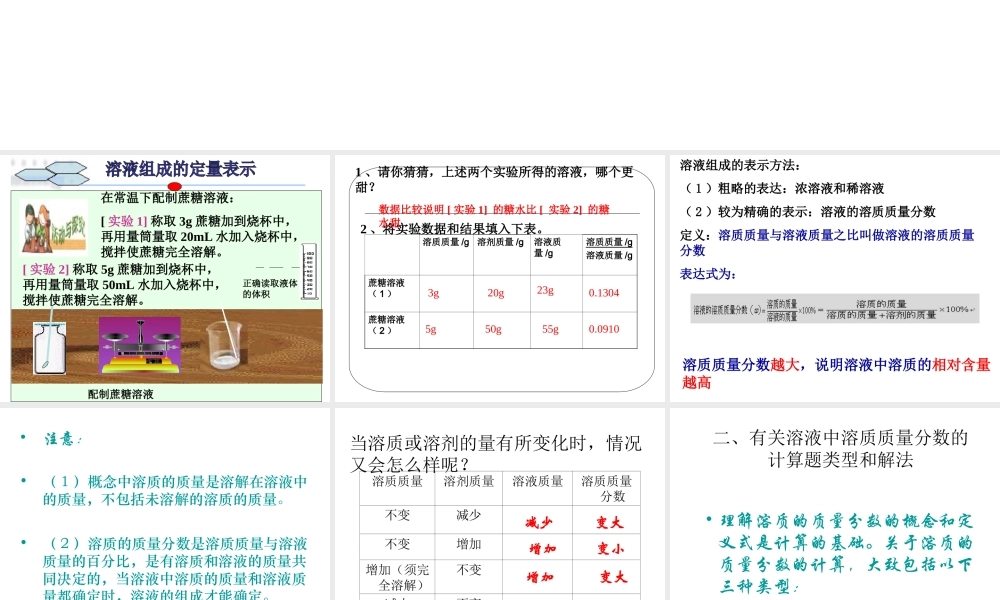
在常温下配制蔗糖溶液:[ 实验 1] 称取 3g 蔗糖加到烧杯中,再用量筒量取 20mL 水加入烧杯中,搅拌使蔗糖完全溶解
[ 实验 2] 称取 5g 蔗糖加到烧杯中,再用量筒量取 50mL 水加入烧杯中,搅拌使蔗糖完全溶解
正确读取液体的体积配制蔗糖溶液1 、请你猜猜,上述两个实验所得的溶液,哪个更甜
2 、将实验数据和结果填入下表
溶质质量 /g溶剂质量 /g溶液质量 /g溶质质量 /g溶液质量 /g蔗糖溶液( 1 )蔗糖溶液( 2 )3g20g23g5g50g55g0
0910数据比较说明 [ 实验 1] 的糖水比 [ 实验 2] 的糖水甜溶液组成的表示方法:( 1 )粗略的表达:浓溶液和稀溶液( 2 )较为精确的表示:溶液的溶质质量分数定义:溶质质量与溶液质量之比叫做溶液的溶质质量分数表达式为:溶质质量分数越大,说明溶液中溶质的相对含量越高•注意:•( 1 )概念中溶质的质量是溶解在溶液中的质量,不包括未溶解的溶质的质量
•( 2 )溶质的质量分数是溶质质量与溶液质量的百分比,是有溶质和溶液的质量共同决定的,当溶液中溶质的质量和溶液质量都确定时,溶液的组成才能确定
当溶质或溶剂的量有所变化时,情况又会怎么样呢
溶质质量溶剂质量溶液质量溶质质量分数不变减少不变增加增加(须完全溶解)不变减少不变增加增加变小变大减少变小变大减少二、有关溶液中溶质质量分数的计算题类型和解法• 理解溶质的质量分数的概念和定义式是计算的基础
关于溶质的质量分数的计算,大致包括以下三种类型:例 1 :实验 1 :称取 10g 白糖加到烧杯中
再加入40g 水,搅拌,使白糖溶解
实验 2 :称取 12g 白糖加到另一烧杯中
再加入 48g 水,搅拌,使白糖溶解
问题:实验 1 、 2 所得两种糖水,那种更甜
你的根据是什么
已知溶质和溶剂的量,计算溶质的质量分数
[ 分析 ]实验