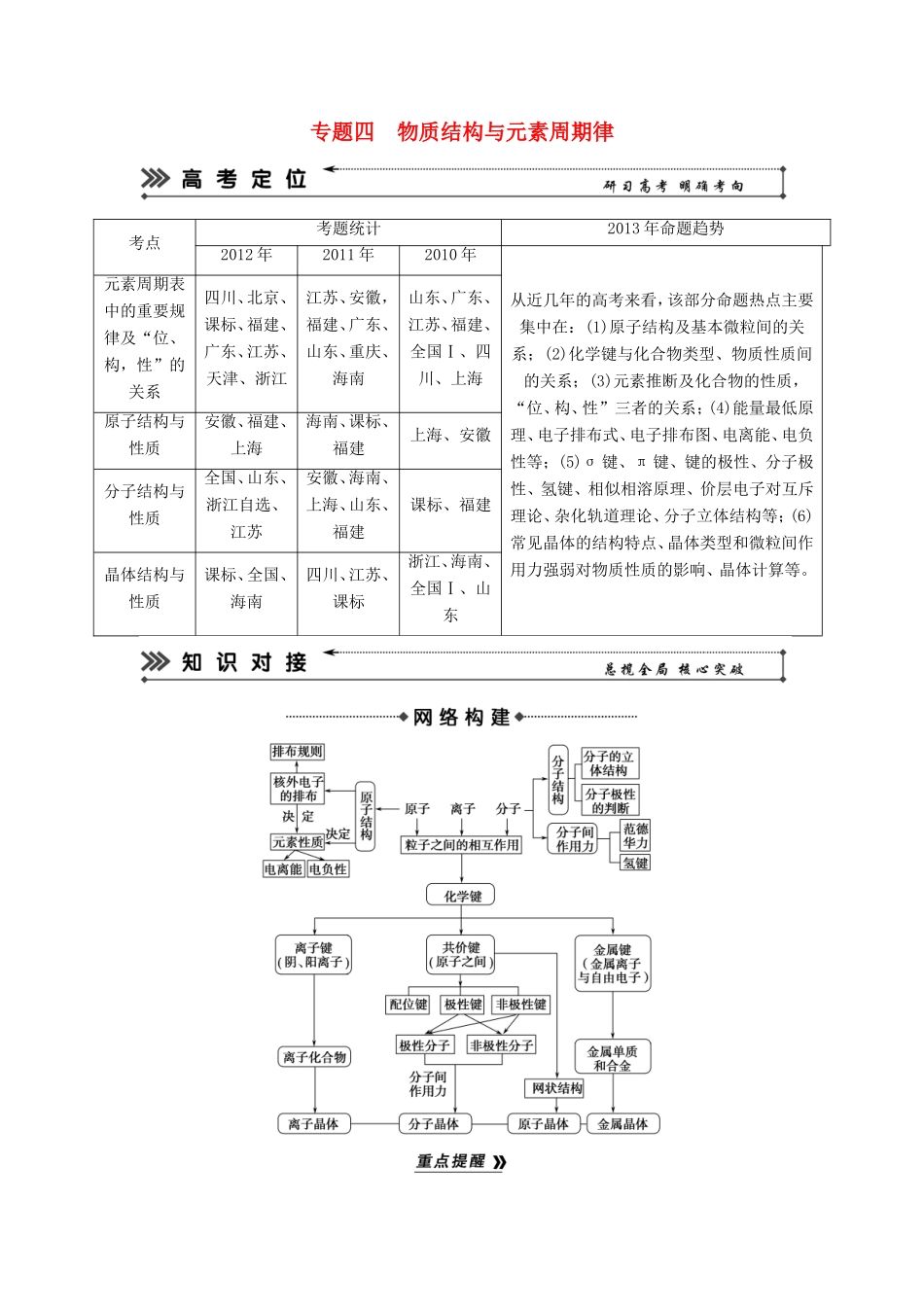
专题四物质结构与元素周期律考点考题统计2013年命题趋势2012年2011年2010年从近几年的高考来看,该部分命题热点主要集中在:(1)原子结构及基本微粒间的关系;(2)化学键与化合物类型、物质性质间的关系;(3)元素推断及化合物的性质,“位、构、性”三者的关系;(4)能量最低原理、电子排布式、电子排布图、电离能、电负性等;(5)σ键、π键、键的极性、分子极性、氢键、相似相溶原理、价层电子对互斥理论、杂化轨道理论、分子立体结构等;(6)常见晶体的结构特点、晶体类型和微粒间作用力强弱对物质性质的影响、晶体计算等
元素周期表中的重要规律及“位、构,性”的关系四川、北京、课标、福建、广东、江苏、天津、浙江江苏、安徽,福建、广东、山东、重庆、海南山东、广东、江苏、福建、全国Ⅰ、四川、上海原子结构与性质安徽、福建、上海海南、课标、福建上海、安徽分子结构与性质全国、山东、浙江自选、江苏安徽、海南、上海、山东、福建课标、福建晶体结构与性质课标、全国、海南四川、江苏、课标浙江、海南、全国Ⅰ、山东1.原子的构成微粒及其数量关系
2.原子核外电子排布规律
3.同主族、同周期元素的性质
4.元素的电离能、电负性
5.共价键类型、极性与分子的极性
6.杂化轨道理论、价层电子对互斥理论
7.分子间的作用力与氢键
8.晶体结构及类型对物质性质的影响
1.核外电子排布遵循哪些原理
答案(1)能量最低原理:原子核外的电子排布遵循构造原理使整个原子的能量处于最低状态;(2)泡利原理:1个原子轨道里最多只能容纳2个电子,而且自旋方向相反;(3)洪特规则:当电子排布在同一能级的不同轨道时,总是优先单独占据一个轨道,而且自旋方向相同
2.元素性质周期性变化规律的内容是什么
答案(1)原子半径:同一周期元素从左到右,原子半径越来越小;同一主族元素从上到下,原子半径越来越大
(2)电离能:同一周期元素从左到右,电离