(45分钟100分)一、选择题(本题包括15小题,每小题4分,共60分)1
在以下的分子或离子中,空间结构的几何形状不是三角锥形的是()A
下列有关金属键的叙述中错误的是()A
金属键没有饱和性和方向性B
金属键是指金属阳离子和自由电子之间强烈的静电吸引作用C
金属键中的电子属于整块金属D
金属的性质和金属固体的形成都与金属键有关3
(2012·日照高二检测)下列元素的原子在形成不同物质时,既可形成离子键,又可形成极性键和非极性键的是()A
(双选)下列描述中正确的是()A
CS2为V形的极性分子B
ClO3-的空间构型为平面三角形C
SF6中有6对完全相同的成键电子对D
SiF4和SO32-的中心原子均为sp3杂化5
下列关于氢键的说法中不正确的是()A
HF的沸点比HCl的沸点高是由于HF分子间存在氢键B
水在结冰时体积膨胀,是由于水分子之间存在氢键C
NH3的稳定性很强,是因为其分子间能形成氢键D
在氨水中水分子和氨分子之间也存在着氢键6
(2012·宿州高二检测)下列关于离子键和离子化合物的说法中正确的是()A
阴、阳离子通过静电引力形成离子键B
阴、阳离子间通过离子键一定能形成离子化合物C
离子化合物一定能导电D
只有在活泼金属元素和活泼非金属元素化合时,才能形成离子键7
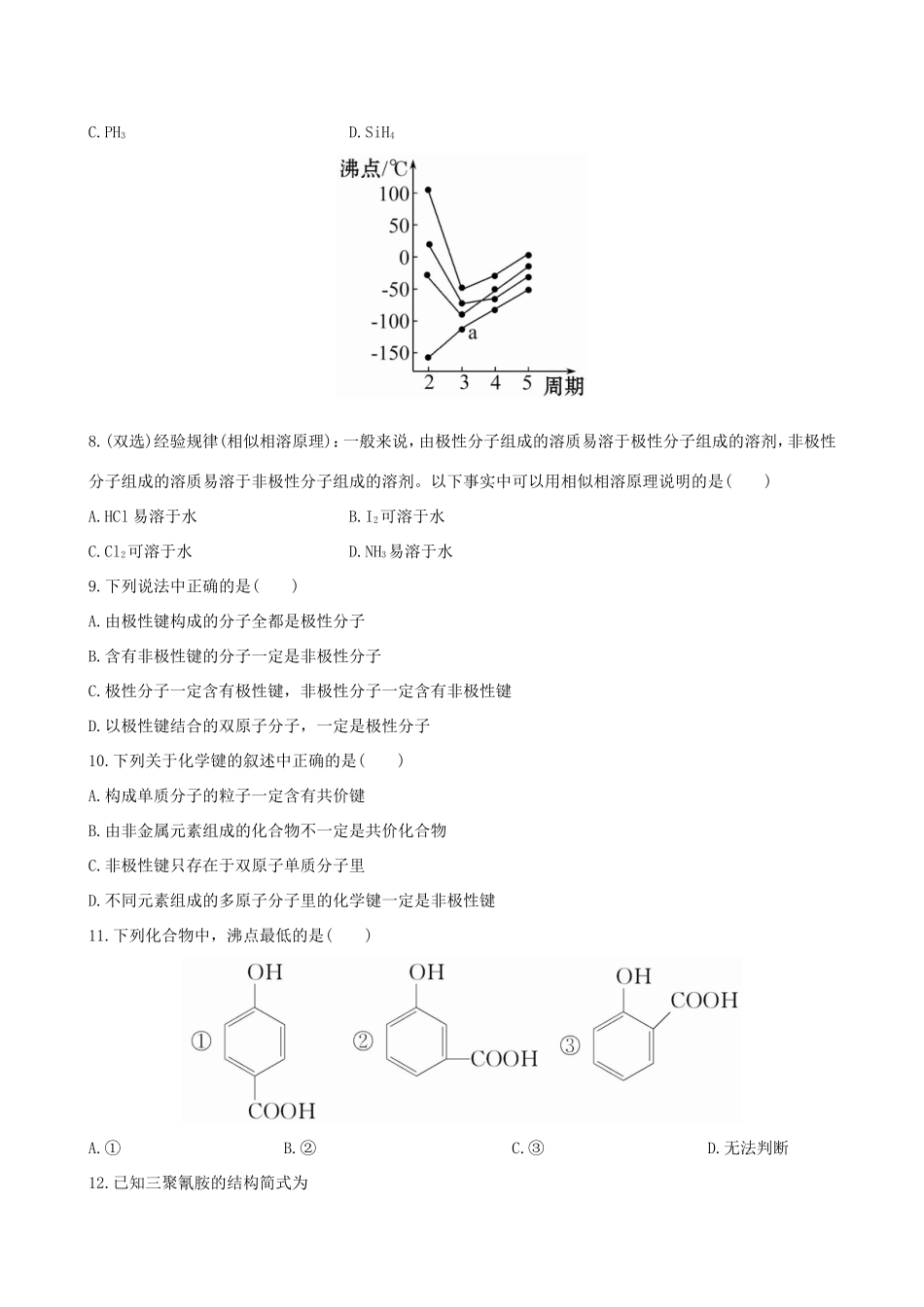
如图所示每条折线表示周期表ⅣA族~ⅦA族中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是()A
(双选)经验规律(相似相溶原理):一般来说,由极性分子组成的溶质易溶于极性分子组成的溶剂,非极性分子组成的溶质易溶于非极性分子组成的溶剂
以下事实中可以用相似相溶原理说明的是()A
HCl易溶于水B
I2可溶于水C
Cl2可溶于水D
NH3易溶于水9