氧气、二氧化碳的制法课题一轮复习-3氧气、二氧化碳的制法复备人教学时间教学目标1.了解实验室制取气体的方法和设计思路;2.学会氧气、二氧化碳的实验室制法,初步理解操作原理
教学重点掌握O2、CO2制法教学难点根据制取气体、收集气体原理解决相关实验题教学方法讨论、归纳、比较教学媒体电子白板【教学过程】:【创设情景】:【明确目标】:一、回顾、预习与交流(一).氧气的实验室制备1.反应原理:高锰酸钾制氧气(化学方程式)氯酸钾制氧气(化学方程式)双氧水制氧气(化学方程式)反应物为固体,反应条件为加热时,可选用装置;反应物为,反应条件为时,可选用装置B或C;2.收集方法:因为氧气,可用法收集;因为氧气,可用法收集;3.验满方法:复备栏(1)若用排水法收集时,当看到,表明氧气已收集满;(2)若用向上排空气法收集时,则用带火星的木条放在,若,说明氧气已收集满
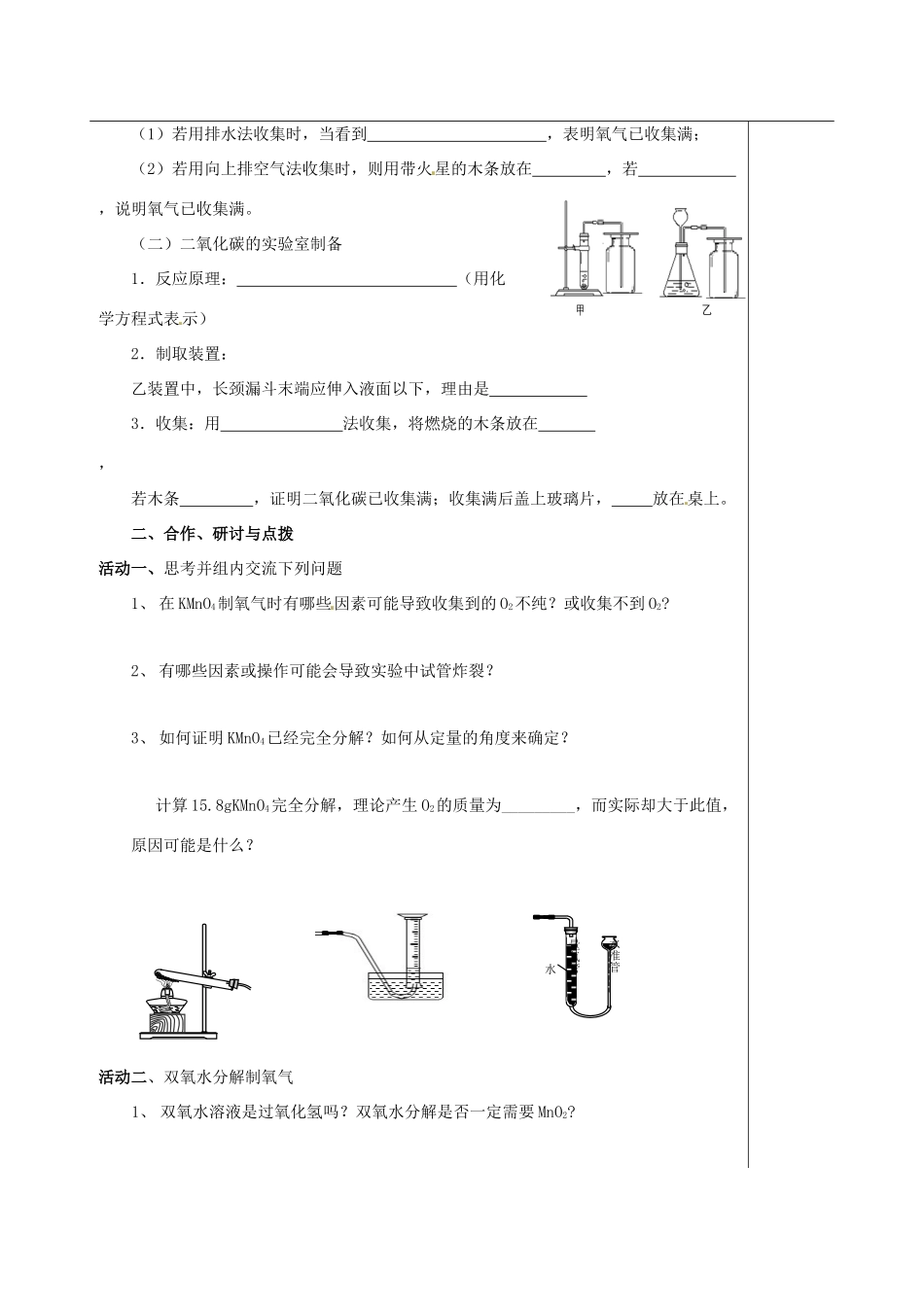
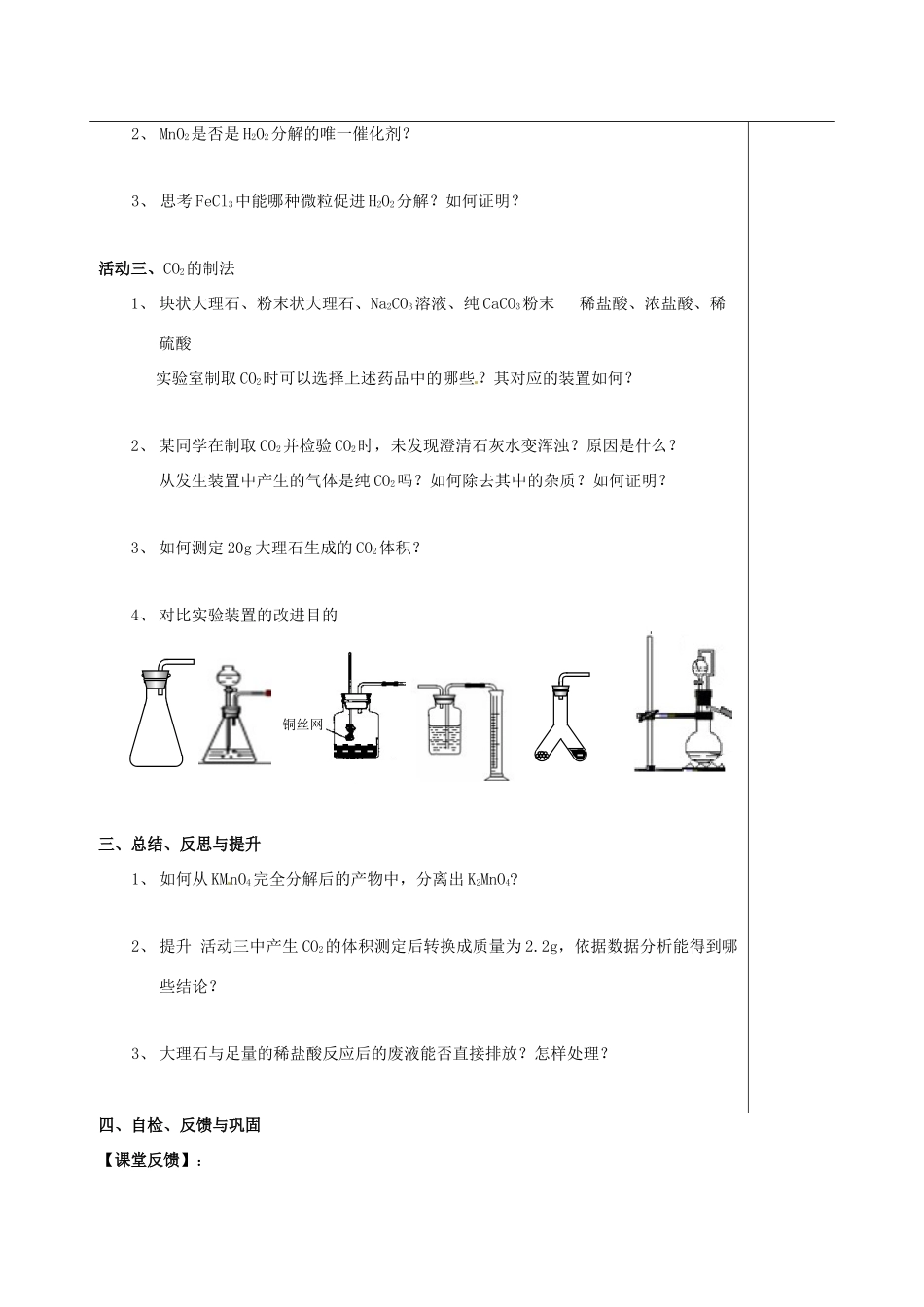
(二)二氧化碳的实验室制备1.反应原理:(用化学方程式表示)2.制取装置:乙装置中,长颈漏斗末端应伸入液面以下,理由是3.收集:用法收集,将燃烧的木条放在,若木条,证明二氧化碳已收集满;收集满后盖上玻璃片,放在桌上
二、合作、研讨与点拨活动一、思考并组内交流下列问题1、在KMnO4制氧气时有哪些因素可能导致收集到的O2不纯
或收集不到O2
2、有哪些因素或操作可能会导致实验中试管炸裂
3、如何证明KMnO4已经完全分解
如何从定量的角度来确定
8gKMnO4完全分解,理论产生O2的质量为_________,而实际却大于此值,原因可能是什么
活动二、双氧水分解制氧气1、双氧水溶液是过氧化氢吗
双氧水分解是否一定需要MnO2
量气管水水准管2、MnO2是否是H2O2分解的唯一催化剂
3、思考FeCl3中能哪种微粒促进H2O2分解
活动三、CO2的制法1、块状大理石、粉末状大理石、Na2CO3溶液、纯CaCO3粉末稀盐