山东省茌平县博平镇中学九年级化学下册《酸和碱的性质》复习教案新人教版复习目标:1、掌握常见酸和碱的俗称、化学式、物理性质和化学性质,2、通过复习形成知识网络,找到解题的方法和技巧,培养学生分析问题、解决问题的能力
复习学案:一、以小组为单位,对子之间相互检测基础知识
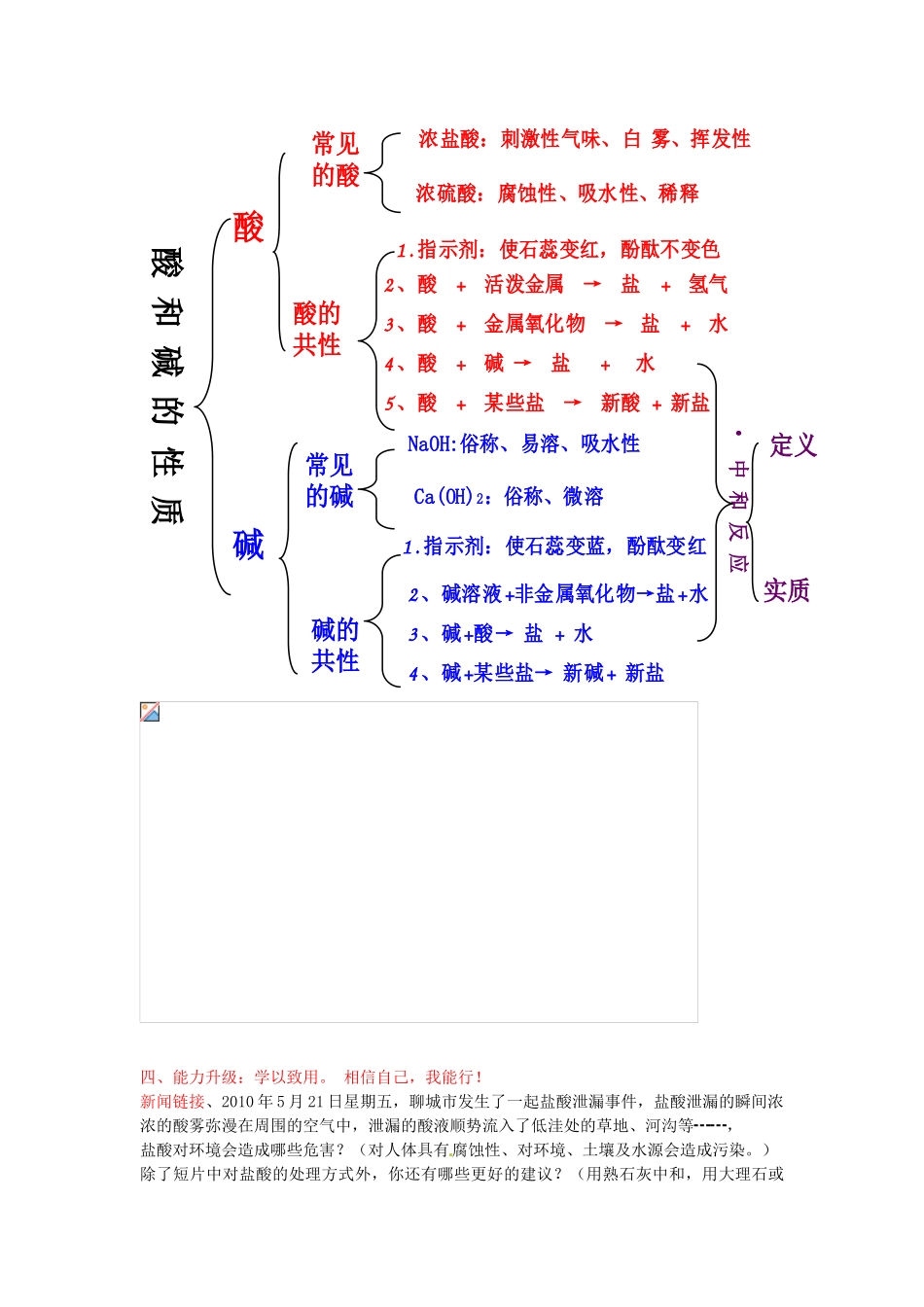
1、常见酸:浓硫酸、浓盐酸的物理性质色、态、味挥发性吸水性腐蚀性浓盐酸无色液体、具有刺激性气味有无有浓硫酸无色液体、无味无有有2、酸的化学性质:(各写出一个反应的化学方程式)1、酸能使紫色石蕊试液变红;无色酚酞试液不变色;2、酸+活泼金属→盐+氢气Fe+2HCl==FeCl2+H2↑3、酸+金属氧化物→盐+水Fe2O3+6HCl==2FeCl3+3H2O4、酸+碱→盐+水(中和反应)HCl+NaOH==NaCl+H2O5、酸+某些盐→新酸+新盐CaCO3+2HCl==CaCl2+H2O+CO2↑二、碱的性质1、常见碱:氢氧化钠、氢氧化钙的俗称及物理性质:俗称化学式色、态水溶性吸水性腐蚀性氢氧化钠苛性钠、烧碱、火碱NaOH白色固体易溶有有氢氧化钙熟石灰、生石灰Ca(OH)2白色固体微溶无有2、碱的化学性质:(各写出一个反应的化学方程式)1、碱溶液能使紫色石蕊试液变蓝,无色酚酞试液变红
2、碱溶液+非金属氧化物→盐+水Ca(OH)2+CO2==CaCO3↓+H2O3、碱+酸→盐+水Ca(OH)2+2HCl==CaCl2+2H2O4、碱+某些盐→新碱+新盐Na2CO3+Ca(OH)2==CaCO3↓+NaOH基础闯关:知识竞答
比一比,我能赢
1、浓盐酸与浓硫酸共同的物理性质有哪些
(无色、液体)2、用手在盛浓盐酸的瓶口轻轻扇动,会闻到什么气味
(刺激性气味)3、浓盐酸敞口放置在空气中,会产生什么现象
(白雾)4、怎样稀释浓硫酸
(把浓硫酸沿器壁慢慢注入水中,并不断用玻璃棒搅拌;防止酸液四处飞溅)5、氢氧化钠