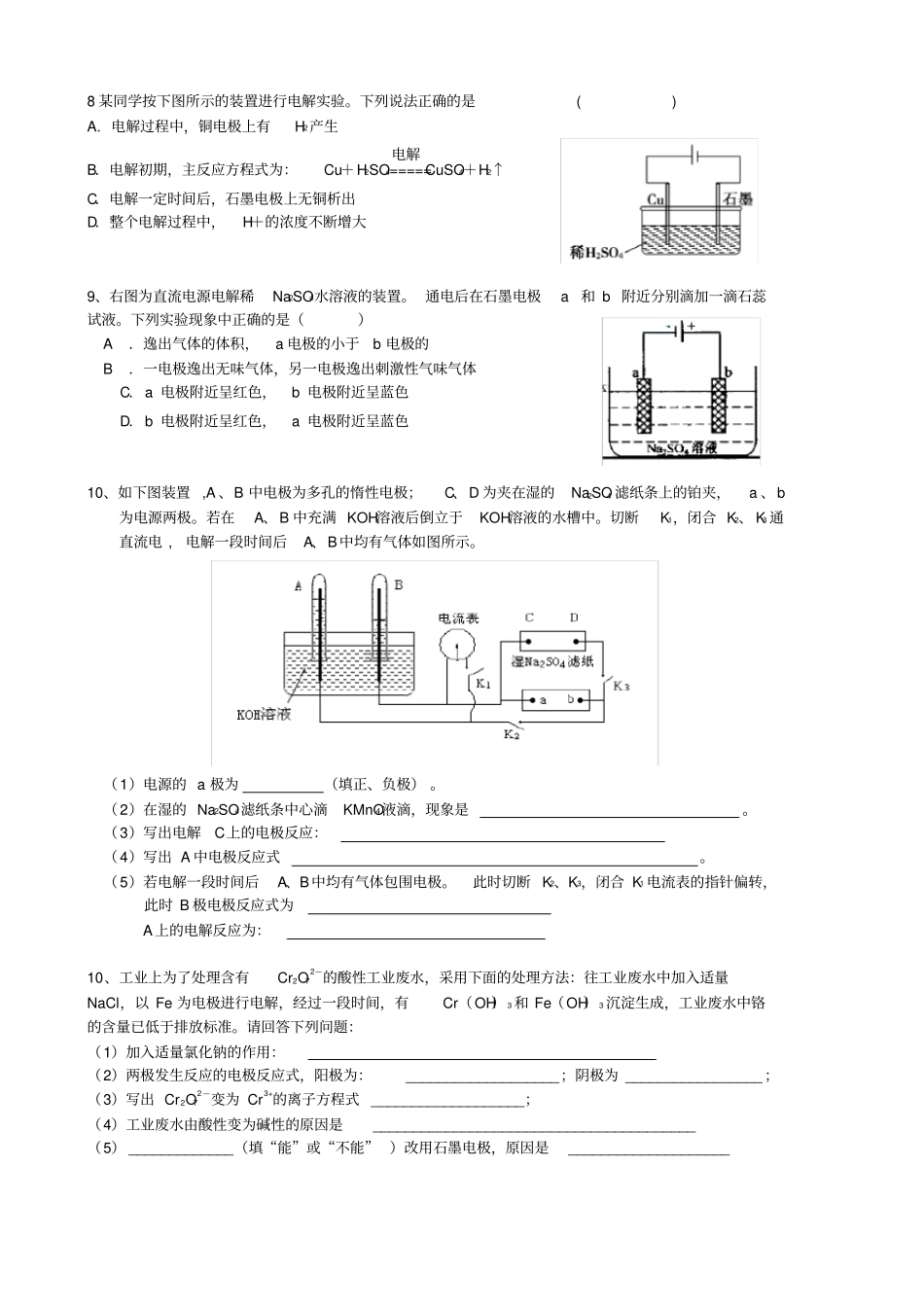
专题复习一电解复习一、知识总结:1、惰性电极指的是:活性电极指的是:2、离子的放电顺序问题:(1)阳极发生:,强的先反应,若为活性电极,若为惰性电极,则,放电顺序为(2)阴极发生:,强的先反应,阴极任何时候都是:放电,放电顺序为:3、如图所示回答下列问题阳极的电极反应为:阴极电极反应为:总方程式:。实现的能量转化是:随着电解的进行溶液的pH将会:(填升高,减低或不变)若让电解后的溶液恢复到原来的浓度,应该加的物质是:。若硝酸银溶液的体积是100ml,电解的结果,阴极增重了0.108克,则电解后溶液常温的pH为:(溶液体积变化不计)。请分析硝酸在哪个极上产生的,原因是:。二、电解规律(用惰性电极电解)电解类型物质类型电解总反应电解实质电解质溶液中浓度变化pH变化电解质溶液复原来电解溶剂型强碱(NaOH)含氧酸(H2SO4)活泼金属的含氧酸盐(Na2SO4)电解溶质型无氧酸(HCl)不活泼金属的无氧酸盐(CuCl2)溶质溶剂同时被电解活泼金属的无氧酸盐(NaCl)不活泼金属的含氧酸盐(CuSO4)不活泼金属的含氧酸盐(AgNO3)强化训练1、pH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH<a,则该电解质可能的是()A、NaOHB、NaClC、AgNO3D、Na2SO42、用铂电极(惰性)电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是()A.稀盐酸B.硫酸铜溶液C.稀硫酸溶液D.酸性AgNO3溶液3、X、Y、Z、M代表四种金属元素。金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为()AX>Z>Y>MBX>Y>Z>MCM>Z>X>YDX>Z>M>Y4、用惰性电极实现电解,下列说法正确的是()A电解稀硫酸溶液,实质上是电解水,故溶液pH不变B电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小C电解硫酸钠溶液,在阴极上和阳极上析出产物的物质的量之比为1:2D电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:15、化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是()A.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-==Cl2↑B.氢氧燃料电池的负极反应式:O2+2H2O+4e-==4OH-C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-==Cu2+D.钢铁发生电化学腐蚀的正极反应式:Fe-2e-==Fe2+6、用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是A.燃料电池工作时,正极反应为:O2+2H2O+4e-===4OH-B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等7、如下图所示,下列叙述正确的是()A.Y为阴极,发生还原反应B.X为正极,发生氧化反应C.Y与滤纸接触处有氧气生成D.X为滤纸接触处变红H2CuSO4溶液含金属催化剂的多孔电极酸性电解质O2H2O8某同学按下图所示的装置进行电解实验。下列说法正确的是()A.电解过程中,铜电极上有H2产生B.电解初期,主反应方程式为:Cu+H2SO4=====电解CuSO4+H2↑C.电解一定时间后,石墨电极上无铜析出D.整个电解过程中,H+的浓度不断增大9、右图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加一滴石蕊试液。下列实验现象中正确的是()A.逸出气体的体积,a电极的小于b电极的B.一电极逸出无味气体,另一电极逸出刺激性气味气体C.a电极附近呈红色,b电极附近呈蓝色D.b电极附近呈红色,a电极附近呈蓝色10、如下图装置,A、B中电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条上的铂夹,a、b为电源两极。若在A、B中充满KOH溶液后倒立于KOH溶液的水槽中。切断K1,闭合K2、K3通直流电,电解一段时间后A、B中均有气体如图所示。(1)电源的a极为(填正、负极)。(2)在湿的Na2SO4滤纸条中心滴KMnO4液滴,现象是。(3)写出电解C上的电极反应:(4)写出A中电极反应式。(5)若电解一段时间后A、B中均有气体包围电极。此时切断K2、K3,闭合K1电流表的指针偏转,此时B极电...