第2课时离子晶体过渡晶体与混合型晶体发展目标体系构建1
借助离子晶体模型认识离子晶体的结构和性质
能利用离子键的有关理论解释离子晶体的物理性质
知道介于典型晶体之间的过渡晶体及混合型晶体是普遍存在的
一、离子晶体1.结构特点(1)构成粒子:阳离子和阴离子
(2)作用力:离子键
(3)配位数:一个离子周围最邻近的异电性离子的数目
微点拨:大量离子晶体的阴离子或阳离子不是单原子离子,有的还存在电中性分子
离子晶体中不仅有离子键还存在共价键、氢键等
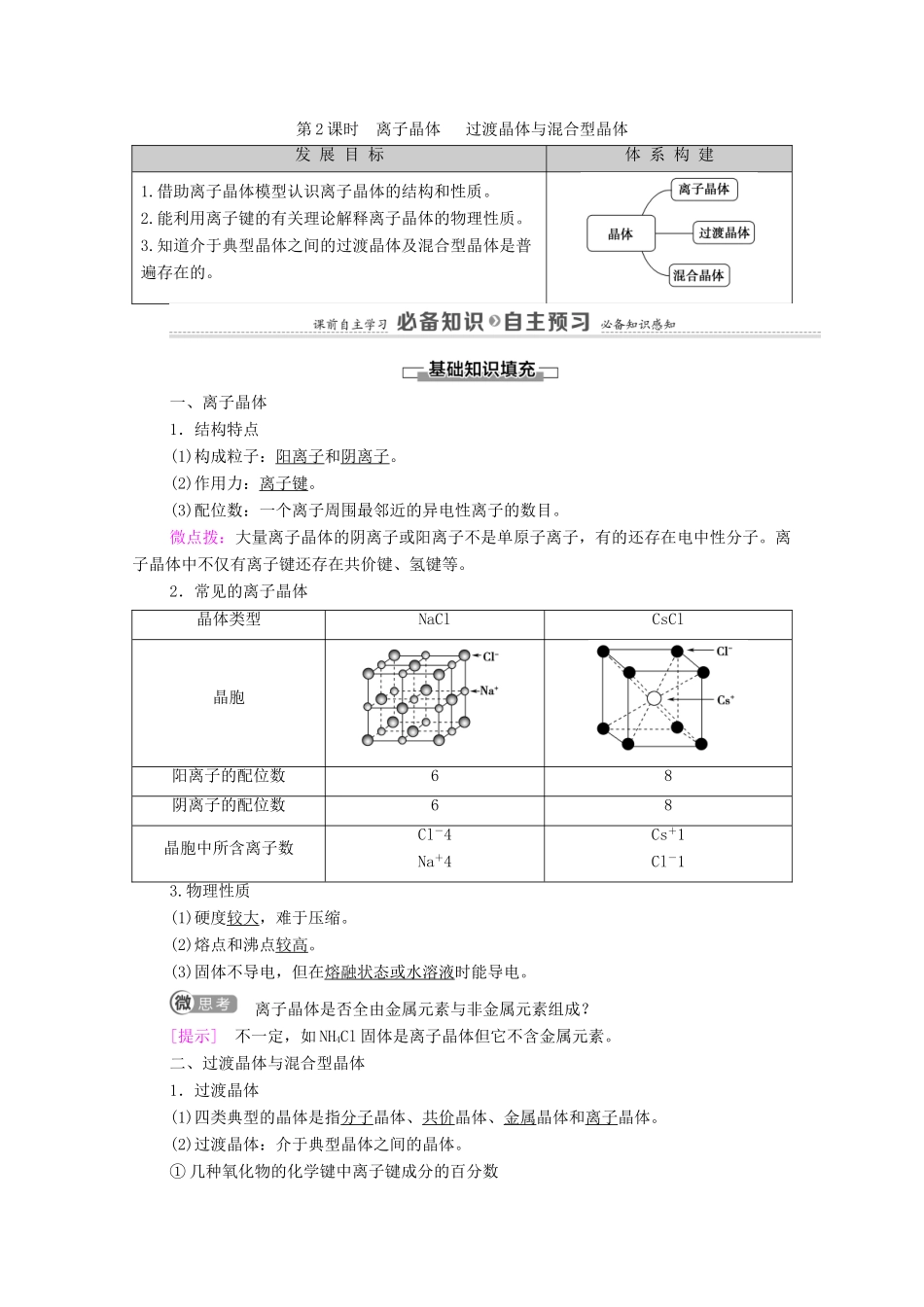
2.常见的离子晶体晶体类型NaClCsCl晶胞阳离子的配位数68阴离子的配位数68晶胞中所含离子数Cl-4Na+4Cs+1Cl-13
物理性质(1)硬度较大,难于压缩
(2)熔点和沸点较高
(3)固体不导电,但在熔融状态或水溶液时能导电
离子晶体是否全由金属元素与非金属元素组成
[提示]不一定,如NH4Cl固体是离子晶体但它不含金属元素
二、过渡晶体与混合型晶体1.过渡晶体(1)四类典型的晶体是指分子晶体、共价晶体、金属晶体和离子晶体
(2)过渡晶体:介于典型晶体之间的晶体
①几种氧化物的化学键中离子键成分的百分数氧化物Na2OMgOAl2O3SiO2离子键的百分数/%62504133从上表可知,表中4种氧化物晶体中的化学键既不是纯粹的离子键,也不是纯粹的共价键,这些晶体既不是纯粹的离子晶体也不是纯粹的共价晶体,只是离子晶体与共价晶体之间的过渡晶体
②偏向离子晶体的过渡晶体在许多性质上与纯粹的离子晶体接近,因而通常当作离子晶体来处理,如Na2O等
同样,偏向共价晶体的过渡晶体则当作共价晶体来处理,如Al2O3、SiO2等
微点拨:四类典型晶体都有过渡晶体存在
2.混合型晶体(1)晶体模型石墨结构中未参与杂化的p轨道(2)结构特点——层状结构①同层内碳原子采取sp2杂化,以共价键(σ键)结合,形成平面六元并环结构
②层与层之间靠