第1课时焓变反应热[明确学习目标]1
了解化学反应中能量转化的原因,能说出常见的能量转化形式
了解反应热和焓变的含义
一、焓变反应热1.焓与焓变(1)焓(H):与□内能有关的物理量
(2)焓变(ΔH):生成物与反应物的□焓值差,决定了某一化学反应是吸热反应还是放热反应
2.反应热(1)概念:化学反应过程中所□放出或吸收的能量
(2)与焓变的关系:□恒压条件下的反应热等于焓变
(3)单位:□kJ·mol-1
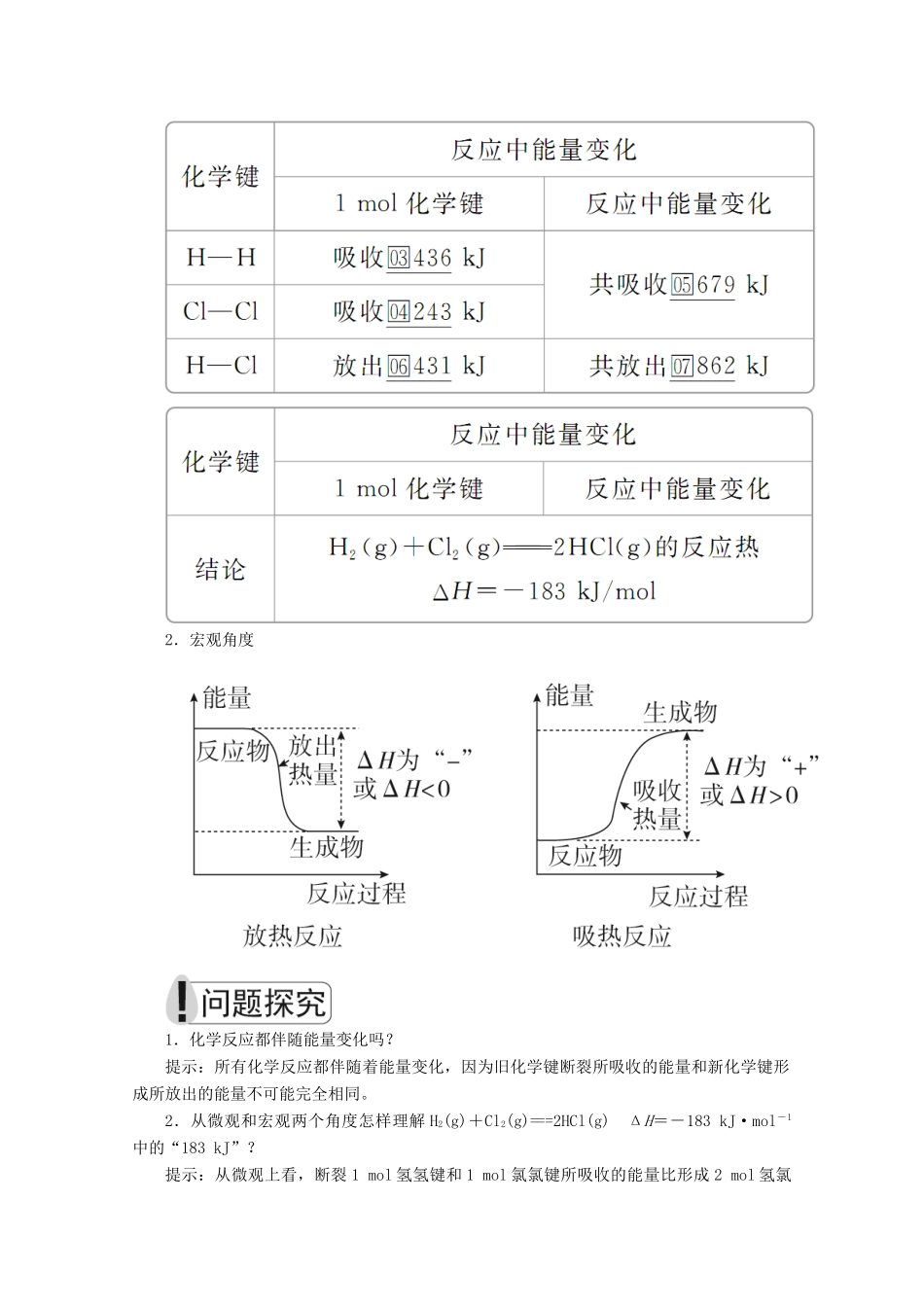
二、化学反应过程中能量变化的原因1.微观角度(1)化学反应的本质:(2)以H2(g)+Cl2(g)===2HCl(g)反应的能量变化为例:2.宏观角度1.化学反应都伴随能量变化吗
提示:所有化学反应都伴随着能量变化,因为旧化学键断裂所吸收的能量和新化学键形成所放出的能量不可能完全相同
2.从微观和宏观两个角度怎样理解H2(g)+Cl2(g)===2HCl(g)ΔH=-183kJ·mol-1中的“183kJ”
提示:从微观上看,断裂1mol氢氢键和1mol氯氯键所吸收的能量比形成2mol氢氯键释放的能量少183kJ
从宏观上看1molH2(g)和1molCl2(g)所具有的总能量比2molHCl(g)所具有的总能量多183kJ
3.H2(g)和Cl2(g)在光照条件下也可以发生上述反应,那么该反应的ΔH是否发生变化
提示:焓变不发生变化,ΔH仍为-183kJ·mol-1;因为化学反应的焓变与反应条件无关
一、焓变反应热1.ΔH=H生成物-H反应物
2.影响ΔH大小的因素有:参加反应的物质的物质的量的多少;反应体系的温度和压强;反应体系中物质的聚集状态
[即时练]1.判断正误(正确的打“√”,错误的打“×”):(1)反应热即化学反应过程中所放出的热量
()(2)焓是用来描述物质所具有能量高低的物理量
()(3)焓变是反应物与生成物的焓值差
()(4)焓变的单位与能量的单位