第一节原子结构模型的演变(1课时)【教学目标】了解原子结构模型的演变,认识假说、实验等科学方法在人类探索原子结构奥秘过程的作用
【教学重难点】认识假说、实验等科学方法在人类探索原子结构奥秘过程的作用
【教学过程】〖问题导学〗1、什么叫原子
2、科学家眼中的原子是怎样的
3、科学家是怎样探索原子结构的
4、有哪些科学家为探索原子结构作出了重大贡献
5、你认为实验的方法是科学研究的重要方法吗
实验手段的不断进步是化学发展的一个关键吗
6、何为8电子稳定结构
7、原子核外最外层电子数与元素的性质有什么关系
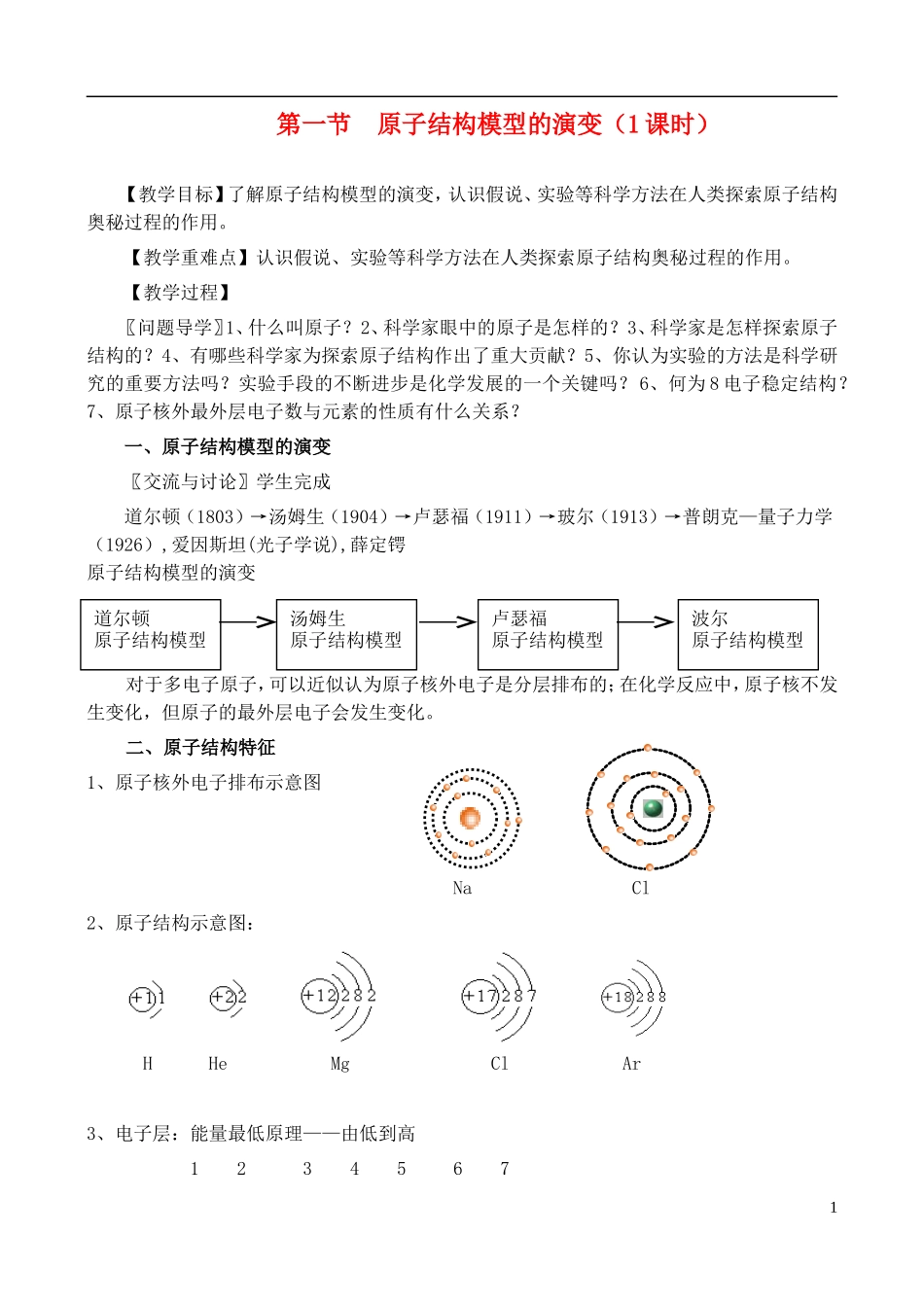
一、原子结构模型的演变〖交流与讨论〗学生完成道尔顿(1803)→汤姆生(1904)→卢瑟福(1911)→玻尔(1913)→普朗克—量子力学(1926),爱因斯坦(光子学说),薛定锷原子结构模型的演变对于多电子原子,可以近似认为原子核外电子是分层排布的;在化学反应中,原子核不发生变化,但原子的最外层电子会发生变化
二、原子结构特征1、原子核外电子排布示意图NaCl2、原子结构示意图:HHeMgClAr3、电子层:能量最低原理——由低到高12345671道尔顿原子结构模型汤姆生原子结构模型卢瑟福原子结构模型波尔原子结构模型KLMNOPQ4、核外电子的排布规律(请熟记1~20号元素):四不超规律
最外层电子数排不超过8个(K层为最外层时不超过2个),次外层不超过18个,倒数第三层不超过32个,每一层最多容纳的个数为2n2个
〖交流与讨论〗学生完成5、8电子稳定结构Mg2+、O2-、Cl-、Na+、CO2、Cl2、N2但有物质不遵守8电子规则,如BeCl2、BF3、H2、He、PCl5〖问题解决〗学生完成三、核外电子排布与元素性质的关系(1)活泼的金属在化学反应中易失去电子,活泼非金属在化学反应中易得到电子
(2)金属元素:一般化合价数=最外层电子数非金属元素:一般化合价数=8—最外层