海水中的化学元素第二课时知识和技能1.使学生掌握卤族元素的主要物理性质和化学性质,学会比较卤素单质的氧化性强弱;2.使学生对溴的化合物的用途有一个初步的认识;3.认识卤素的一些特殊性质;4.培养学生的比较、分析、归纳能力
过程和方法1.通过对卤索性质的实验探究、对比、归纳来学习它们的性质;2.通过性质的了解,分析它们的用途
情感、态度与价值观1.通过实验探究,进一步加强学生认识物质的准确方法,进一步提高学生对知识的探究欲和探索精神;2.认识物质对人类生活、生产的作用,激发学生珍爱自然资源的情感
教学重点:卤素的物理性质、化学性质教学难点:卤素的化学性质教具准备:投影仪、试管、试管夹、酒精灯、火柴、氯气、液溴、碘固体、氯水、溴水、碘水、NaCl溶液、NaBr溶液、KI淀粉溶液、酒精、四氯化碳、AgNO3溶液、稀硝酸教学过程:[引入新课]上一节课,我们大家一起探讨了海水中的丰富元素,重点学习了NaCl、Mg的性质
今天这堂课,我们将要继续来探究海水中其他元素的性质
不过,今天这堂课主要是靠我们同学自己来探究它们的性质,行吗
对自己有信心吗
学生非常响亮的回答:有
[推进新课]本节课我们要探究的是溴以及与溴性质相似的一类物质——卤素的性质
[板书]三、卤素[讲解]氯、溴、碘等元素因为在原子结构和元素性质上有相似的方面,因此,我们把它们归在一起,统称为卤素
(展示样品)一瓶液溴、一瓶氯气、一瓶碘单质
请学生通过自己的探究活动来认识它们的物理用心爱心专心性质
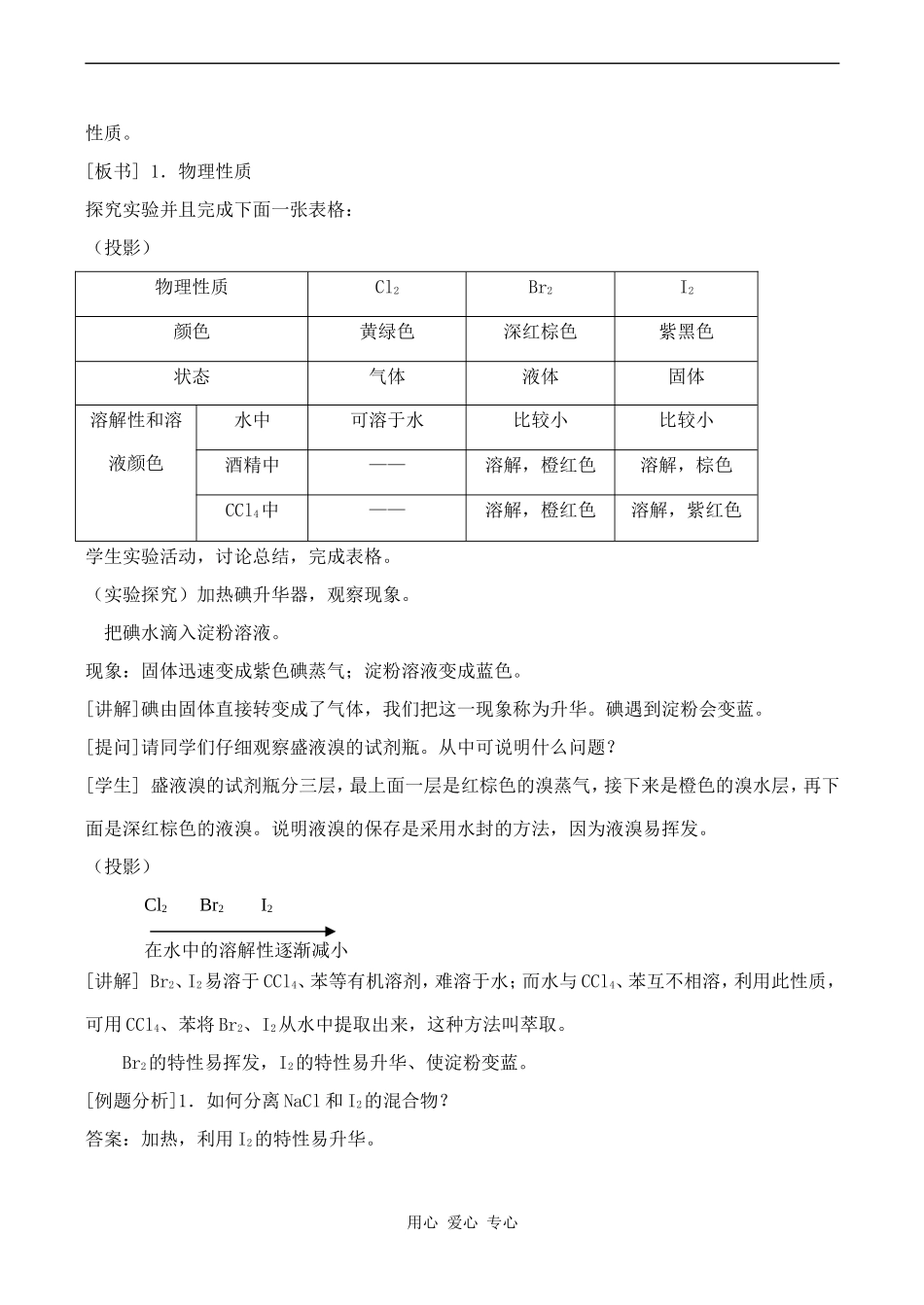
[板书]1.物理性质探究实验并且完成下面一张表格:(投影)物理性质Cl2Br2I2颜色黄绿色深红棕色紫黑色状态气体液体固体溶解性和溶液颜色水中可溶于水比较小比较小酒精中——溶解,橙红色溶解,棕色CCl4中——溶解,橙红色溶解,紫红色学生实验活动,讨论总结,完成表格
(实验探究)加热碘升华器,观察现象
把碘水滴入淀粉溶液