第1课时化学反应中能量变化的本质及转化形式核心素养发展重点学业要求丰富对化学变化的认识角度,认识化学反应中能量变化
了解化学反应中存在能量变化以及化学反应的实质
知道常见的放热反应和吸热反应
了解化学反应中能量变化的实质
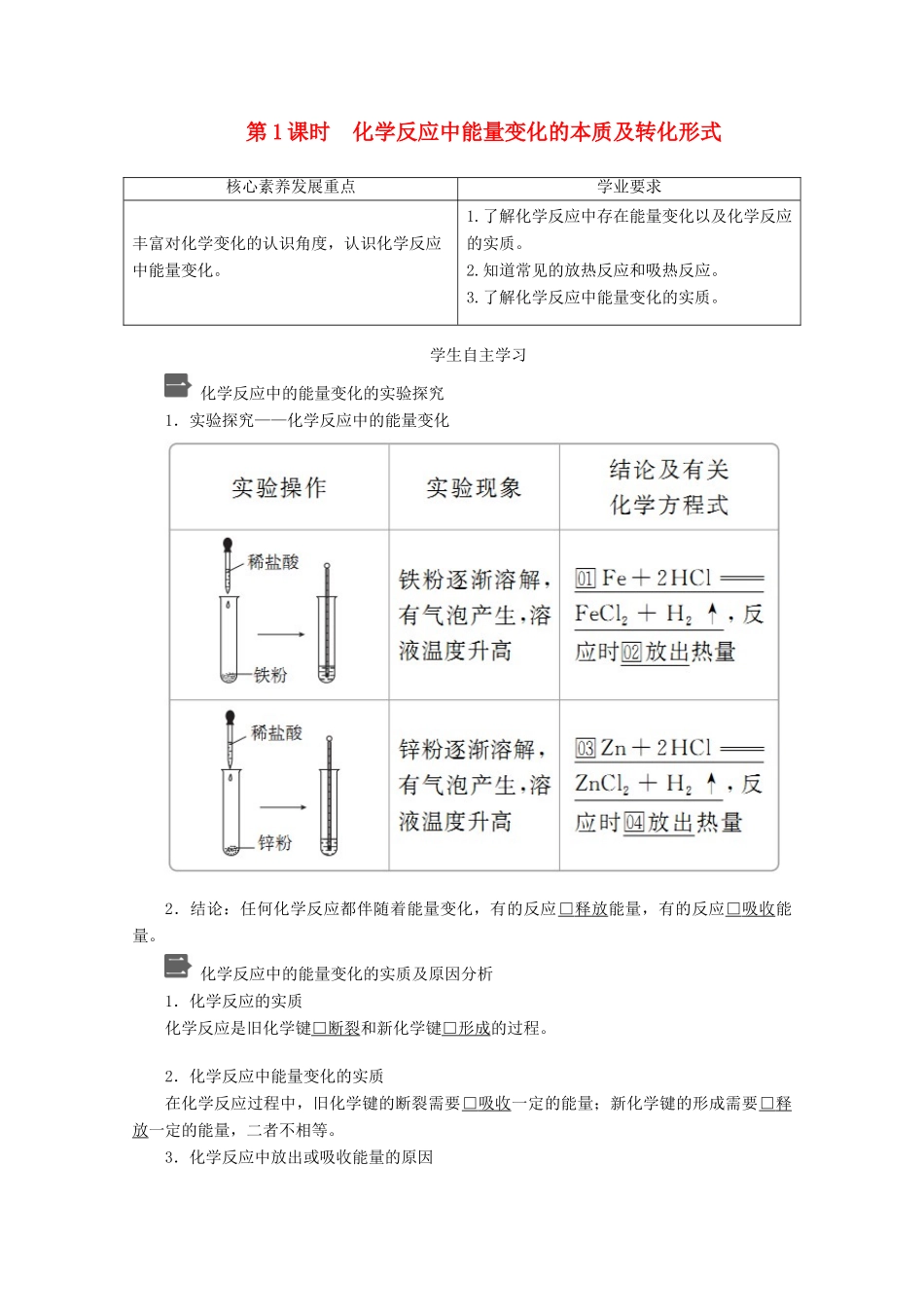
学生自主学习化学反应中的能量变化的实验探究1.实验探究——化学反应中的能量变化2.结论:任何化学反应都伴随着能量变化,有的反应□释放能量,有的反应□吸收能量
化学反应中的能量变化的实质及原因分析1.化学反应的实质化学反应是旧化学键□断裂和新化学键□形成的过程
2.化学反应中能量变化的实质在化学反应过程中,旧化学键的断裂需要□吸收一定的能量;新化学键的形成需要□释放一定的能量,二者不相等
3.化学反应中放出或吸收能量的原因若形成新化学键所释放的总能量大于破坏旧化学键所吸收的总能量,就会有一定的能量以热能、电能或光能等形式□释放出来能量;如果形成新化学键所释放的能量小于破坏旧化学键所吸收的能量,则需要□吸收能量
4.化学反应中能量转化的形式化学反应的过程可以看作是“储存”在物质内部的能量(化学能)转化为□热能、□电能或□光能等释放出来,或是□热能、□电能或□光能等物质外部的能量转化为物质内部的能量(化学能)被“储存”起来的过程
一个确定的化学反应发生时是吸收能量还是释放能量,取决于□反应物的总能量与生成物的总能量的相对大小
课堂互动探究一、化学反应中的能量变化1.放热反应一定容易发生,吸热反应一定难以发生吗
提示:放热反应不一定容易发生,如合成氨的反应;吸热反应不一定难以发生,如Ca(OH)2与NH4Cl的反应
2.需要加热才能发生的反应一定是吸热反应吗
提示:不一定
如木炭的燃烧
1.概念放热反应:放出热量的化学反应;吸热反应:吸收热量的化学反应
2.常见的放热反应(1)所有的燃烧反应,如木炭、H2、CH4等在氧气中的燃烧,H2在Cl2中的燃烧