化学常用计量教学目标知识技能:掌握物质的量及其单位——摩尔、摩尔质量、气体摩尔体积的涵义
掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状态下)之间的相互关系
能力培养:通过基本计算问题的讨论,培养学生的计算思维能力
科学思想:在阿伏加德罗定律的应用上,着重掌握有关比例的数学思想
科学方法:演绎推理法
重点、难点物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系是重点,气体摩尔体积的应用条件是难点
教学过程设计教师活动【引入】今天我们复习化学常用计量
【提问】科学家引入物质的量这个物理量的意义是什么
【再问】谁来说说物质的量是怎样联系宏观和微观的
学生活动回答:把质量、体积等宏观物理量和微观的微粒个数联系起来
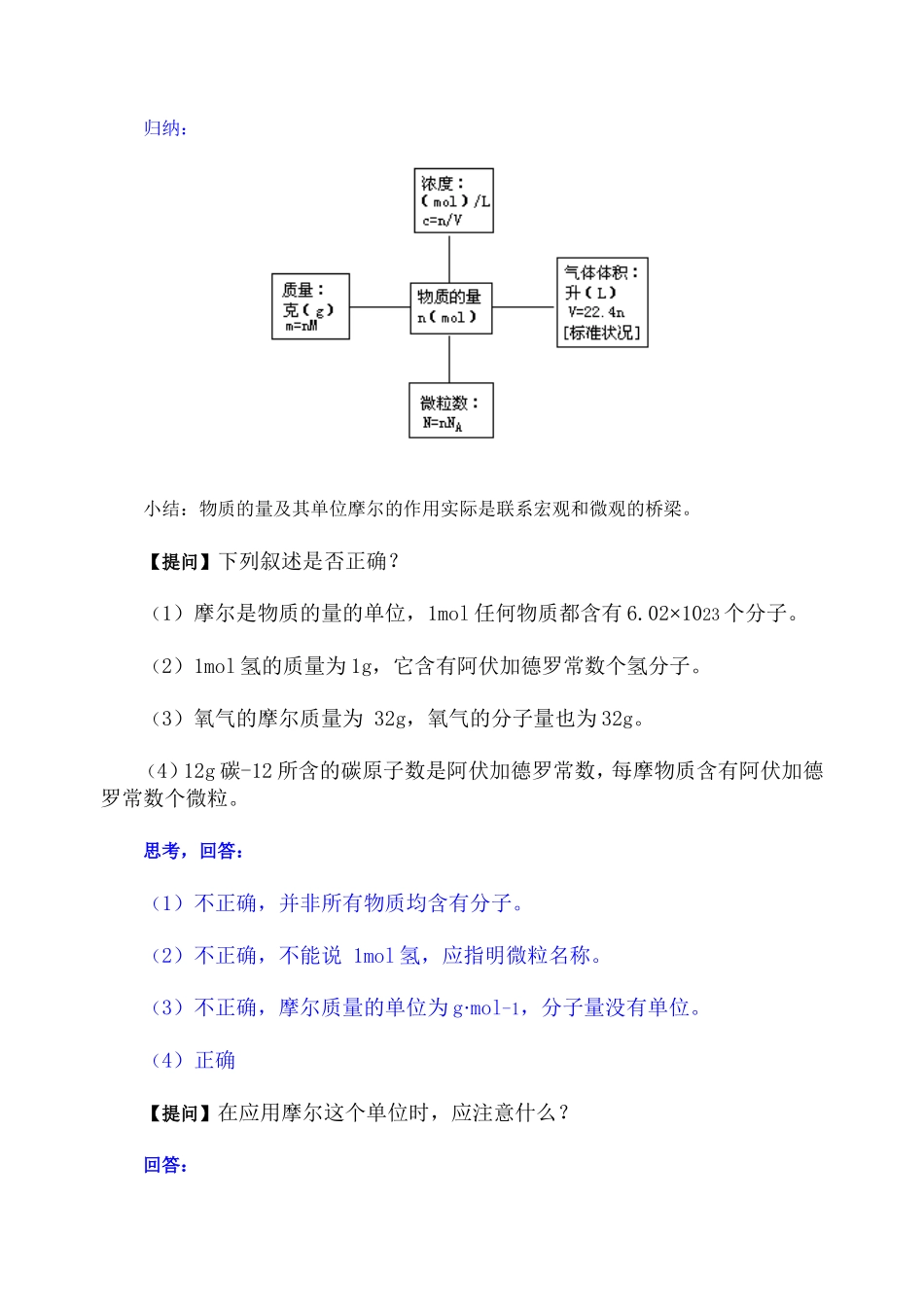
回答:主要通过以物质的量为核心物理量建立的下列关系图,把微粒数、物质质量、气体标准状况下的体积、溶液的物质的量浓度等相互关联起来
归纳:小结:物质的量及其单位摩尔的作用实际是联系宏观和微观的桥梁
【提问】下列叙述是否正确
(1)摩尔是物质的量的单位,1mol任何物质都含有6
02×1023个分子
(2)1mol氢的质量为1g,它含有阿伏加德罗常数个氢分子
(3)氧气的摩尔质量为32g,氧气的分子量也为32g
(4)12g碳-12所含的碳原子数是阿伏加德罗常数,每摩物质含有阿伏加德罗常数个微粒
思考,回答:(1)不正确,并非所有物质均含有分子
(2)不正确,不能说1mol氢,应指明微粒名称
(3)不正确,摩尔质量的单位为g·mol-1,分子量没有单位
(4)正确【提问】在应用摩尔这个单位时,应注意什么
回答:(1)摩尔只能用来表示微粒的集体数目;(2)必须指明微粒的具体名称
【讲解】微粒可以是真实的,如:1mol水分子;也可以是假想的,如:1molNaCl,表示1molNa+和1molCl-的特定组合
【提问】在化学反应中,下列