第一单元走进化学工业课题二人工固氮技术——合成氨第1课时教学目标1
利用所学的化学反应速率和化学平衡理论解释合成氨中的相关问题;2
了解合成氨的主要原理、原料、重要设备、流程和意义
教学重点利用所学的化学反应速率和化学平衡理论解释合成氨中的相关问题
课时安排2课时教学过程新课教学:固氮反应:叫“固氮反应”
主要的固氮反应有:生物固氮、自然固氮、化学固氮和人工模拟生物固氮
1、生物固氮:是一种主要的自然固氮反应,如植物在根瘤菌作用下直接吸收空气中的N2转化为氨等,进一步合成氮白质
2、自然固氮:如闪电产生的巨大电压,其电火花足可以击破氮分子的叁键,促使其与氧气反应生成NO
进而生成NO2和HNO3等
3、化学固氮:合成氨反应;在放电条件下使氮气与氧气反应生成NO等;氮气与镁反应生成氮化镁
4、人工模拟生物固氮:通过化学方法,制备出类似生物“固氮菌”的物质,使空气中的氮气在常温常压下与水及二氧化碳等反应,转化为氨态氮或铵态氮,进而实现人工合成大量的蛋白质等,最终实现工厂化生产蛋白质食品
对比思考:“固硫”反应的概念是:将废气中对空气造成污染的SO2转化为固态含硫化合物
如实验室用NaOH溶液吸收多余的SO2生成Na2SO3,硫酸工业中用氨水吸收SO2生成亚硫酸铵,燃烧煤等产生的SO2用Na2SO3溶液吸收生成NaHSO3,在煤中加入一定比例的CaCO3或CaO使SO2转化为CaSO3
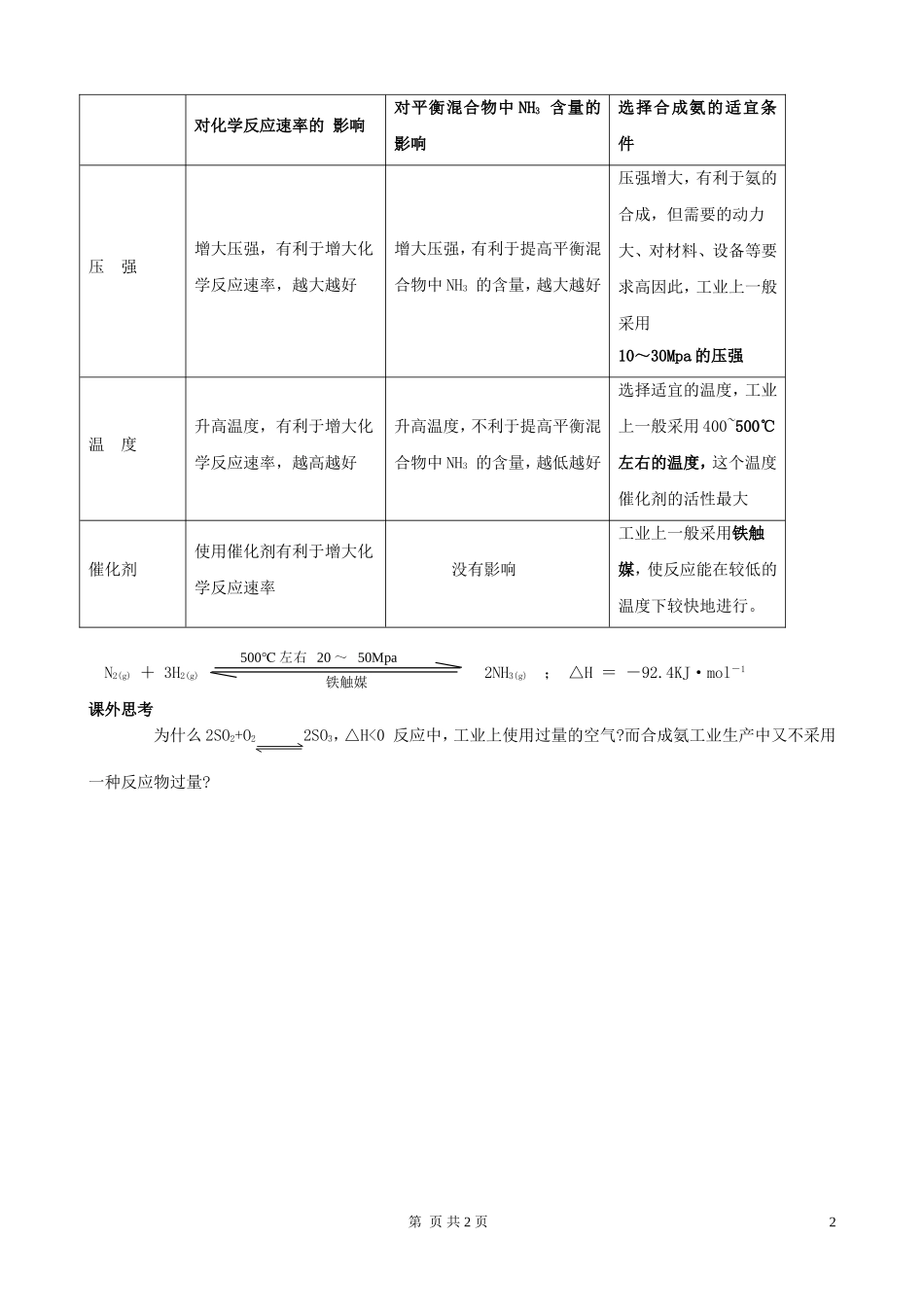
一、应用化学反应速率和化学平衡移动原理,解释合成氨工业的适宜条件的选择理由工业生产中既要考虑尽量增大反应物的转化率,充分利用原料,又要选择较快的反应速率,提高单位时间产率
以上两点是选择反应条件的出发点
当二者发生矛盾时,要结合具体情况辩证分析,找出最佳反应条件
合成氨反应条件的选择原理:选择根据:N2(g)+3H2(g)2NH3(g)△H=-92
4KJ·mol-11、反应特点:①N2极不活泼,