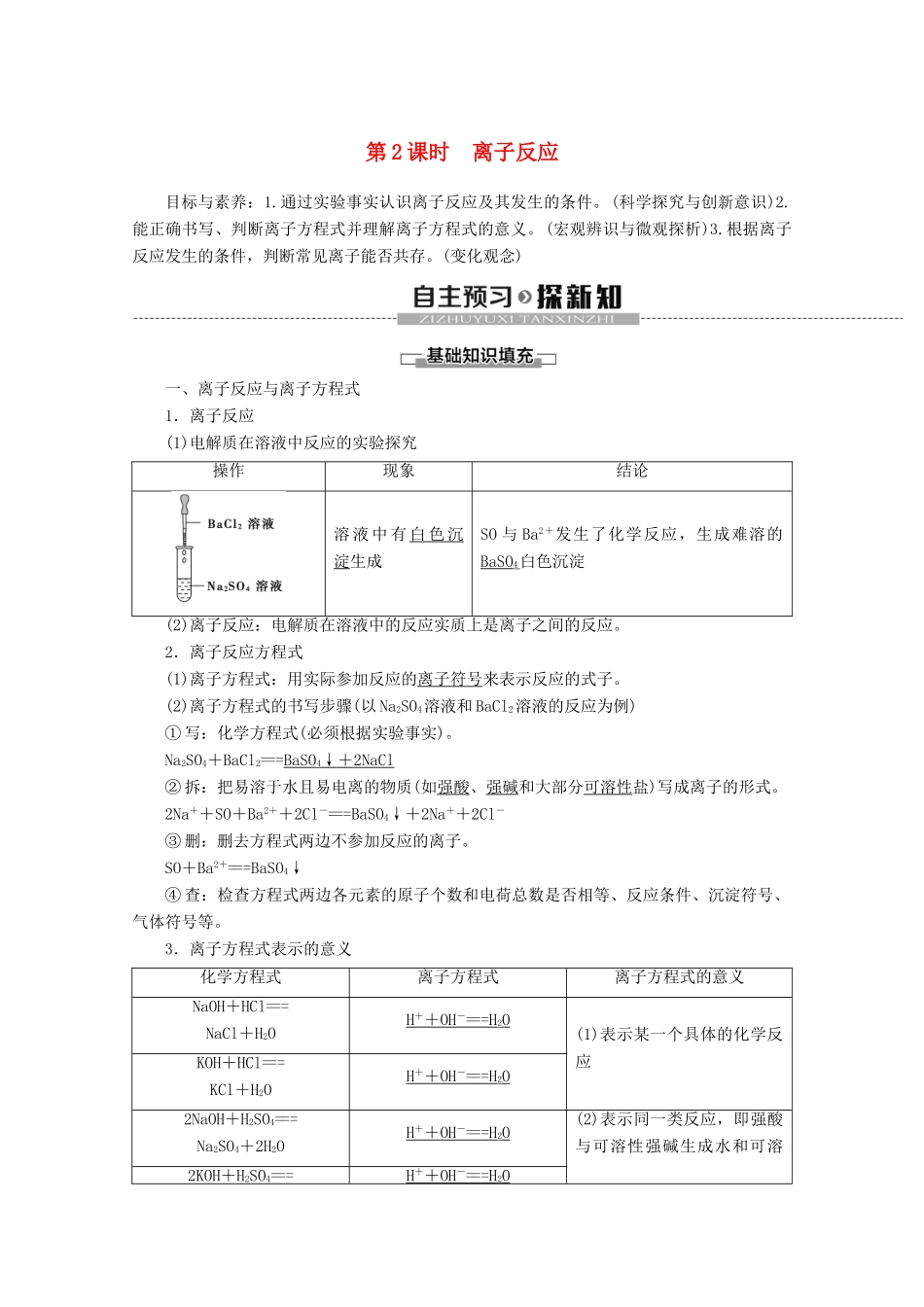
第2课时离子反应目标与素养:1.通过实验事实认识离子反应及其发生的条件。(科学探究与创新意识)2.能正确书写、判断离子方程式并理解离子方程式的意义。(宏观辨识与微观探析)3.根据离子反应发生的条件,判断常见离子能否共存。(变化观念)一、离子反应与离子方程式1.离子反应(1)电解质在溶液中反应的实验探究操作现象结论溶液中有白色沉淀生成SO与Ba2+发生了化学反应,生成难溶的BaSO4白色沉淀(2)离子反应:电解质在溶液中的反应实质上是离子之间的反应。2.离子反应方程式(1)离子方程式:用实际参加反应的离子符号来表示反应的式子。(2)离子方程式的书写步骤(以Na2SO4溶液和BaCl2溶液的反应为例)①写:化学方程式(必须根据实验事实)。Na2SO4+BaCl2===BaSO4↓+2NaCl②拆:把易溶于水且易电离的物质(如强酸、强碱和大部分可溶性盐)写成离子的形式。2Na++SO+Ba2++2Cl-===BaSO4↓+2Na++2Cl-③删:删去方程式两边不参加反应的离子。SO+Ba2+===BaSO4↓④查:检查方程式两边各元素的原子个数和电荷总数是否相等、反应条件、沉淀符号、气体符号等。3.离子方程式表示的意义化学方程式离子方程式离子方程式的意义NaOH+HCl===NaCl+H2OH++OH-===H2O(1)表示某一个具体的化学反应KOH+HCl===KCl+H2OH++OH-===H2O2NaOH+H2SO4===Na2SO4+2H2OH++OH-===H2O(2)表示同一类反应,即强酸与可溶性强碱生成水和可溶2KOH+H2SO4===H++OH-===H2OK2SO4+2H2O性盐的反应二、复分解型离子反应发生的条件1.反应条件2.离子共存(1)几种离子在溶液中能否大量共存,取决于它们之间是否发生反应。(2)在溶液中若离子之间不发生反应,则能大量共存;否则不能大量共存。1.判断正误(正确的打“√”,错误的打“×”)(1)离子反应中参加反应的全是离子()(2)CuSO4溶液与BaCl2溶液反应,实质上是SO和Ba2+生成BaSO4的反应()(3)CaCO3与HCl溶液反应的离子方程式:CO+2H+===H2O+CO2↑()(4)AgNO3溶液与NaCl溶液反应和AgNO3溶液与盐酸反应都可用Ag++Cl-===AgCl↓来表示()[答案](1)×(2)√(3)×(4)√2.下列化学方程式中,不可以用H++OH-===H2O表示的是()A.2NaOH+H2SO4===Na2SO4+2H2OB.Ba(OH)2+2HCl===BaCl2+2H2OC.Cu(OH)2+2HNO3===Cu(NO3)2+2H2OD.KOH+HCl===KCl+H2OC[H++OH-===H2O代表强酸和可溶性强碱反应生成可溶性盐和H2O的反应,A、B、D均符合;而C项中Cu(OH)2为难溶性弱碱,应写成Cu(OH)2形式。]3.请写出下列复分解反应的离子方程式:(1)碳酸钙和盐酸:___________________________________。(2)氧化镁和稀硫酸:_________________________________。[答案](1)CaCO3+2H+===Ca2++CO2↑+H2O(2)MgO+2H+===Mg2++H2O离子方程式的书写与正误判断1.书写离子方程式的注意事项(1)微溶物处理方式有三种情况。①出现在生成物中写化学式。②反应物处于溶液状态写离子符号。③反应物处于浊液或固态时写化学式。(2)溶液中铵盐与碱反应加热放出NH3,不加热写NH3·H2O。(3)浓盐酸、浓硝酸在离子方程式中写离子符号,浓硫酸保留化学式。(4)HCO、HS-、HSO等弱酸的酸式酸根离子不能拆开写。(5)单质、氧化物保留化学式。2.离子方程式正误判断(1)看是否符合客观事实。(2)看拆分是否正确。(3)看是否符合原子守恒和电荷守恒。(4)看是否漏写离子反应。1.下列反应的离子方程式书写正确的是()A.稀硫酸滴在铜片上:Cu+2H+===Cu2++H2↑B.稀硫酸与Ba(OH)2溶液混合:SO+Ba2+===BaSO4↓C.稀硝酸滴在大理石上:CaCO3+2H+===Ca2++H2CO3D.氧化铁与稀盐酸混合:Fe2O3+6H+===2Fe3++3H2OD[某个离子方程式书写是否正确应遵循客观事实。A反应不能发生,因为Cu的金属活动性弱,不能置换出氢气;B忽视了H+、OH-均参加反应;C反应生成的H2CO3不稳定,应分解成CO2和H2O。]2.下列反应可以用同一离子方程式表示的是()A.HCl溶液+Na2CO3溶液,HCl溶液+NaHCO3溶液B.NaOH溶液+HCl溶液,Ba(OH)2溶液+H2SO4溶液C.BaCl2溶液+H2SO4溶液,Ba(OH)2溶液+Na2SO4溶液D.CaCO3+HCl溶液,Na2CO3溶液+H2SO4溶液C[A项,第1组反应为2H++CO===CO2↑+H2O,第2组反应为H++HCO===C...