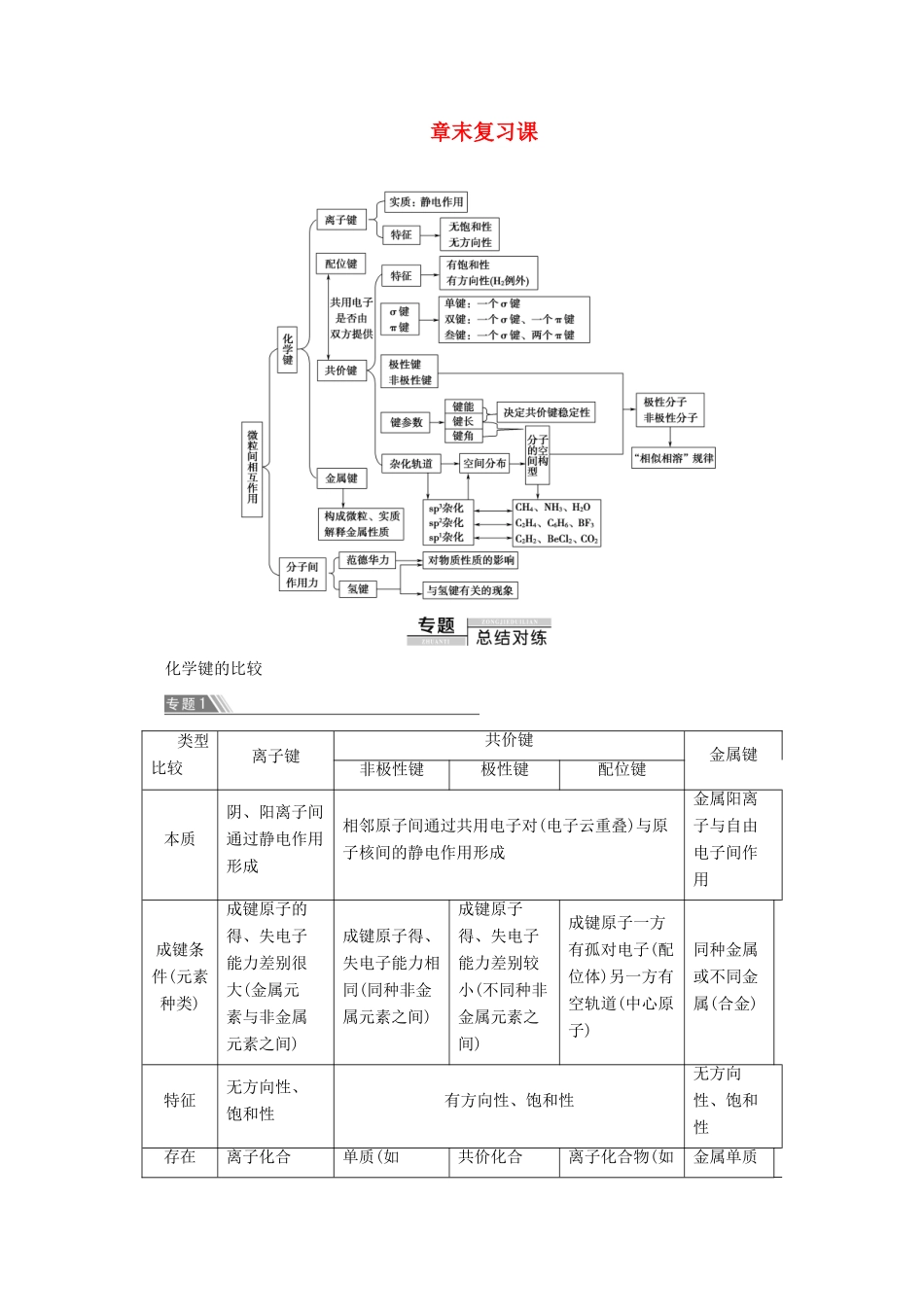
章末复习课化学键的比较类型比较离子键共价键金属键非极性键极性键配位键本质阴、阳离子间通过静电作用形成相邻原子间通过共用电子对(电子云重叠)与原子核间的静电作用形成金属阳离子与自由电子间作用成键条件(元素种类)成键原子的得、失电子能力差别很大(金属元素与非金属元素之间)成键原子得、失电子能力相同(同种非金属元素之间)成键原子得、失电子能力差别较小(不同种非金属元素之间)成键原子一方有孤对电子(配位体)另一方有空轨道(中心原子)同种金属或不同金属(合金)特征无方向性、饱和性有方向性、饱和性无方向性、饱和性存在离子化合单质(如共价化合离子化合物(如金属单质物(离子晶体)H2),共价化合物(如H2O2),离子化合物(如Na2O2)物(如HCl),离子化合物(如NaOH)NH4Cl)(金属晶体)影响强弱因素一般阴、阳离子电荷越多,半径越小,离子键越强成键原子电负性差值越大,键的极性越强;键能越大,键长越短,共价键越牢固--金属阳离子半径越小,价电子越多,金属键越强1.(2019·全国Ⅰ卷)一些氧化物的熔点如下表所示:氧化物Li2OMgOP4O6SO2熔点/℃1570280023.8-75.5解释表中氧化物之间熔点差异的原因_______________________________________________________________________________________________________________________________________________________________________________________。[答案]离子晶体的熔点大于分子晶体,Li2O、MgO为离子晶体,P4O6、SO2为分子晶体;晶格能MgO>Li2O,分子间作用力(分子量)P4O6>SO2杂化轨道类型的判断方法1.根据分子的空间构型判断根据杂化轨道理论,中心原子轨道采取一定的杂化方式后,其空间构型和键角如下:杂化轨道类型杂化轨道空间构型键角sp1直线形180°sp2平面三角形120°sp3正四面体形109.5°由于常考的分子或离子构型多为直线形、平面三角形、V形、正四面体形、三角锥形等,故可按图索骥、简单判断。分子或离子的空间构型常见分子或离子中心原子杂化轨道类型直线形CO2、CS2、BeCl2、HC≡CH、HC≡N等sp1平面三角形BF3、BCl3、SO3、NO、CO等sp2正四面体形CH4、CCl4、SiF4、ClO、SO、PO、SiO等sp3三角锥形NH3、NCl3、PH3、SO、ClOsp3微点拨:常见的C2H4、C6H6为平面形分子,键角为120°,可推断其碳原子的杂化轨道类型为sp2。2.根据价电子对互斥理论判断根据价电子对互斥理论能够比较容易而准确地判断ABm型共价分子或离子的空间构型和中心原子杂化轨道类型,其关系如下表。中心原子价电子对数杂化轨道空间构型中心原子杂化轨道类型2直线形sp13平面三角形sp24正四面体形sp3运用该理论的关键是准确计算中心原子的价电子对数,其计算方法如下:注意:对于阳离子,a=中心原子价电子数-离子电荷数;对于阴离子,a=中心原子价电子数+|离子电荷数|。3.应用等电子原理判断等电子体具有相同的结构特征,一般来说,等电子体的中心原子的杂化类型相同。对于结构模糊或复杂的分子、离子,可将其转化成熟悉的等电子体,然后进行判断。常见的等电子体往往是同族不同元素或同周期相近元素构成的微粒。4.根据共价键类型判断从杂化轨道理论可知,原子之间成键时,未杂化轨道形成π键,杂化轨道形成σ键。对于能够明确结构式的分子、离子,可直接用下式判断其中心原子的杂化轨道类型:杂化轨道数n=中心原子的σ键数+中心原子的孤电子对数(双键、叁键中只有一个σ键,其余均为π键)。(1)SiF4分子中硅原子杂化轨道类型分析:基态硅原子有4个价电子,与4个氟原子恰好形成4个σ键,无未成键电子,n=4,则SiF4分子中硅原子采用sp3杂化。(2)基态碳原子有4个价电子,在HCHO分子中,碳原子与2个氢原子形成2个σ键,与氧原子形成C===O键,C===O键中有1个σ键、1个π键,碳原子无未成键电子,n=3,则HCHO分子中碳原子采用sp2杂化。(3)三聚氰胺(结构简式如图所示)中有两种环境的氮原子,环外氮原子分别形成3个σ键,用去基态氮原子5个价电子中的3个,余下1对孤对电子,n=4,则环外氮原子采用sp3杂化;环内氮原子分别形成2个σ键、1个π键,用去基态氮原子5个价电子中的3个,余下1对孤对电子,n=3,则环内氮原子采用sp2杂化。5.应用取代法...