4电解质溶液在通电情况下的变化(共两课时)第2课时电解氯化铜溶液[设计思想]本课时主要包含三个部分:运用电解原理确定直流电源的正负极、氯化铜溶液电解以及阳离子得电子能力大小、电解池与原电池异同比较
其中,运用电解原理确定直流电源的正负极,旨在促进学生从不同的角度全面认识电解原理及电解池
氯化铜溶液电解在于完善对于电解过程中阳离子得电子能力大小的认识,再次感受电解池的实质即氧化还原反应的应用
而对电解池与原电池异同比较则是将分散学习的电化学知识进行归纳整理,以突出学科知识的逻辑体系,促进相关知识结构化
本课教学设计与第一课时保持一致——着重强化应用氧化还原理论分析实验现象的微观本质,让学生以主动的姿态进行科学论证,同时提高观察能力及对比、分析的思维能力
同时,在完成学习任务后又点明学习电解池的科学方法——控制变量法,不仅为学生寻找新的变量继续研究电解池指出了方向,也为学生运用科学方法进行研究提供了范例
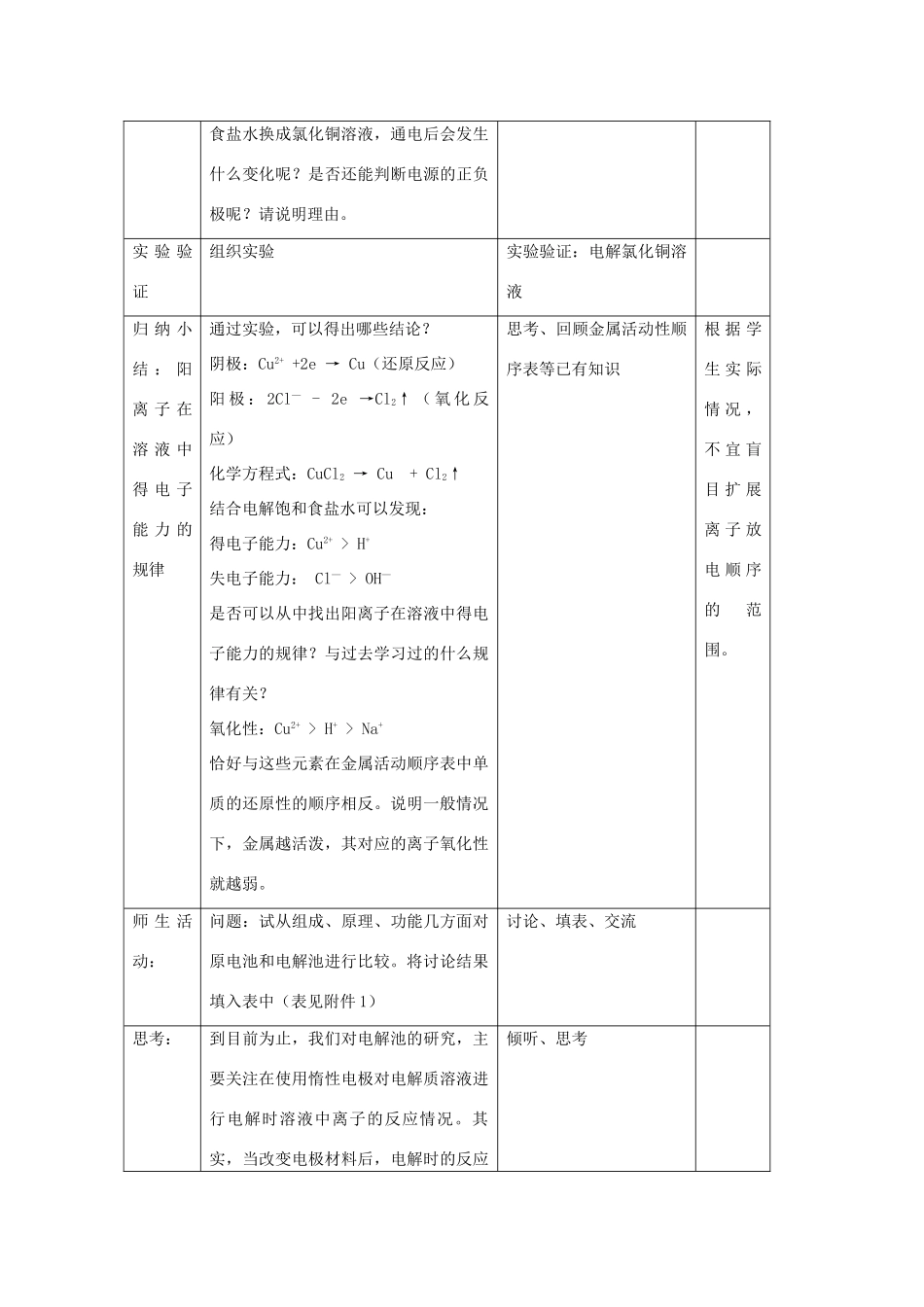
一、教学目标1、知识与技能(1)氯化铜溶液的电解(B)(2)电解池的构造与工作原理(B)2、过程与方法通过电解氯化铜溶液的实验,运用观察、分析、抽象、概括的思维方法探究电解质溶液中阳离子的放电顺序
3、情感态度与价值观从对电解饱和食盐水、氯化铜溶液实验现象的分析中,感悟宏观表象和微观本质的关系
二、教学重点和难点1、重点电解氯化铜溶液、溶液中阳离子的放电顺序2、难点电解池与原电池的异同三、教学用品电解氯化铜溶液的电解装置
四、教学流程1、流程图2、流程说明引入:用逆向思维性问题引入,通过学生活动促进对电解原理的深入理解
学生活动I:运用已知电解原理分析问题,问题焦点在阴极产物
学生实验I:验证提出的假设,体验研究过程
小结I:通过前期的预测,结合实验现象运用氧化还原反应原理进行分析,得出Cu2+、H+、Na+三种离子的得电子能力大小顺序,并可结合金属之间的置换反应归纳出阳离