7.2研究电解质在溶液中的化学反应(共两课时)第1课时离子反应[设计思想]本节是在初中复分解反应发生的条件以及高中电解质与非电解质、强电解质与弱电解质、电离等基础上展开
教学时,从离子反应的本质出发,通过学生实验,让学生展开讨论,引导学生运用电解质在水中发生电离,电离方程式等知识进行分析,并联系复分解反应趋于完成的条件,研究在什么条件下可使反应物的某些离子浓度减小,得出:电解质在溶液里发生反应的实质是离子间的反应,理解离子反应总是向离子浓度降低的方向进行的规律
通过简单离子方程式的书写,认识用实际参加反应的离子来表示化学反应,即离子方程式以及离子方程式与化学方程式的区别与联系,理解离子方程式的意义
一.教学目标1.知识与技能(1)离子反应发生的条件、本质及规律(B)(2)离子方程式意义(B)2.过程与方法通过盐酸与氢氧化钠的中和反应、碳酸根离子检验等实验,综合运用物质结构知识、电解质溶液电离等知识,经历分析问题、解决问题,逐步形成分析、比较、归纳的科学研究的方法
3.情感态度与价值观通过盐酸与氢氧化钠的中和反应、碳酸根离子检验等实验现象的观察、记录、交流,体验化学的乐趣,感悟科学实验时认真、严谨、求真的重要意义
二.教学重点和难点离子反应本质和理解离子反应总是向离子浓度降低的方向进行的规律
三.教学用品药品:HCl、NaOH、NaCl、BaCl2、AgNO3、CuSO4、Na2CO3、K2CO3、(NH4)2CO3溶液、酚酞溶液
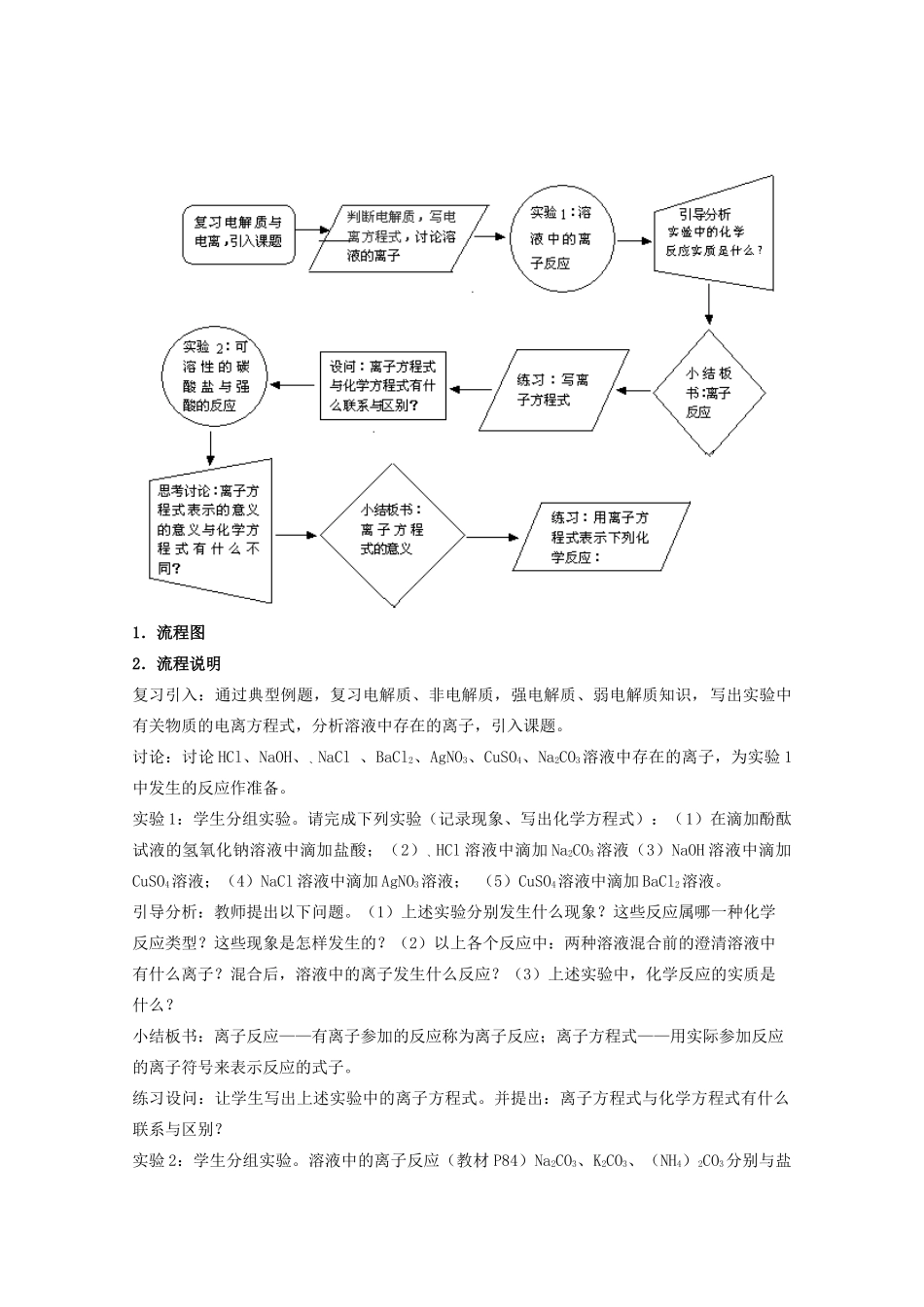
仪器:试管、滴管四.教学流程1.流程图2.流程说明复习引入:通过典型例题,复习电解质、非电解质,强电解质、弱电解质知识,写出实验中有关物质的电离方程式,分析溶液中存在的离子,引入课题
讨论:讨论HCl、NaOH、、NaCl、BaCl2、AgNO3、CuSO4、Na2CO3溶液中存在的离子,为实验1中发生的反应作准备
实验1:学生分组实验