第三节电解池[实验引入][师]请大家仔细观察下面两个实验的组成装置(如图),并分析实验产生的现象
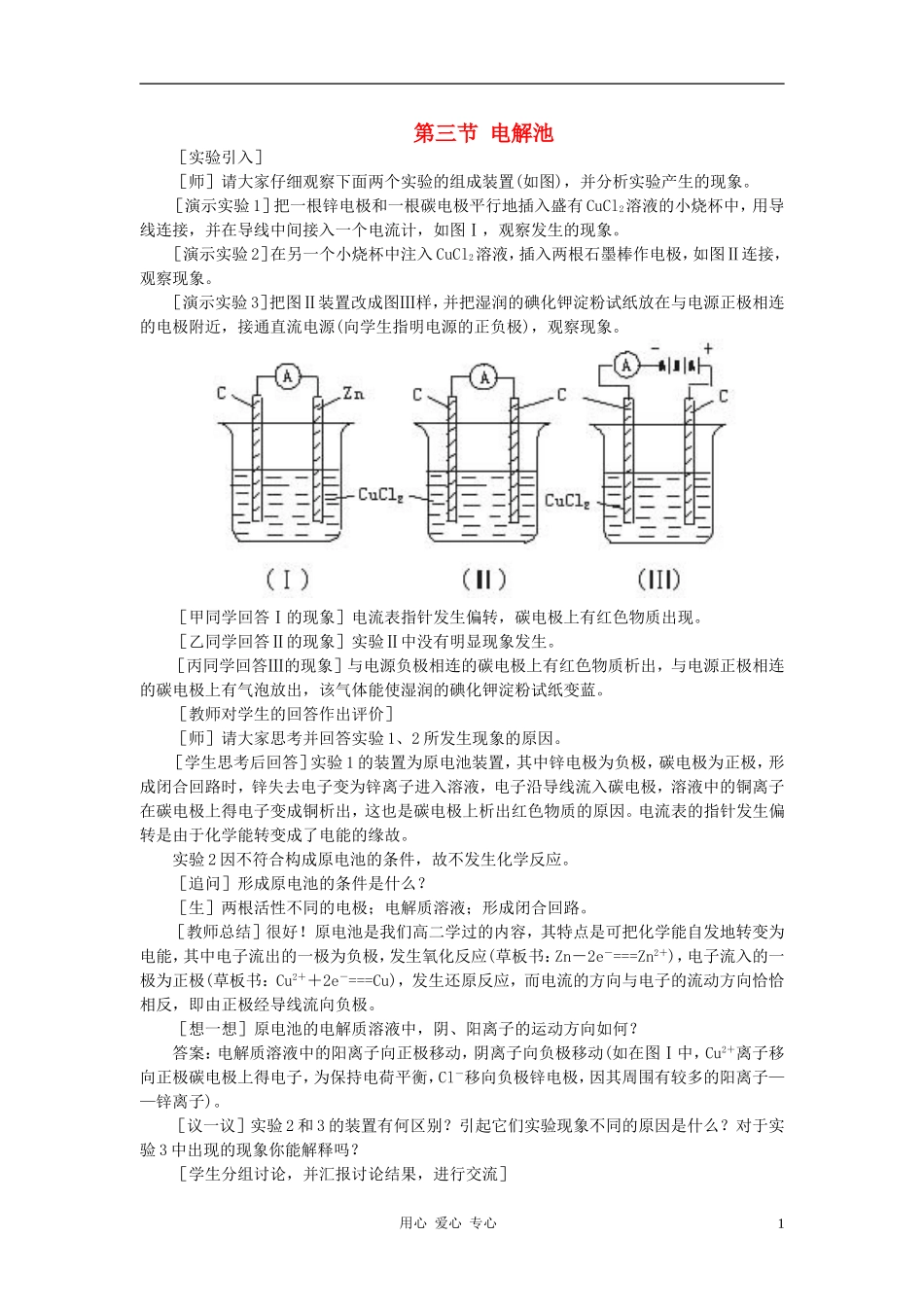
[演示实验1]把一根锌电极和一根碳电极平行地插入盛有CuCl2溶液的小烧杯中,用导线连接,并在导线中间接入一个电流计,如图Ⅰ,观察发生的现象
[演示实验2]在另一个小烧杯中注入CuCl2溶液,插入两根石墨棒作电极,如图Ⅱ连接,观察现象
[演示实验3]把图Ⅱ装置改成图Ⅲ样,并把湿润的碘化钾淀粉试纸放在与电源正极相连的电极附近,接通直流电源(向学生指明电源的正负极),观察现象
[甲同学回答Ⅰ的现象]电流表指针发生偏转,碳电极上有红色物质出现
[乙同学回答Ⅱ的现象]实验Ⅱ中没有明显现象发生
[丙同学回答Ⅲ的现象]与电源负极相连的碳电极上有红色物质析出,与电源正极相连的碳电极上有气泡放出,该气体能使湿润的碘化钾淀粉试纸变蓝
[教师对学生的回答作出评价][师]请大家思考并回答实验1、2所发生现象的原因
[学生思考后回答]实验1的装置为原电池装置,其中锌电极为负极,碳电极为正极,形成闭合回路时,锌失去电子变为锌离子进入溶液,电子沿导线流入碳电极,溶液中的铜离子在碳电极上得电子变成铜析出,这也是碳电极上析出红色物质的原因
电流表的指针发生偏转是由于化学能转变成了电能的缘故
实验2因不符合构成原电池的条件,故不发生化学反应
[追问]形成原电池的条件是什么
[生]两根活性不同的电极;电解质溶液;形成闭合回路
[教师总结]很好
原电池是我们高二学过的内容,其特点是可把化学能自发地转变为电能,其中电子流出的一极为负极,发生氧化反应(草板书:Zn-2e-===Zn2+),电子流入的一极为正极(草板书:Cu2++2e-===Cu),发生还原反应,而电流的方向与电子的流动方向恰恰相反,即由正极经导线流向负极
[想一想]原电池的电解质溶液中,阴、阳离子的运动方向如何
答案:电解质溶液中的阳离子向正极移动,阴