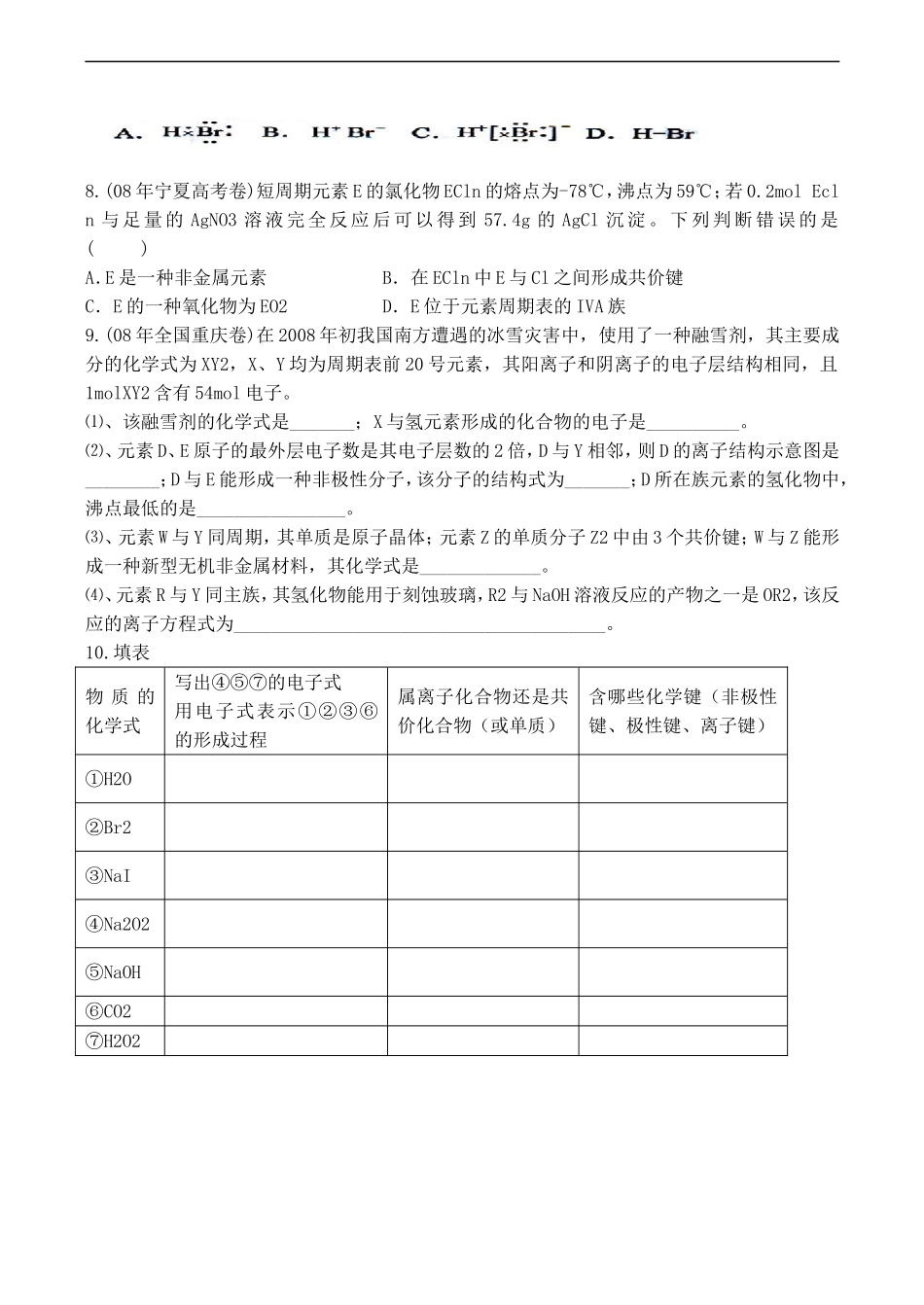
第三节化学键(第二课时)【学习目标】(1)、对共价键和共价化合物概念的理解;从化学键的角度理解化学反应的本质
(2)、极性键和非极性键的判断和被破坏的化学键类型的判断
【基础知识】一、共价键(1)共价键的成因:非金属元素的原子容易得电子,当非金属元素的原子间形成化学键时一般不发生电子的,通常通过形成化学键
(2)共价键的概念:叫做共价键
(3)共价键的分类:①非极性键:由的原子问形成的共价键,共用电子对,成键的原子因此不显电性,这样的共价键叫做非极性共价键,简称非极性键
②极性键:在化合物分子中,由不同种原子形成共价键时,因为原子吸引电子的能力不同,共用电子对将偏向吸引电子能力强的一方,所以吸引电子能力强的原子一方显,吸引电子能力弱的原子一方显
像这样共用电子对的共价键叫做极性共价键,简称极性键
二、结构式在化学上,用表示的图式叫做结构式
三、共价化合物以的化合物叫做共价化合物
如H20、C02、Si02:、CH3CH20H等都是共价化合物
四、化学键(1)定义:使相结合或相结合的通称为化学键
(3)化学反应的实质:物质发生化学变化的过程就是旧化学键与新化学键的过程
五、分子间作用力与氢键(1)分子间作用力①概念:分子之间存在着一种把分子叫做分子间作用力,又称
②强弱:分子间作用力比化学键,它主要影响物质的、、等物理性质,化学键属分子内作用力,主要影响物质的化学性质
③规律:一般来说,对于组成和结构相似的物质,越大,分子间作用力,物质的熔点、沸点也越
④存在:分子间作用力只存在于由分子组成的共价化合物、共价单质和稀有气体的分子之间
在离子化合物、金属单质、金刚石、晶体硅、二氧化硅等物质中只有化学键,没有分子间作用力
(2)氢键①概念:像、、这样分子之间存在着一种比的相互作用,使它们只能在较高的温度下才能汽化,这种相互作用叫做氢键
②对物质性质的影响:分子间形成的氢键会使物质