高考化学第三节氧化还原反应第2课时教案高考化学第三节氧化还原反应第2课时教案三维目标知识与技能1
应用电子转移的观点进一步理解氧化还原反应
应用电子转移的观点判断、分析氧化还原反应,并能举例说明化学反应中元素化合价的变化与电子转移的关系
认识氧化还原反应中各有关物质的相互关系
过程与方法1
经过对氧化还原反应探究的过程,理解科学探究的意义,学习科学探究的基本方法,提高科学探究能力
能够发现和提出有探究价值的化学问题,敢于质疑,勤于思索,逐步形成独立思考的能力,善于与人合作,具有团队精神
情感、态度与价值观1
发展学习化学的兴趣,乐于探究氧化还原反应的奥秘,体验科学探究的艰辛和喜悦,感受化学世界的奇妙与和谐
树立辩证唯物主义的世界观,养成求真务实、勇于创新、积极实践的科学态度
氧化还原反应的实质2
氧化剂、还原剂教学难点1
氧化还原反应的实质2
培养探究能力、思维能力、归纳能力教具准备多媒体课件、投影仪教学过程导入新课【投影】1
什么叫氧化反应
什么叫还原反应
生:氧化反应:元素化合价升高的反应
还原反应:元素化合价降低的反应
请判断下表中的反应是不是氧化还原反应,分析反应前后元素化合价的变化
氧化还原反应方程式编号得氧、失氧化合价变化是否属于氧化还原反应CuO+H2△Cu+H2O(1)Fe2O3+3CO高温2Fe+3CO2(2)2Na+Cl2点燃2NaCl(3)H2+Cl2点燃2HCl(4)生:(1)和(2)是物质得氧、失氧的化学反应,反应前后元素化合价发生了变化,是氧化还用心爱心专心1原反应
(3)和(4)反应中没有氧的得失,但反应前后元素化合价发生了变化,也是氧化还原反应
师:(3)和(4)也是氧化还原反应,那么,反应前后元素化合价的变化与电子得失又是什么关系
这就要从微观的角度上认识氧化还原反应
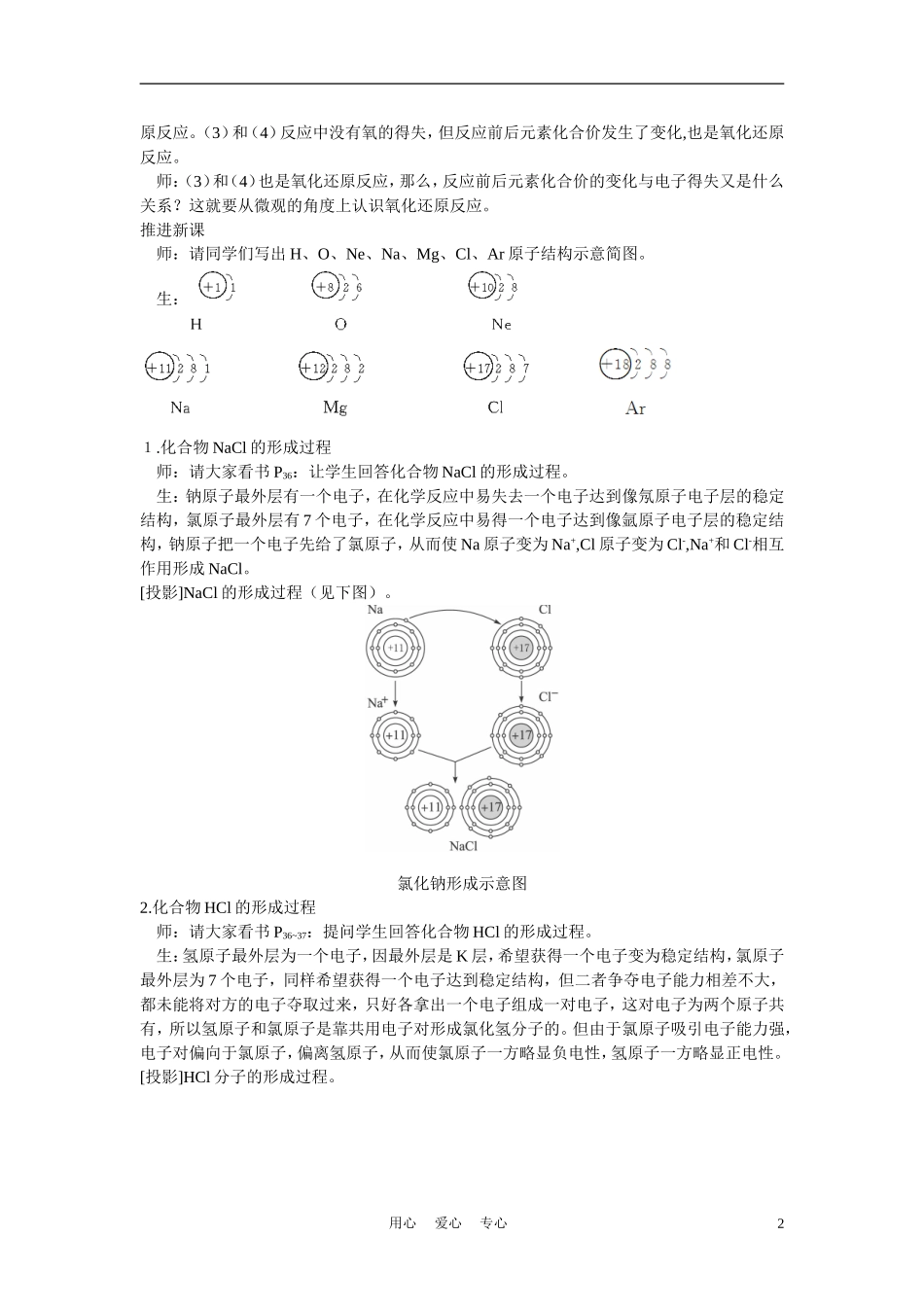
推进新课师:请同学们写出H、O、Ne、N