高一化学第二节元素周期律(第二课时)教学目标:1.了解元素金属性周期性变化
2.认识元素性质的周期性变化是元素原子核外电子排布周期性变化的必然结果,从而理解元素周期律的实质
3.通过本课时学习,使学生对以前学过的知识进行概括、综合,实现由感性认识上升到理性认识;同时,也会以此理论来指导后续学习
4.通过自学、思考、对比、实验等方法培养观察、分析、推理、归纳等探究式学习能力
教学重点、难点:同一周期元素金属性、非金属性变化的规律;元素周期律的涵义和实质;
教学方法:归纳法、诱导探究法、练习法、实验启发等教学过程:[复习填下下列1~18号元素的元素符号及核外电子排步(用原子结构式意图)原子序数12元素名称氢氦元素符号核外电子排步主要化合价+10原子序数345678910元素名称锂铍硼碳氮氧氟氖元素符号核外电子排步最高正化合价和最低负化和价+1+2+3+4-4+5-3-2-10原子序数1112131415161718元素名称钠镁铝硅磷硫氯氩元素符号核外电子排步最高正化合价和最低负化和价+1+2+3+4-4+5-3+6-2+7-10[思考·探究]随原子序数的递增,元素核外电子层排步及元素化合价呈现什么规律性变化
(学生发言)[引入]从面讨论中,我们认识到随着原子序数的递增,元素原子的电子排布,原子半径和化合价均呈周期性的变化
元素的化学性质是由原子结构决定的,那么元素的金属性与非金属性也将随着元素原子序数的递增而呈现周期性的变化
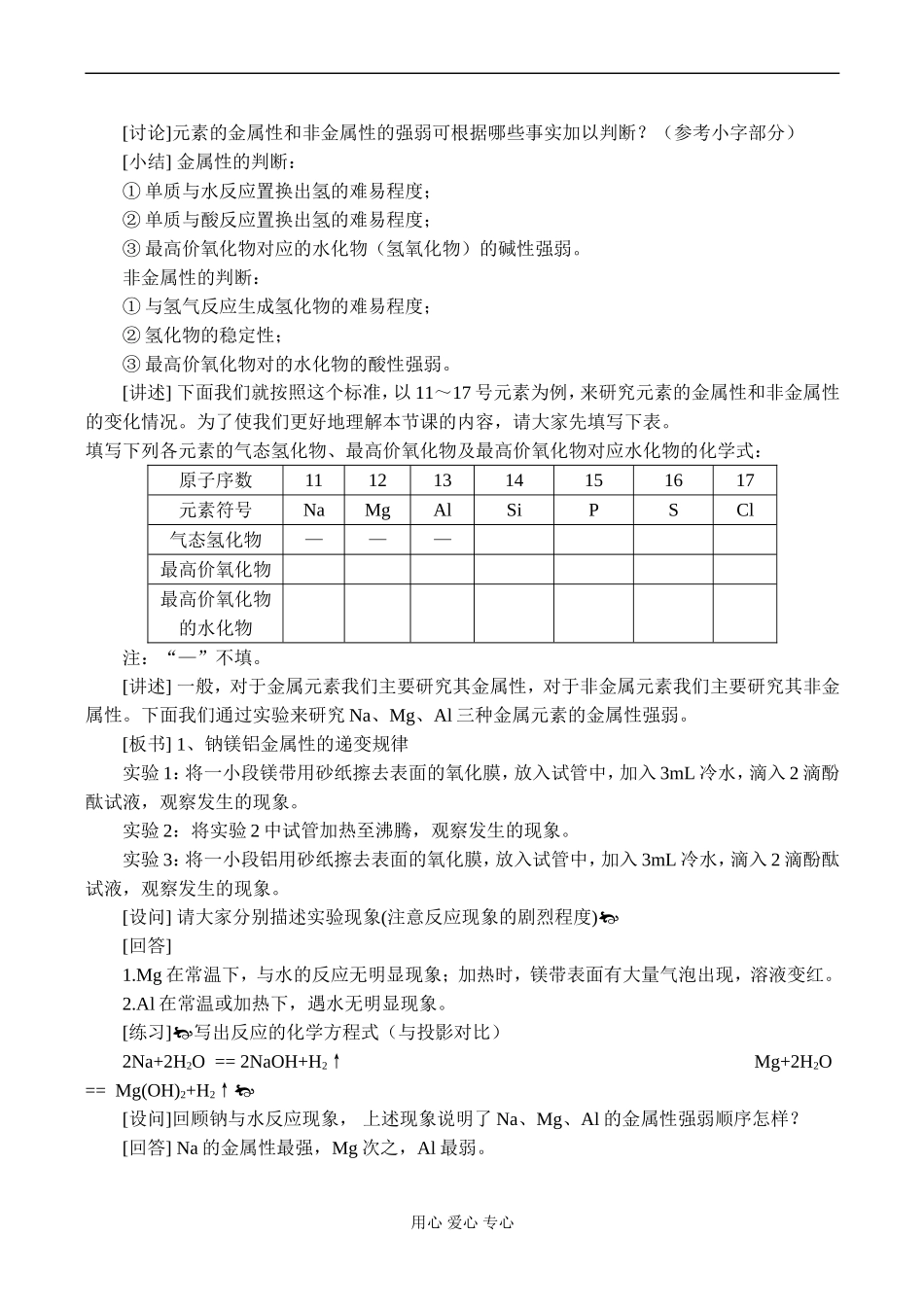
[板书]二、元素周期律用心爱心专心[讨论]元素的金属性和非金属性的强弱可根据哪些事实加以判断
(参考小字部分)[小结]金属性的判断:①单质与水反应置换出氢的难易程度;②单质与酸反应置换出氢的难易程度;③最高价氧化物对应的水化物(氢氧化物)的碱性强弱
非金属性的判断:①与氢气反应生成氢化物的难易程度;②氢化物的稳定性;③最高价氧化物对的水化物的酸性强弱