高一化学《铁和铁的化合物》第二课时教案[教学目标]1.知识目标(1)初步理解、掌握铁化合物和亚铁化合物之间相互转变的规律及其条件;巩固、加深对氧化还原反应的认识
(2)铁的氢氧化物的性质与比较
(3)铁“三角”(即Fe、Fe2+、Fe3+之间的转化)
铁离子的检验
2.能力和方法目标(1)通过本节内容中的演示实验操作,指导学生用简单的实验探究化学性质、化学事实的能力
(2)通过铁的氧化物的比较、铁的氢氧化物的比较、亚铁离子和铁离子的比较,提高归纳比较能力
明确“比较”是学习和研究化学的一种基本方法
3.情感和价值观目标(1)通过对我国钢铁工业的发展,其中钢产量由1949年居世界第26位跃居1996年的世界首位的事实,对学生进行爱国主义教育
(2)通过用众多的化学实验学习和研究铁及化合物性质,培养“事实胜于雄辩”,用事实说话的态度,教育学生化学是一门以实验为基础的科学,培养他们实事求是、脚踏实地的科学精神
[重点与难点]本课时的重点和难点是“铁三角”
[教学过程]复习回顾:(1)镁、铝和铁的性质有哪些异同点
(2)氯化镁、氯化铝、氯化铁的性质有哪些异同点
(3)铁、镁和铝的冶炼方法有什么不同之处
(4)铁有哪些常见的氧化物
它们分别跟盐酸反应的化学方程式
四、铁的氢氧化物思考:FeCl3和FeCl2溶液中分别滴加NaOH溶液有什么现象
请同学们写出相应的化学方程式
演示实验1:在试管中注入少量FeCl3溶液,再逐滴滴入NaOH溶液
观察发生的现象
现象:溶液里立即生成了红褐色的沉淀
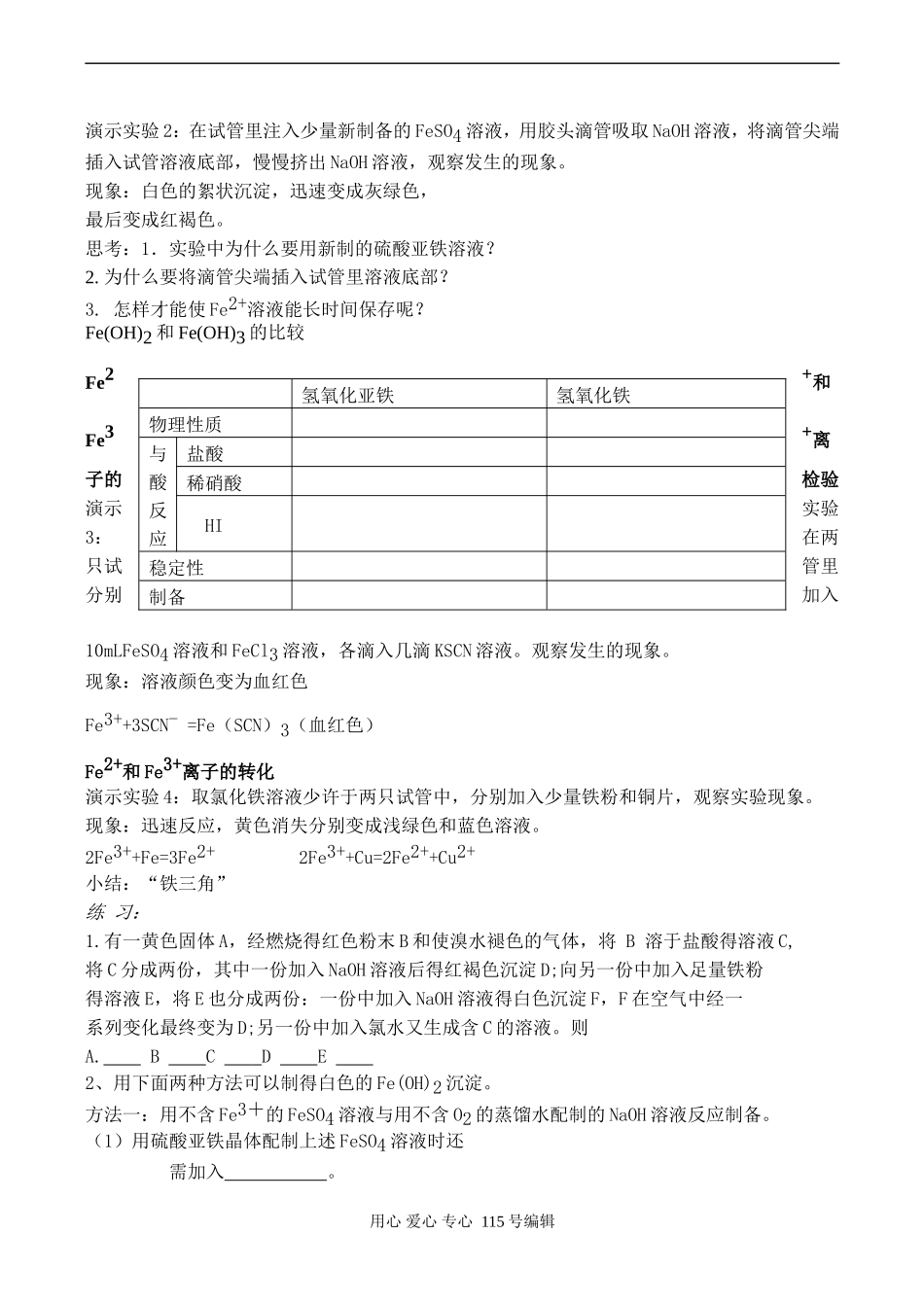
Fe3++3OH-===Fe(OH)3↓(红褐色)用心爱心专心115号编辑演示实验2:在试管里注入少量新制备的FeSO4溶液,用胶头滴管吸取NaOH溶液,将滴管尖端插入试管溶液底部,慢慢挤出NaOH溶液,观察发生的现象
现象:白色的絮状沉淀,迅速变成灰绿色,最后变成红褐色
思考:1.实验中为什么要