第2节物质的微观粒子模型课题第2节物质的微观粒子模型课时类型新课课时安排2教学目标【知识与技能目标】1
知道物质是由分子构成,分子是由原子构成,物质也可由原子直接构成;2
了解原子和分子的主要区别在于化学反应里是否可“分”
【过程与方法目标】通过读图,将学生的认识从宏观的物质引向微观结构中的粒子,提高学生的认知能力
【情感、态度与价值观目标】介绍道尔顿的原子论对化学科学发展的历史作用,培养学生科学探究意识
教学要点教学重点了解原子和分子的主要区别在于化学反应里是否可“分”
教学难点了解原子和分子的主要区别在于化学反应里是否可“分”
教学准备课件教学过程设计意图一、分子的构成师:你能用模型的方式来表示它们的过程吗
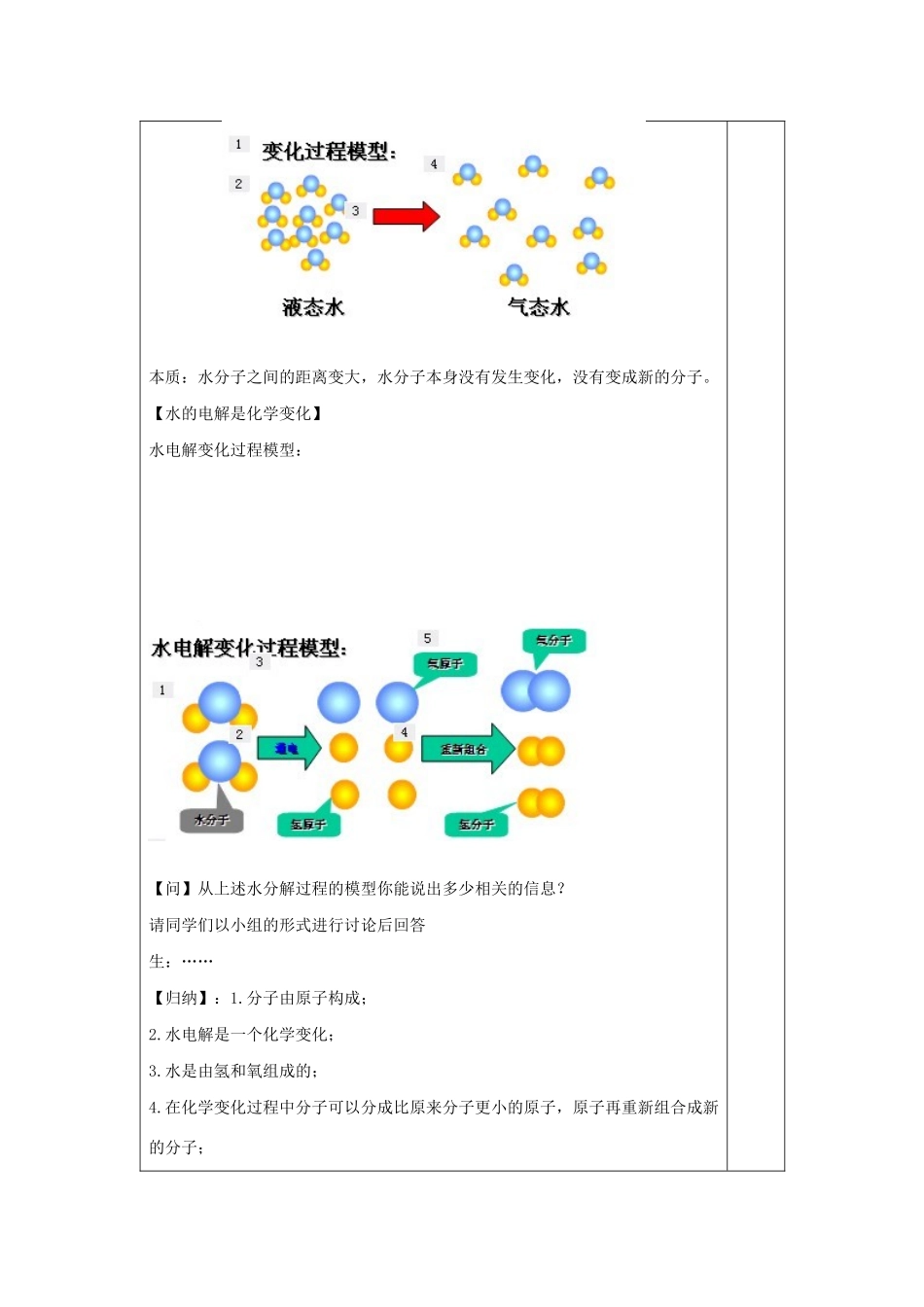
学生讨论完成【水的汽化和液化是物理变化】微观模型:本质:水分子之间的距离变大,水分子本身没有发生变化,没有变成新的分子
【水的电解是化学变化】水电解变化过程模型:【问】从上述水分解过程的模型你能说出多少相关的信息
请同学们以小组的形式进行讨论后回答生:……【归纳】:1
分子由原子构成;2
水电解是一个化学变化;3
水是由氢和氧组成的;4
在化学变化过程中分子可以分成比原来分子更小的原子,原子再重新组合成新的分子;5
在化学变化过程原子不能再分,原子是化学变化中的最小粒子;【小结】分子、原子及其主要区别1
分子在化学变化中可以再分,是保持物质化学性质的最小微粒
原子在化学变化中不能再分,是化学变化中的最小微粒3
原子和分子的主要区别在于化学反应里是否可“分”
师:了解了分子和原子的一些内容后接下来让我们深入思考如下问题【思考】分子能保持物质的化学性质,也能保持物质的物理性质吗
生回答【解析】分子能保持物质的化学性质,但不能保持物质的物理性质
如液态水变成冰时,此时水分子不变,水的化学性质就不变,但水的状态已变(即物理性质已变)
师:接下来请同学们仔细观察这幅图并填