课题第二章第三节化学平衡(第5,6课时)教学目标1.了解化学平衡图像的一般分析方法2.学会利用“先拐先平”“定一议二”等常用的方法,解决一些常见的化学问题
教学重点1.了解化学平衡图像的一般分析方法2.学会利用“先拐先平”“定一议二”等常用的方法,解决一些常见的化学问题
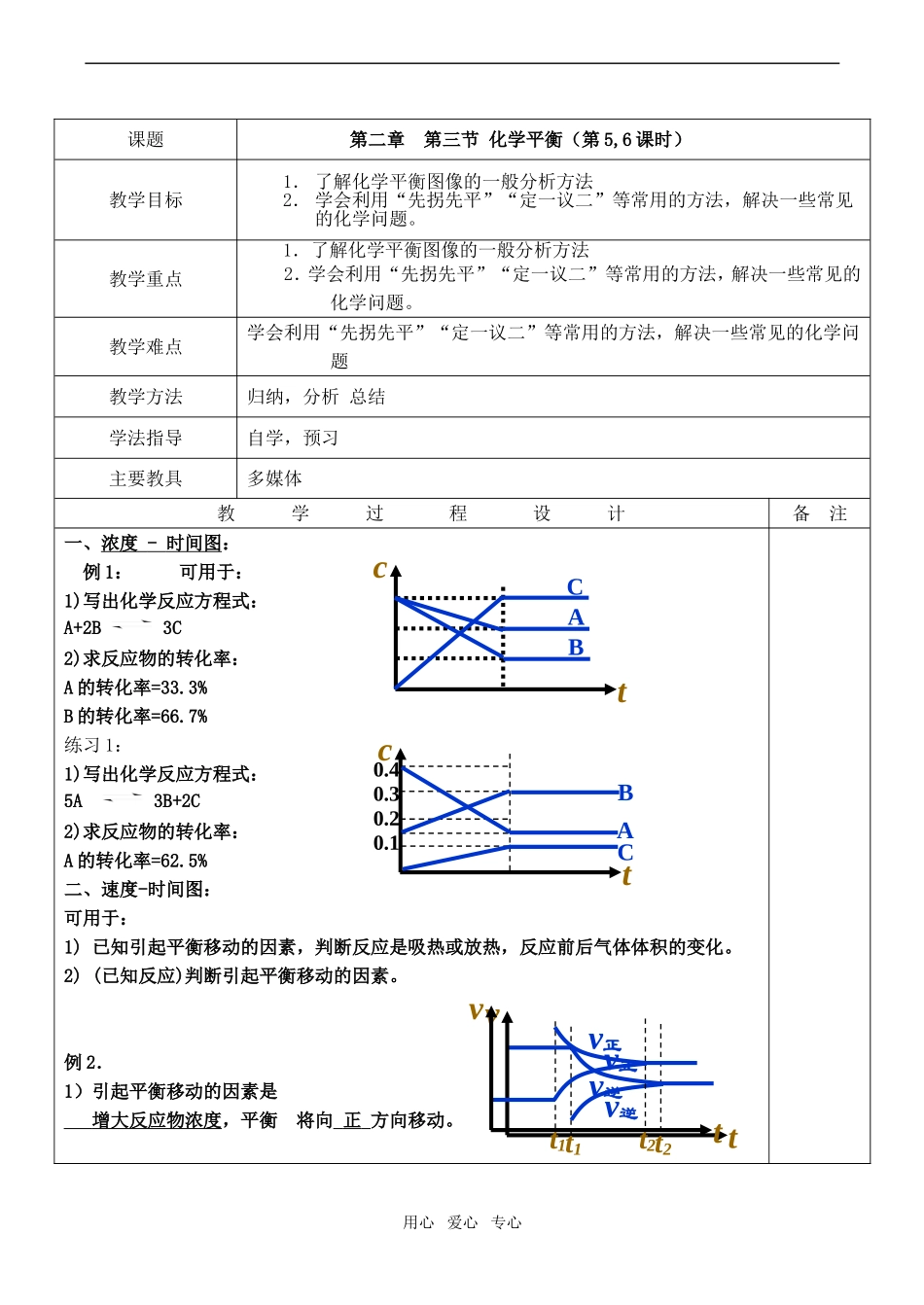
教学难点学会利用“先拐先平”“定一议二”等常用的方法,解决一些常见的化学问题教学方法归纳,分析总结学法指导自学,预习主要教具多媒体教学过程设计备注一、浓度-时间图:例1:可用于:1)写出化学反应方程式:A+2B3C2)求反应物的转化率:A的转化率=33
3%B的转化率=66
7%练习1:1)写出化学反应方程式:5A3B+2C2)求反应物的转化率:A的转化率=62
5%二、速度-时间图:可用于:1)已知引起平衡移动的因素,判断反应是吸热或放热,反应前后气体体积的变化
2)(已知反应)判断引起平衡移动的因素
例2.1)引起平衡移动的因素是增大反应物浓度,平衡将向正方向移动
用心爱心专心tcCABABCtc0
1tvv正v逆t1t2tvv正v逆t1t22)引起平衡移动的因素是减小生成物浓度,平衡将向逆方向移动
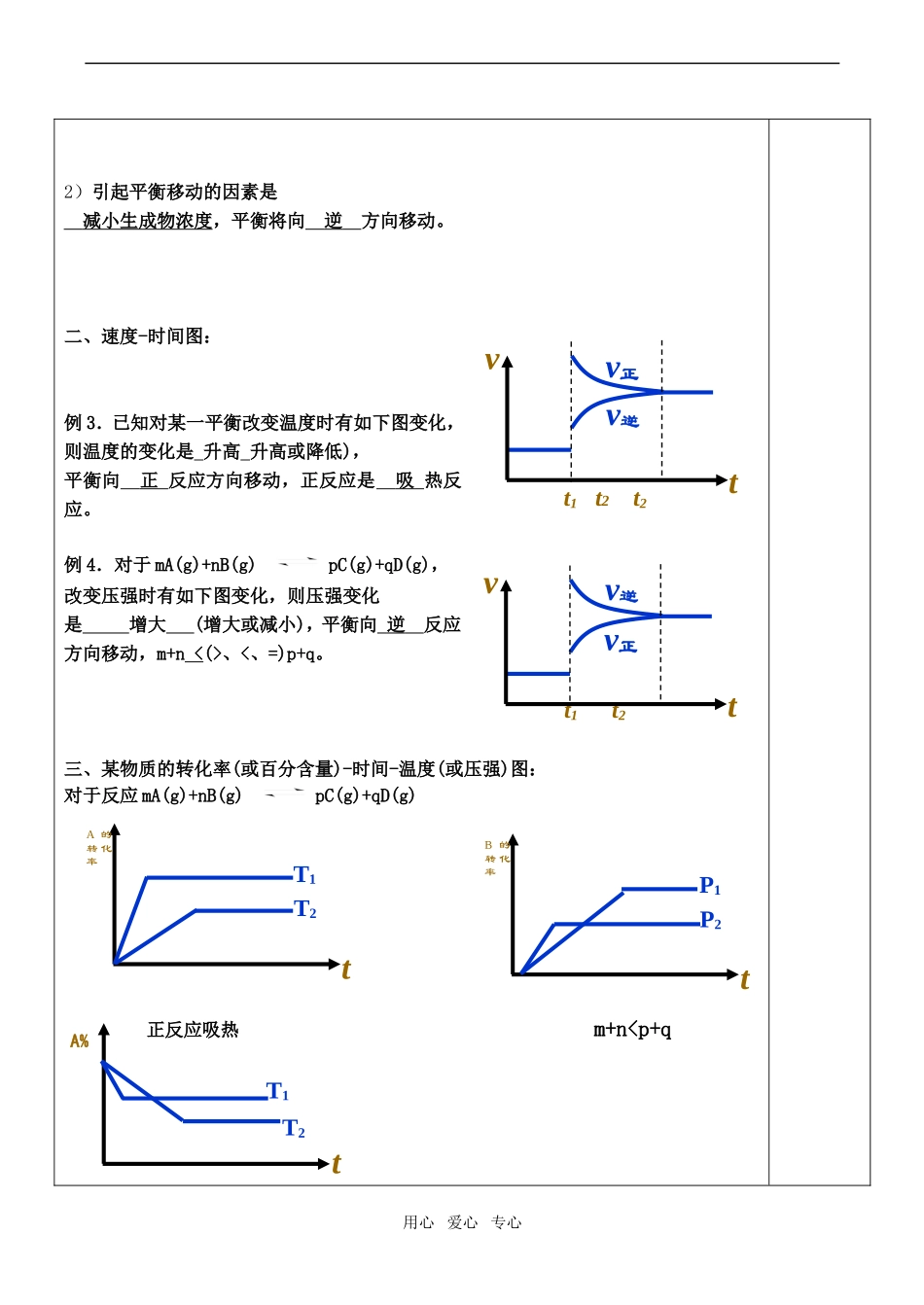
二、速度-时间图:例3.已知对某一平衡改变温度时有如下图变化,则温度的变化是升高升高或降低),平衡向正反应方向移动,正反应是吸热反应
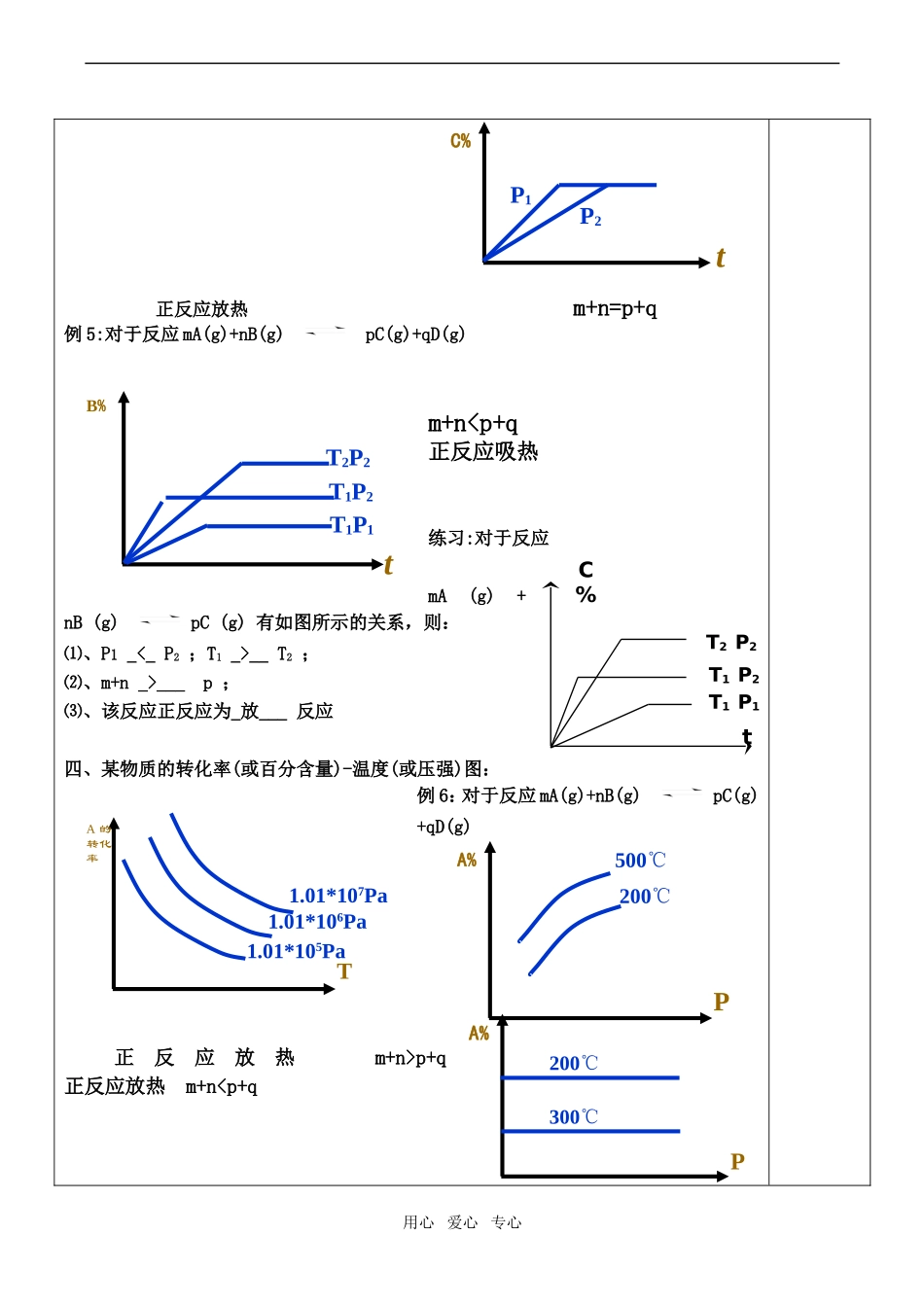
例4.对于mA(g)+nB(g)pC(g)+qD(g),改变压强时有如下图变化,则压强变化是增大(增大或减小),平衡向逆反应方向移动,m+n、P11;;②②m+nm+n与与pp的关系是的关系是m+n>pm+n>p;;③③TT11与与TT22的关系是的关系是TT22P110